Les techniques d’ostéo-intégration (Brånemark 1969/1977, Schroeder 1976/1981) ont radicalement fait évoluer le traitement de l’édentement.
Par la suite, les publications de suivi des patients traités par ces protocoles ont pu montrer des taux de survie implantaire élevés et une reproductibilité multicentrique (Adell et Coll, 1981).
Cette première évaluation passée, apparaissent plus tardivement les premiers consensus sur les critères de succès des implants dentaires (Albrektsson 1986). L’observance thérapeutique reste principalement basée sur le suivi radiographique des fixtures. Ainsi, une perte osseuse marginale, respectivement de 1 mm lors de la première année de mise en charge et de 0,1 mm/an pour les années suivantes, reste dans la marge de tolérance acceptée. La littérature abondante publiée concernait les modèles implantaires en titane essentiellement en technique enfouie ou non enfouie avec une mise en charge prothétique différée.
Le développement de l’implantologie lié à la demande croissante des patients et l’engouement de la profession a vu l‘émergence de concepts de traitement visant à réduire les phases de cicatrisation osseuse et conjointement, à proposer des conditions opératoires plus conviviales. Ce changement de paradigmes a parallèlement introduit des optimisations technologiques (état de surface, dessin implantaire, chirurgie guidée ou naviguée, moyens diagnostiques…) dont la finalité est l’immédiateté prothétique.
Les premières descriptions cliniques (Ericsson et al. (1986) décrivent les réactions inflammatoires autour des implants, mettant en évidence des similitudes avec les maladies parodontales. Par la suite, le colloque de l’European Workshop on Periodontology (1988) a formalisé les premières définitions des pathologies périimplantaires, distinguant la mucosite péri-implantaire (inflammation réversible) et la péri-implantite (avec perte osseuse).
Dans les années 90, Mombelli & Lang (1992) ont établi le concept des maladies péri-implantaires décrivant la microbiologie de la péri-implantite, comparant les bactéries pathogènes à celles de la parodontite.
La littérature scientifique abondante à ce sujet indique, au travers de la revue systématique menée par Derks & Tomasi (2015), des taux de mucosite et de péri-implantite à 22 % et 43 % respectivement. De plus, l’incidence de ces pathologies passe de 0,4 à 43,9 % sur une période de 3 à 5 ans (Dreyer, et al. 2018) indiquant la probabilité de l’occurence et le caractère non linéaire de l’évolutivité.
Les facteurs de risques généraux établis à ce jour retiennent les antécédents de maladie parodontale, le défaut de maintenance, le tabagisme, le diabète et l’obésité. Localement, le contrôle de plaque inadéquat, la mucosite, la malposition de l’implant, la conception prothétique déficiente ou la présence d’un excès de ciment de scellement dans le sulcus sont des éléments à charge.
Dans l’état actuel de nos connaissances, il est encore difficile d’énoncer des modalités thérapeutiques efficientes pour obtenir une guérison complète de ces lésions péri-implantaires signifiant une réostéointégretion.
Pour endiguer la progression de la péri-implantite, le recours à des moyens de décontamination de la surface implantaire assistée par laserthérapie Er-YAG (Para 2019, par nettoyage électrolytique (Galvosurge® , Schneider – 2018), par aéropolissage a pu montrer des résultats inégaux et nécessite encore une observation plus prolongée.
L’apport de l’implantoplastie préalable à une technique de régénération osseuse a été envisagée (Monje et al. 2022).
Cependant, au-delà de toutes les propositions curatrices, la Fédération Européenne de Parodontologie (EFP) n’a établi aucune recommandation directe pour les deux approches non-chirurgicales et chirurgicales et insiste préférentiellement sur les axes de prévention primordiale et primaire. (Herrera et al. 2023).
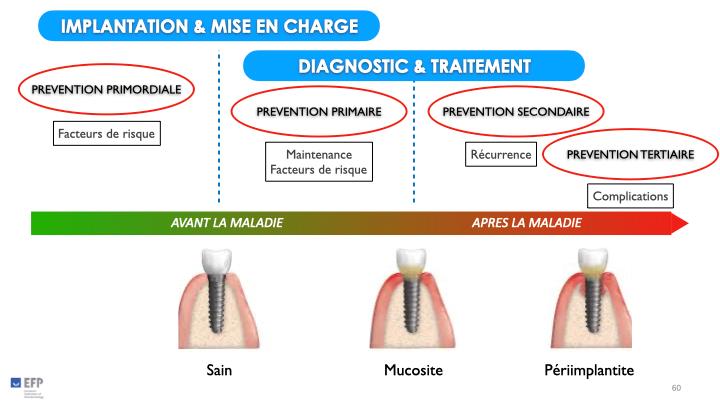
La prévention primordiale consiste notamment en une maitrise des facteurs de risque aussi bien généraux
que locaux. L’aménagement pré-implantaire in situ en optimisant le volume des tissus durs (Capelli M et al.
2013) et des tissus mous (Linkevicius T et al. 2015).
La prévention primaire repose sur une mise en oeuvre d’un suivi et d’une maintenance professionnelle
rigoureuses (Rocuzzo A et al. 2022).
Ces réflexions doivent être complétées par une prise en compte du concept implantaire initial.
Effectivement, la variété des systèmes implantaires, des connexions et des modes opératoires associés a
pu montrer des différences quant à la stabilité des composants péri-implantaires. Dans ce sens, un
consensus se dégage de plus en plus sur un modèle biologiquement compatible (Rompen E 2012).
Très peu abordé dans ces travaux de l’EFP, le recours à des implants en zircone pourrait devenir une option
préventive de la péri-implantite. Bien que les implants céramiques étaient déjà proposés dans les années
60, l’avènement de la full-zircone stabilisée par de l’yttrium (YTZP) a redistribué les points d’intérêt. En
première intention, les points à considérer pour cette famille d’implants peuvent être résumés en 4 points:
1. BIOCOMPATIBILITÉ ÉLEVÉ
– Matériau non métallique (céramique), idéal pour les patients allergiques ou sensibles aux métaux.
– Réduction des réactions inflammatoires par rapport aux implants en titane chez certains patients.
2. ESTHÉTIQUE SUPÉRIEURE
– Couleur blanche proche de celle des dents naturelles, évitant les reflets grisâtres visibles au
niveau des gencives (surtout dans les zones antérieures).
3. RÉSISTANCE ET DURABILITÉ
– Flexibilité et résistance à la fracture grâce à des procédés de fabrication brevetés (ex. zircone
stabilisée ou nanostructurée).
– Résistance à la corrosion dans l’environnement buccal humide, contrairement aux métaux.
4. OSTÉOINTÉGRATION OPTIMISÉE
– Traitements de surface brevetés (micro- ou nanostructures, bioactivation) pour favoriser
l’adhésion osseuse, rivalisant avec le titane.
– Design spécifique (forme, porosité) améliorant la stabilité primaire et secondaire.
LE CONCEPT IMPLANTAIRE PATENTTM (ZIRCON MEDICAL AG)
Conjointement aux caractéristiques évoqués pour les implants zircone, le système implantaire que nous
avons sélectionné conforte notre réflexion sur l’anticipation des complications biologiques périimplantaires
dans la mesure où il répond positivement aux critères recherchés :
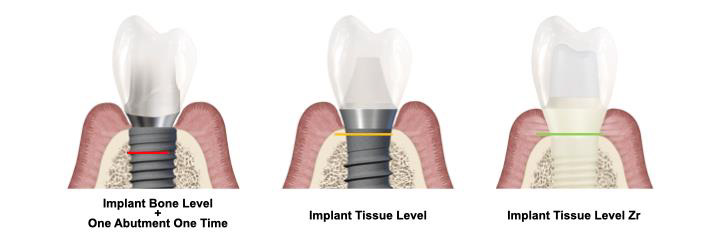
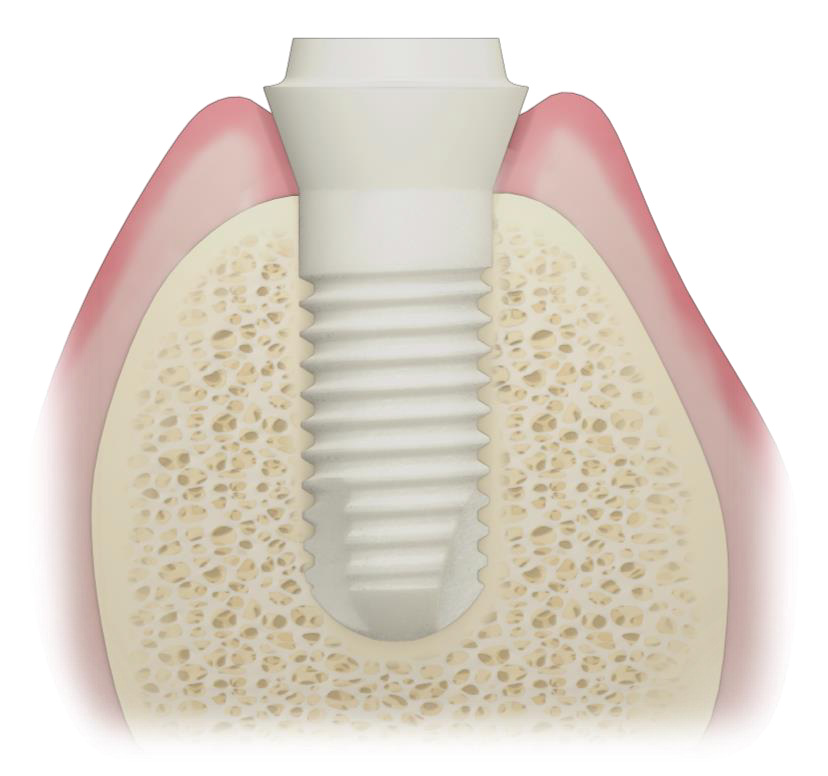
 Le concept implantaire est de type tissue level (supra-crestal). Le positionnement vertical est classique. Pour répondre à l’anatomie cervicale, la limite de finition peut être modifiée intraoralement par une instrumentation
Le concept implantaire est de type tissue level (supra-crestal). Le positionnement vertical est classique. Pour répondre à l’anatomie cervicale, la limite de finition peut être modifiée intraoralement par une instrumentation
rotative adaptée Le corps endosseux présente une surface poreuse hydrophile (Ra = 5,7μm) favorisant un taux de contact os-implant de 70 % après 4 semaines (Glauser R et al. 2022).
Le procédé de sablage est effectué avant le frittage final.
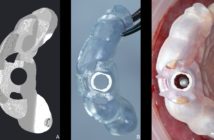
L’implant PatentTM est considéré comme un système en deux pièces.
Le pilier ou inlay core en fibre de verre est collé à la fixture.
L’ensemble assemblé constitue le principe du monobloc hermétique. La stabilité de la restauration prothétique est assurée par l’effet de sertissage (ferrule) procurée par la portion tronconique supracervicale (1,6 mm).
En fait, la zone d’intérêt de cet implant réside dans sa portion transmuqueuse. Cette dernière présente une rugosité obtenue mécaniquement (Ra = 1,25 μm). Ainsi, probablement à l’encontre des opinions préétablies, cet état de surface favorise l’adhésion rapide des tissus mous. Les études histologiques,
menées à ce jour, démontrent cette cinétique entre la formation du biofilm et l’obtention d’un joint sulculaire. Cette « inhibition compétitive » réduit la pénétration de la plaque bactérienne pathogène combinée au concept supra-crestal de l’implant expliquerait une évolution critique de la maladie périimplantaire.
Cette hypothèse, qui a conditionné notre choix clinique, a été étayée par deux études pertinentes :
1- Brunello et al. 2022 .
- 94,1 % taux de survie (1 implant perdu après 110 mois).
- Aucune fracture.
- Indices cliniques identiques entre 2-9 ans de suivi.
- Profondeur de poche : 3 mm
- Niveaux tissulaires stables après 9 ans (MR < 1mm pour . tous les implants)
- Mucosite 13 %
- Aucune péri-implantite n’a été observée selon les critères définis (Berglund et al.)
2- Karapataki S et al. 2023
- Patients malades (maladies systémiques, fumeurs, parodontite, médications…)
- Implants immédiats dans sites d’extraction ou cicatrisés. Mises en charge différées ou immédiates
appliquées. Sites greffés simultanément si nécessaire. - 6 implants montrent des pertes osseuses > 0,7 < 2,1 mm Aucune perte osseuse progressive rapportée.
- 3 patients (9 implants) présentent des signes de mucosite, pas de poches sur les autres implants.
- 11% de mucosite
- Aucune péri-implantite n’a été observée selon les critères définis (Berglund et al.)
En conséquence, les implants endo-osseux zircone peuvent être indiqués chez des patients malades avec
peu de complications biologiques dans le temps.
Cette option peut se situer entre la prévention primordiale et la prévention primaire selon les
recommandations de l’EFP dans la mesure où elle assure une muco-intégration, donc un joint étanche
optimisé, barrière efficace à la colonisation du biofilm. Evidemment, l’indication pour les patients
susceptibles à la maladie péri-implantaire s’impose.
L’utilisation de l’outil Implant Disease Risk Assessment (IDRA) pour évaluer la susceptibilité est une
contribution intéressante pour la prise de décision (Heitz-Mayfield L et al. 2019).
Pour illustrer nos propos, nous vous proposons un cas clinique avec un recul à deux ans montrant l’intérêt
biologique et esthétique des implants Zircone Patent pour le remplacement d’une dent unitaire en secteur
antérieur.
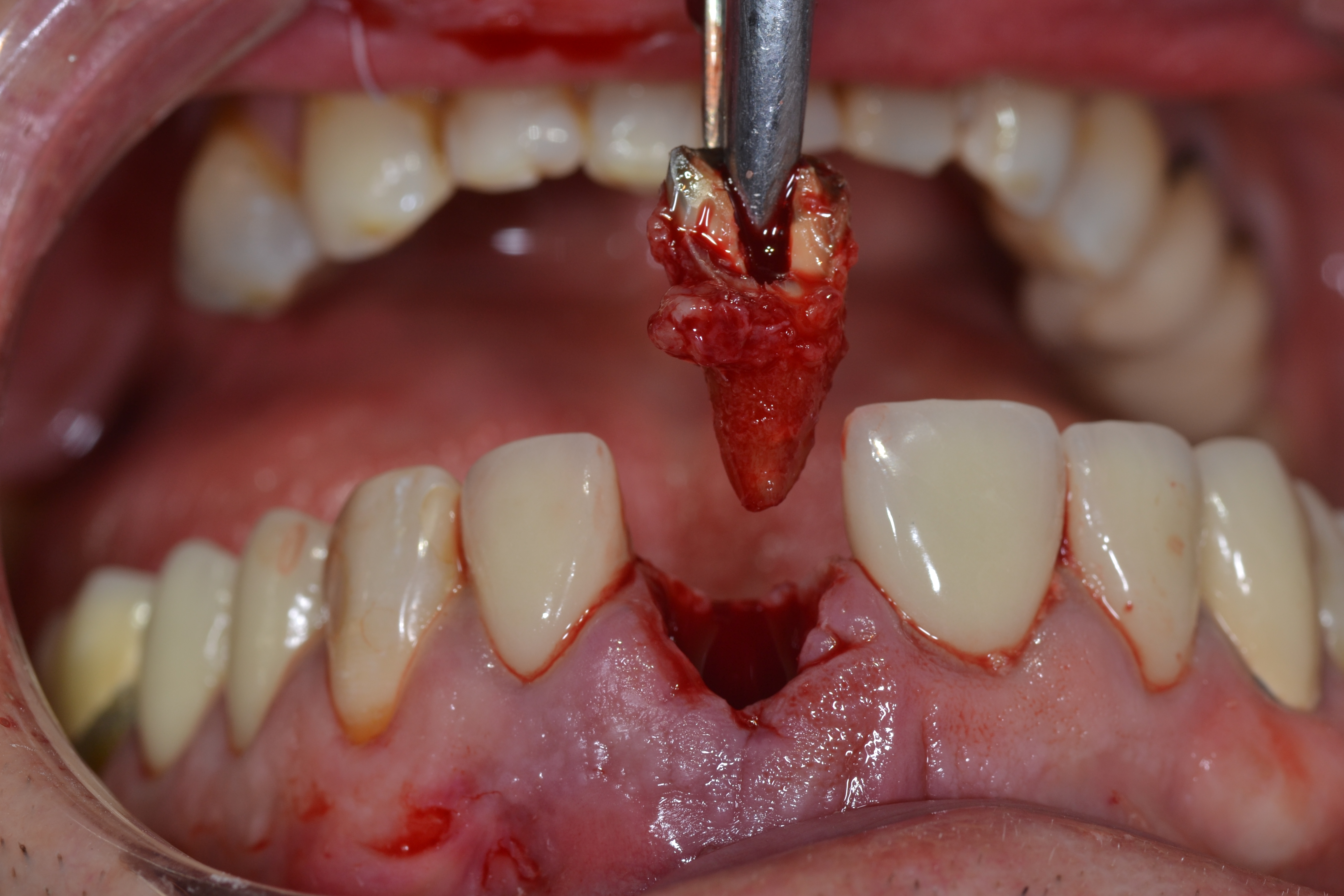
Ce cas montre le concept de muco-intégration dans une situation de fracture radiculaire d’une dent
unitaire (incisive centrale maxillaire gauche) au maxillaire avec altération de la corticale osseuse
vestibulaire associée à une atteinte du complexe mucogingival.
Nous avons opté dans ce cas pour un traitement d’extraction implantation immédiate d’un implant
zircone PatentTM avec mise en esthétique immédiate.
Un comblement du gap buccal a été réalisé avec de l’os autogène de récupération (obtenu lors du forage)
et un renforcement mucogingival a été décidé en suturant en direction cervicale un greffon conjonctif
issu d’un prélèvement palatin compensant le « V » vestibulaire ; le tout dans le même temps chirurgical.
Nous avons observé dès les premières semaines le remodelage du feston gingival et avons constaté au
bout de 3 mois un bon esthetic score malgré une situation initiale assez péjorative où avec une
technique d’implantation classique en titane nous aurions dû extraire la dent et temporiser en faisant
une préservation d’alvéole puis dans un second temps poser l’implant en y associant une ROG et un
remaniement de tissus mous sans être certains d’obtenir un si bon résultat final sur le plan biologique
et esthétique.
De plus, utiliser un implant de couleur blanche sur un parodonte fin permet une meilleure réfraction de la
lumière avec un aspect plus esthétique de la gencive
et du rebord gingival qui dans le temps ne risque pas de se colorer avec halo grisâtre comme on peut le
voir parfois à moyen et long terme sur les implants titane.
Par ailleurs, savoir que l’implant zircone PatentTM ne présenterait pas statistiquement selon l’étude de
Karapataki de risque de péri-implantite à 12 ans, c’est pour nous cliniciens un critère de choix pour
implanter les patients jeunes en secteur esthétique ; patients qui devront tout au long de leur vie avoir une
stabilité des tissus osseux et muqueux autour des implants.
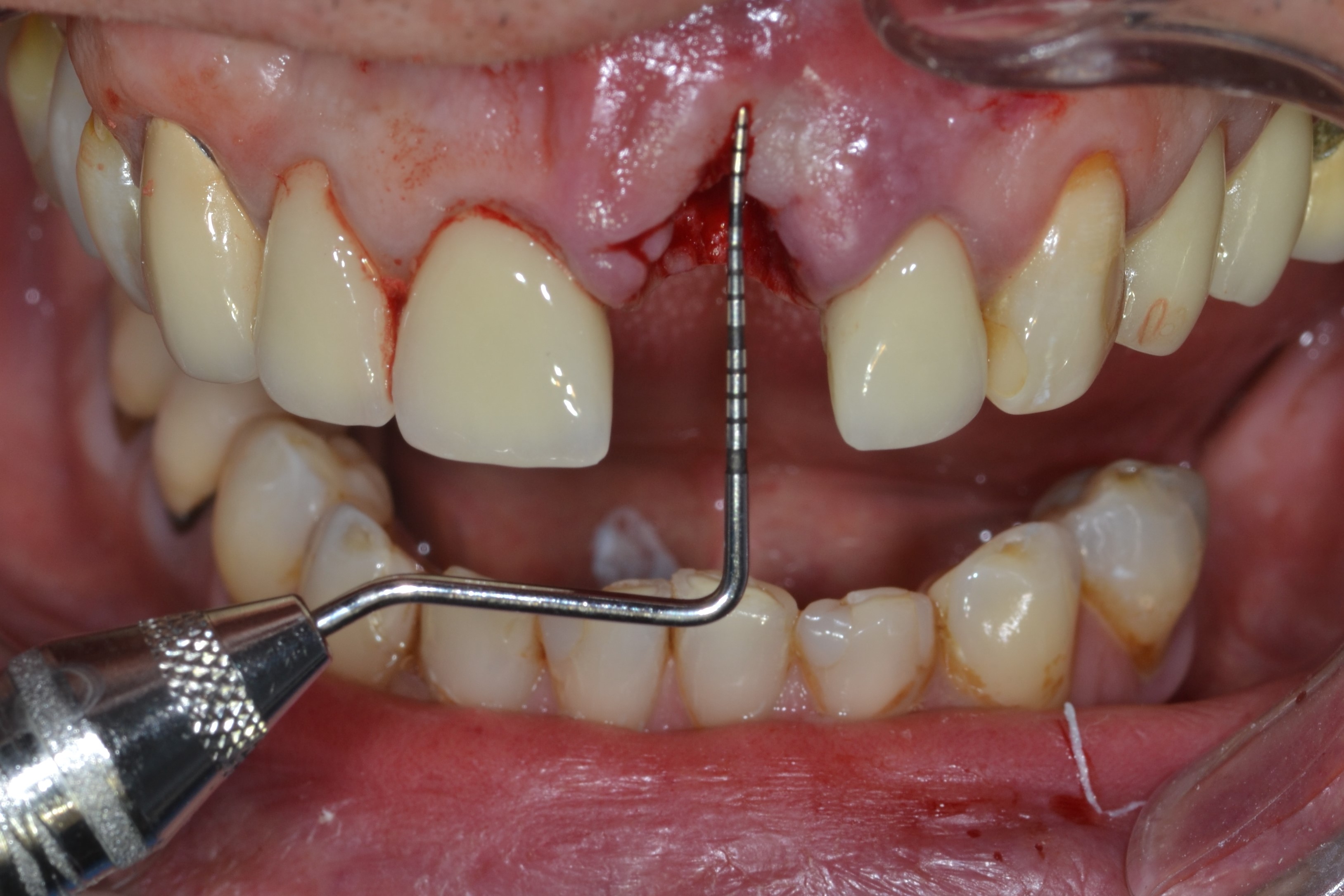
Fig.2 : la sonde parodontale pointe le défaut en « V » buccal lié à la fonte de la corticale vestibulaire
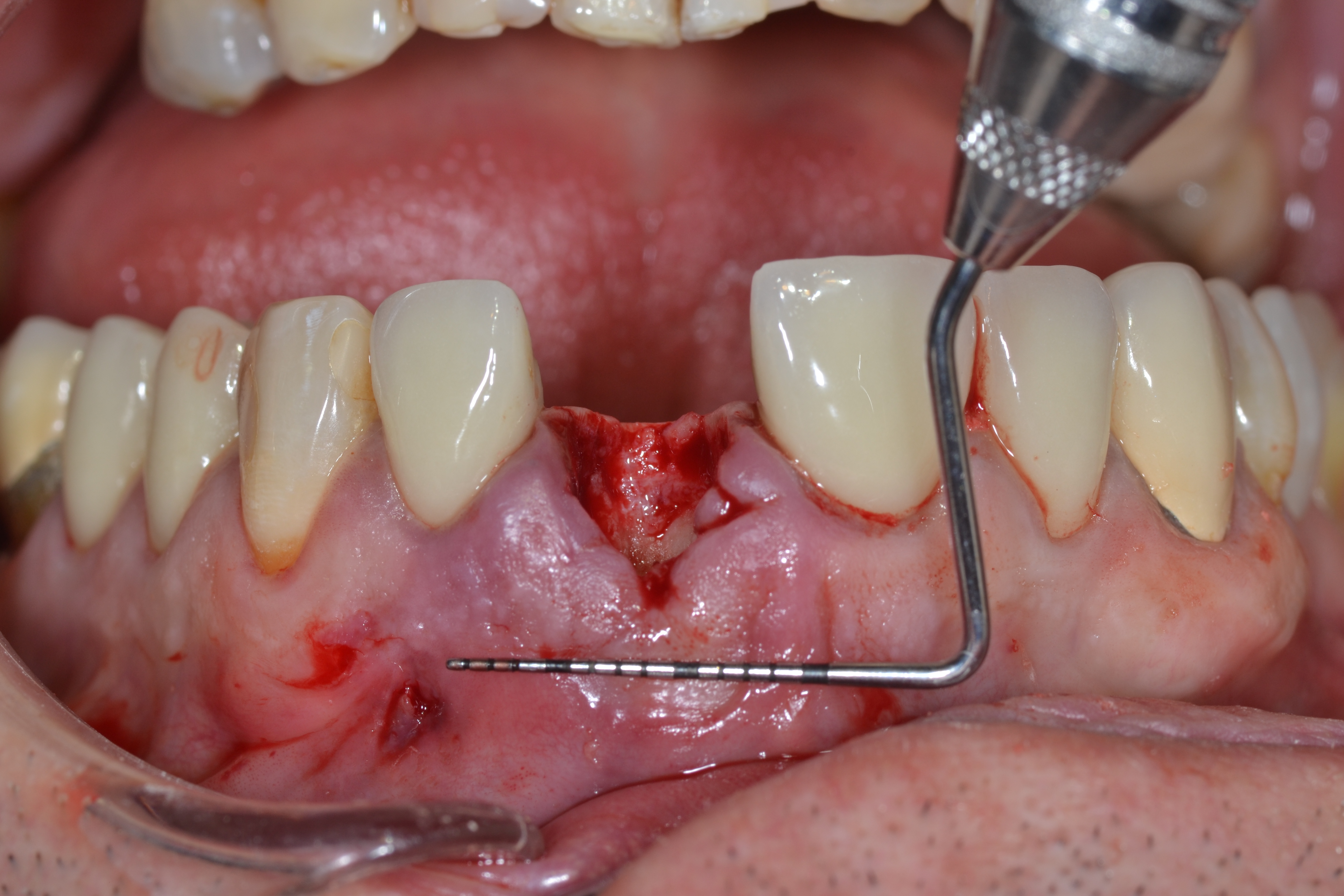
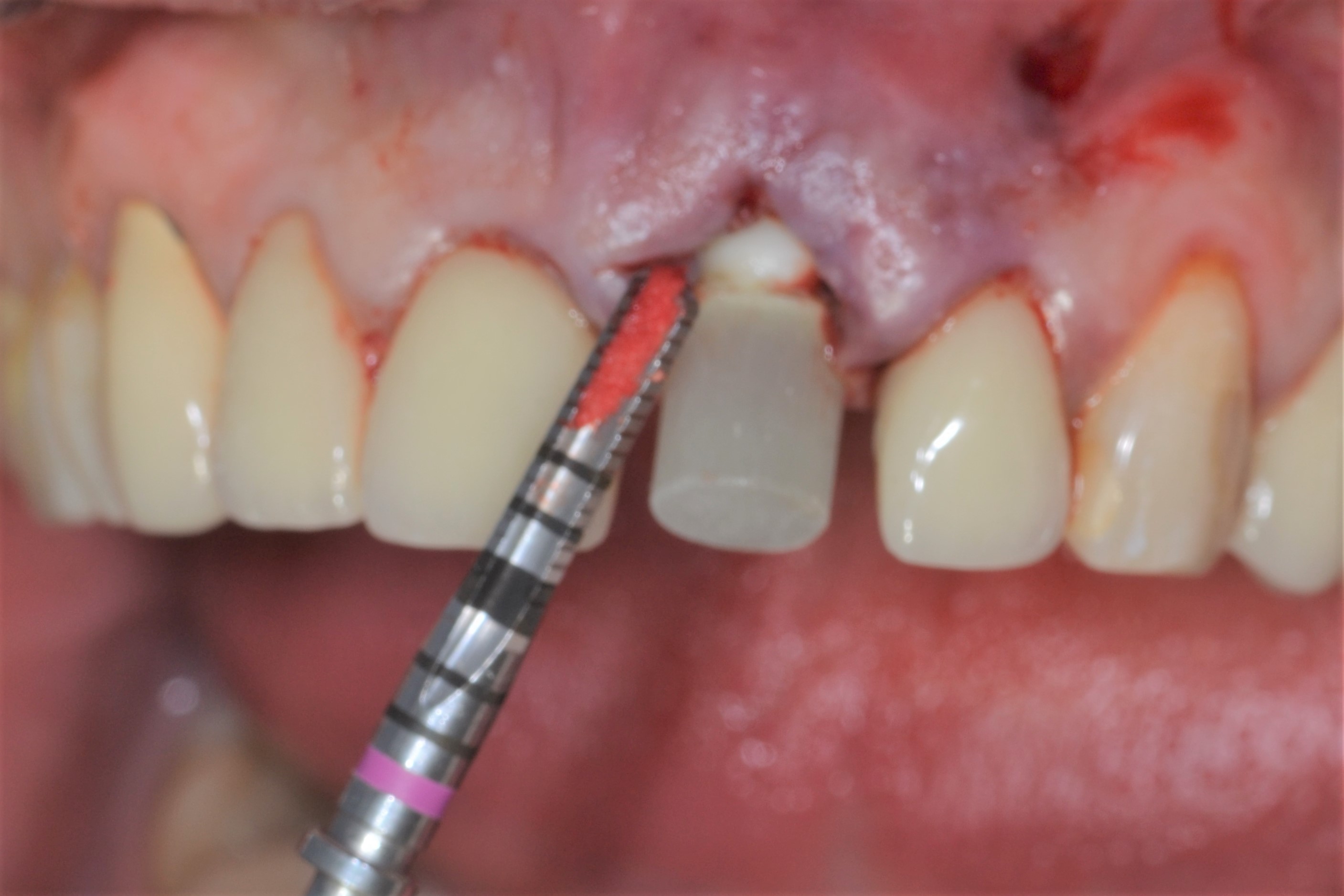
Fig.3 : la sonde parodontale objective de site de réception de la greffe conjonctive prévue en tunnélisation.
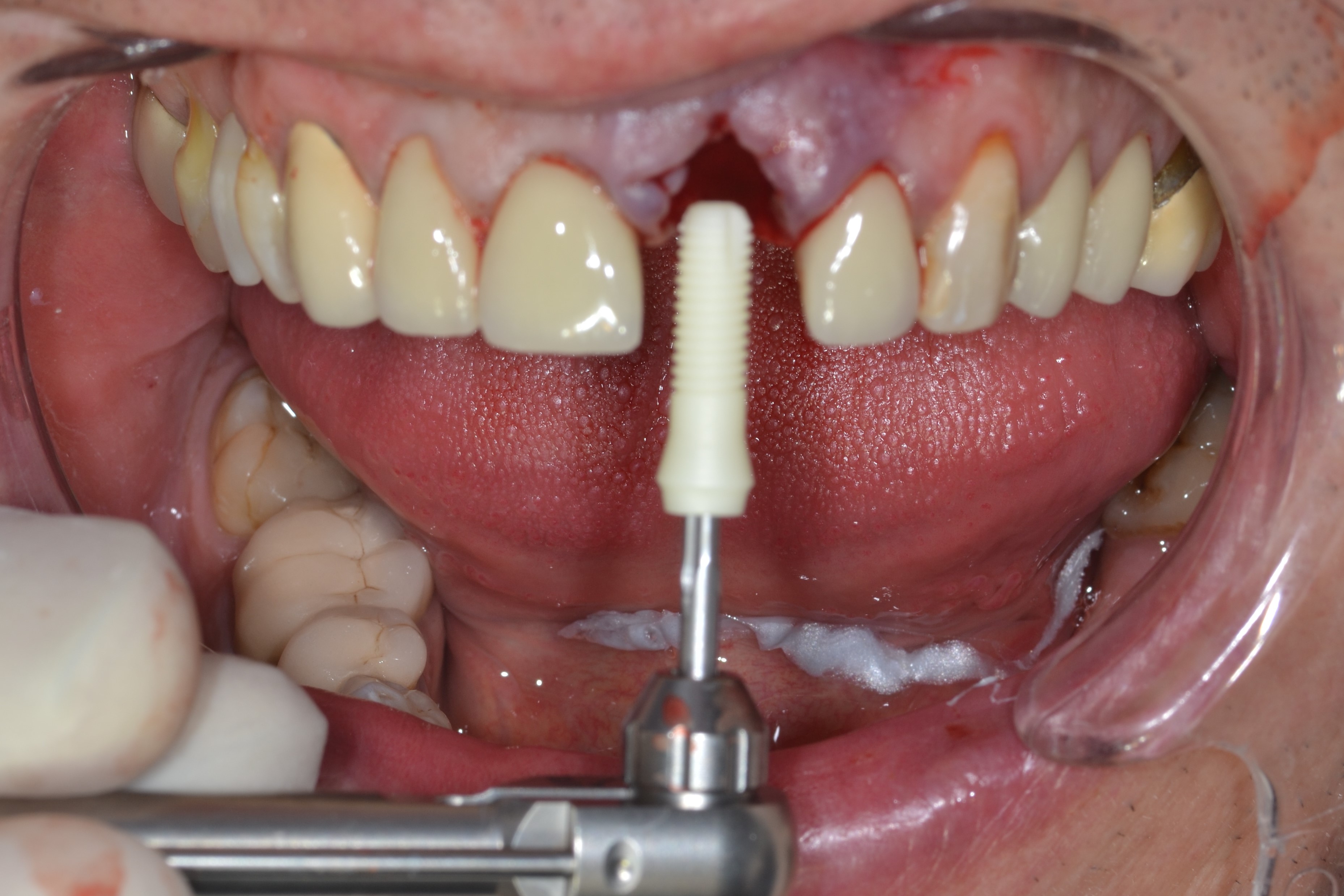
Fig.4 : vue buccale de l’implant PatentTM dans l’axe de l’alvéole immédiatement après l’extraction de la 21, le curetage et la désinfection de l’alvéole.
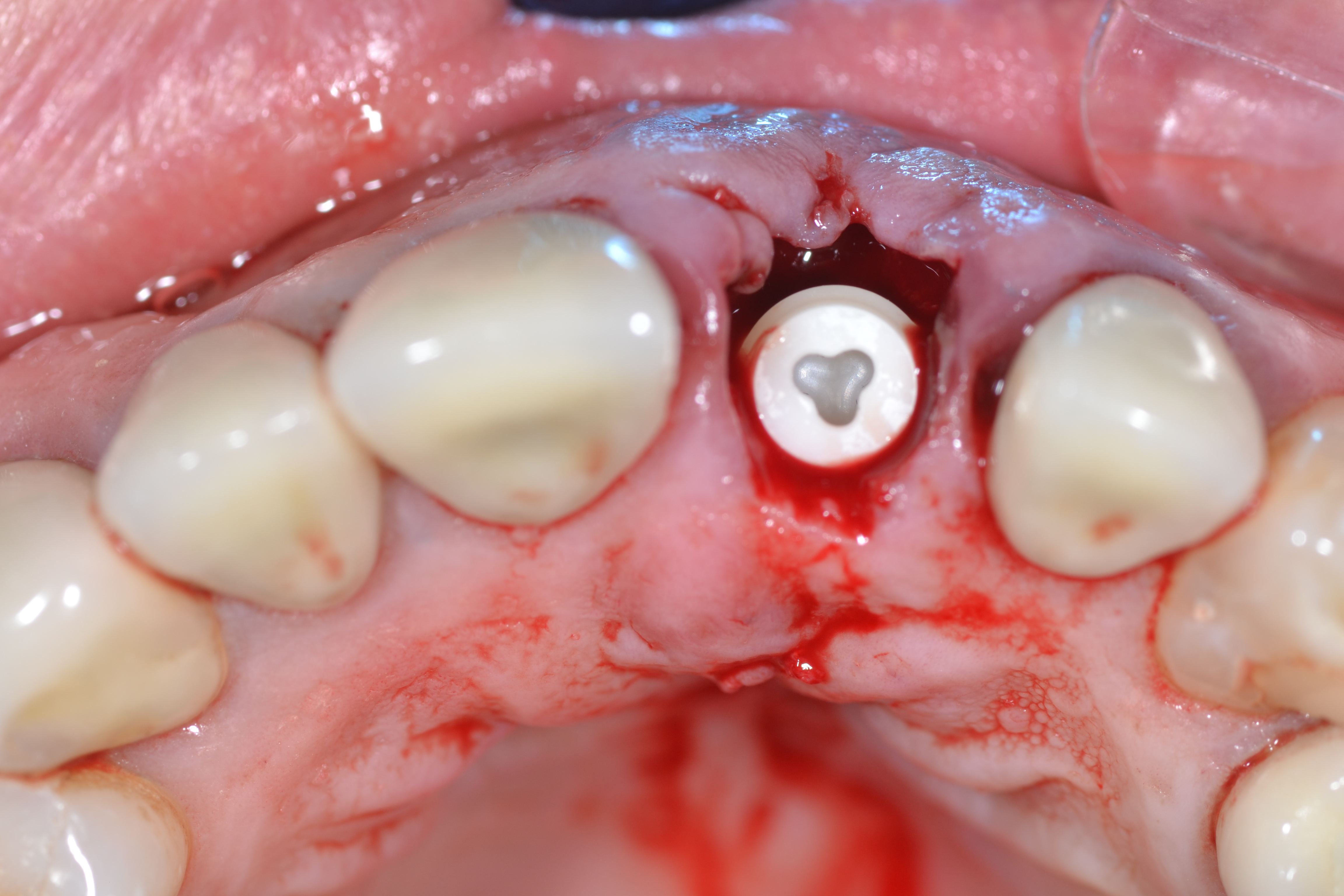
Fig.5 : vue occlusale de l’implant PatentTM avec sa connexion 3C près extraction/ implantation immédiate.
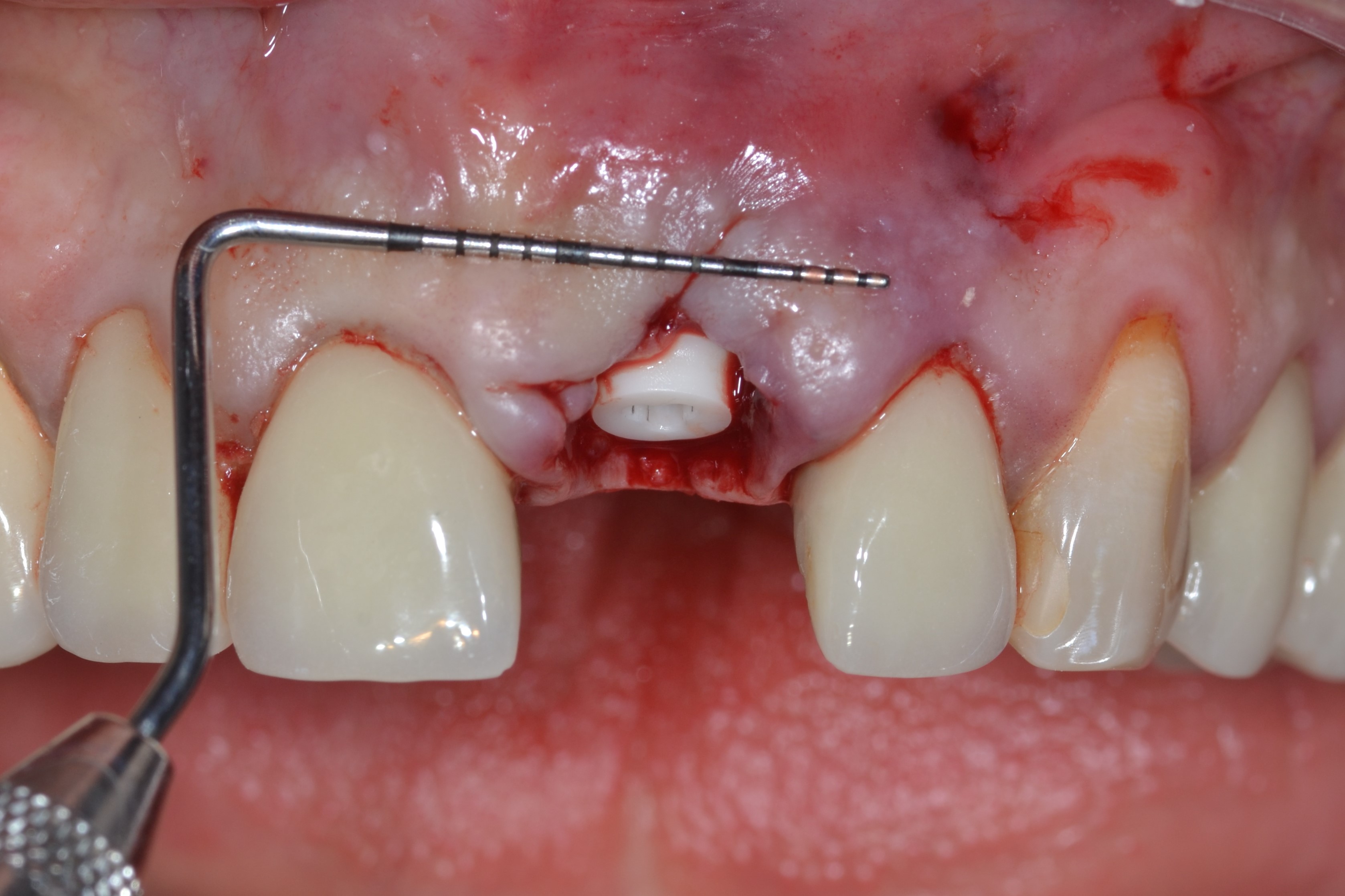
Fig.6 : vue buccale de l’implant où l’on voit la partie supragingivale du Tissue Level avec son effet ferrule sur le futur pilier implantaire.
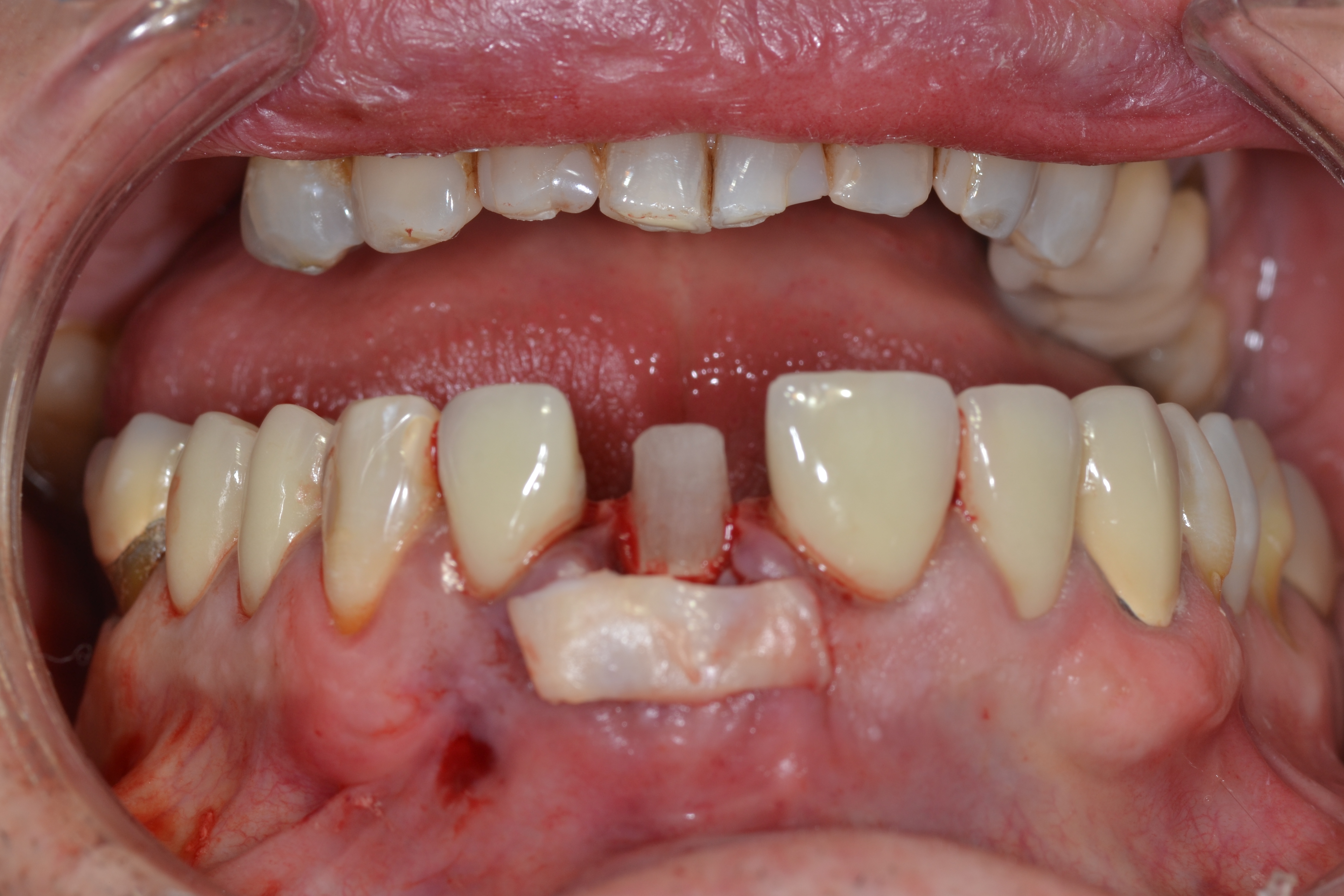
Fig.8 : positionnement du greffon conjonctif en regard de la zone tunnélisée autour de l’implant sur la zone marginale.
.
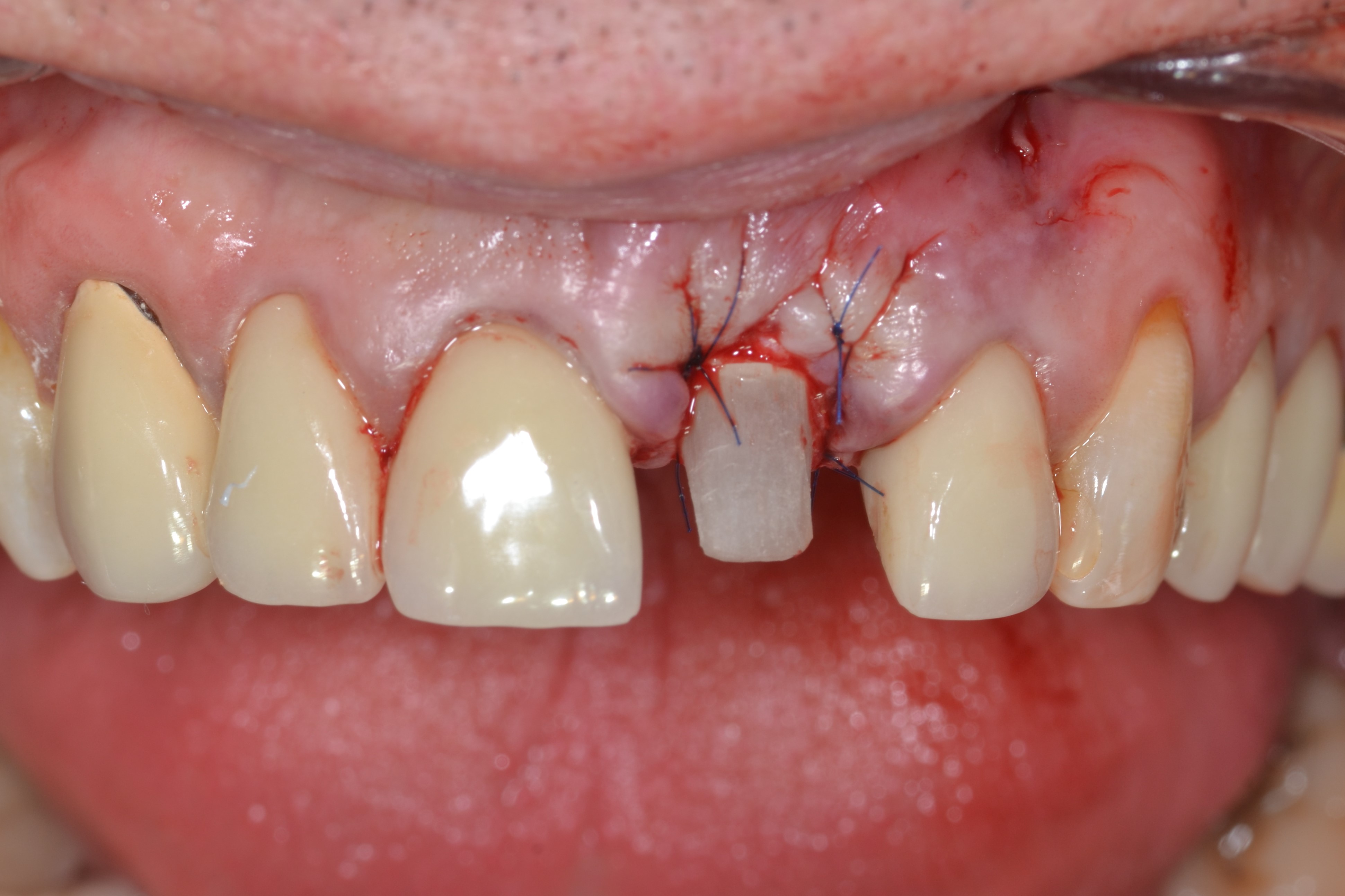
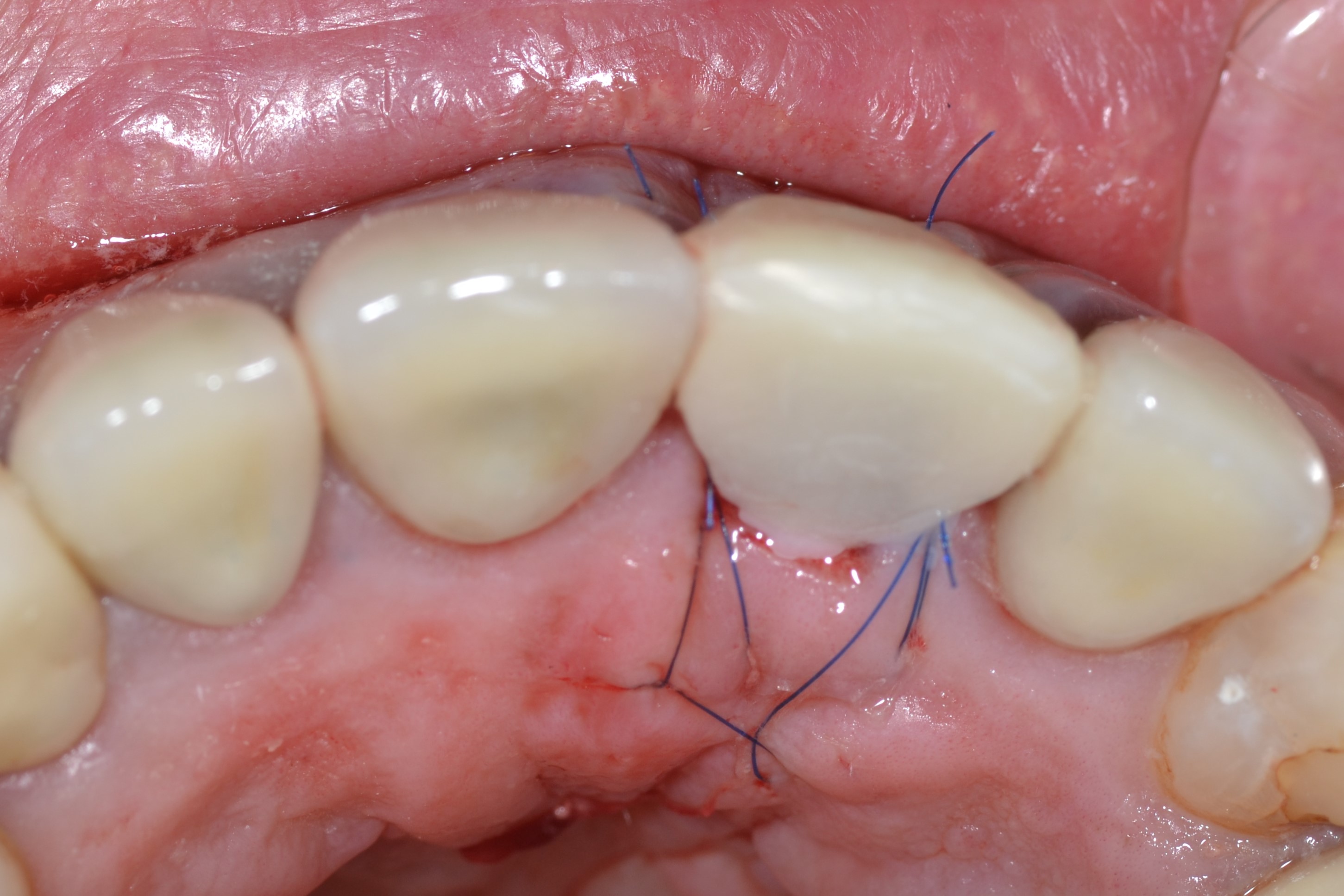
Fig.9 : sutures 6-0 tractées autour du pilier (points suspendus) pour positionner le greffon conjonctif coronairement et renforcer la zone péri-implantaire.
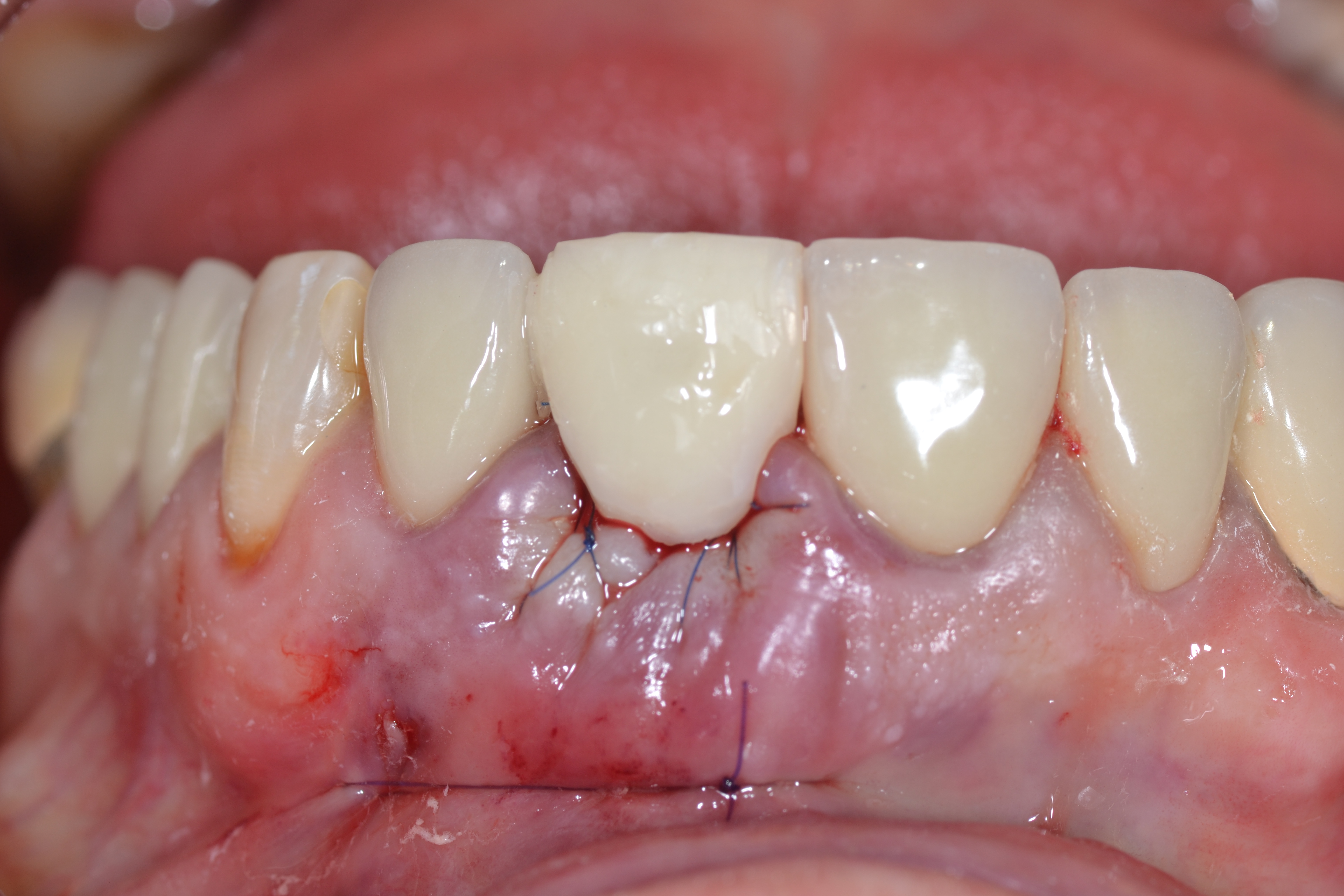
Fig.10 : positionnement de la couronne transitoire en résine de laboratoire et scellement au ciment semi-permanent « Implantlink » sur le pilier en fibre de verre.
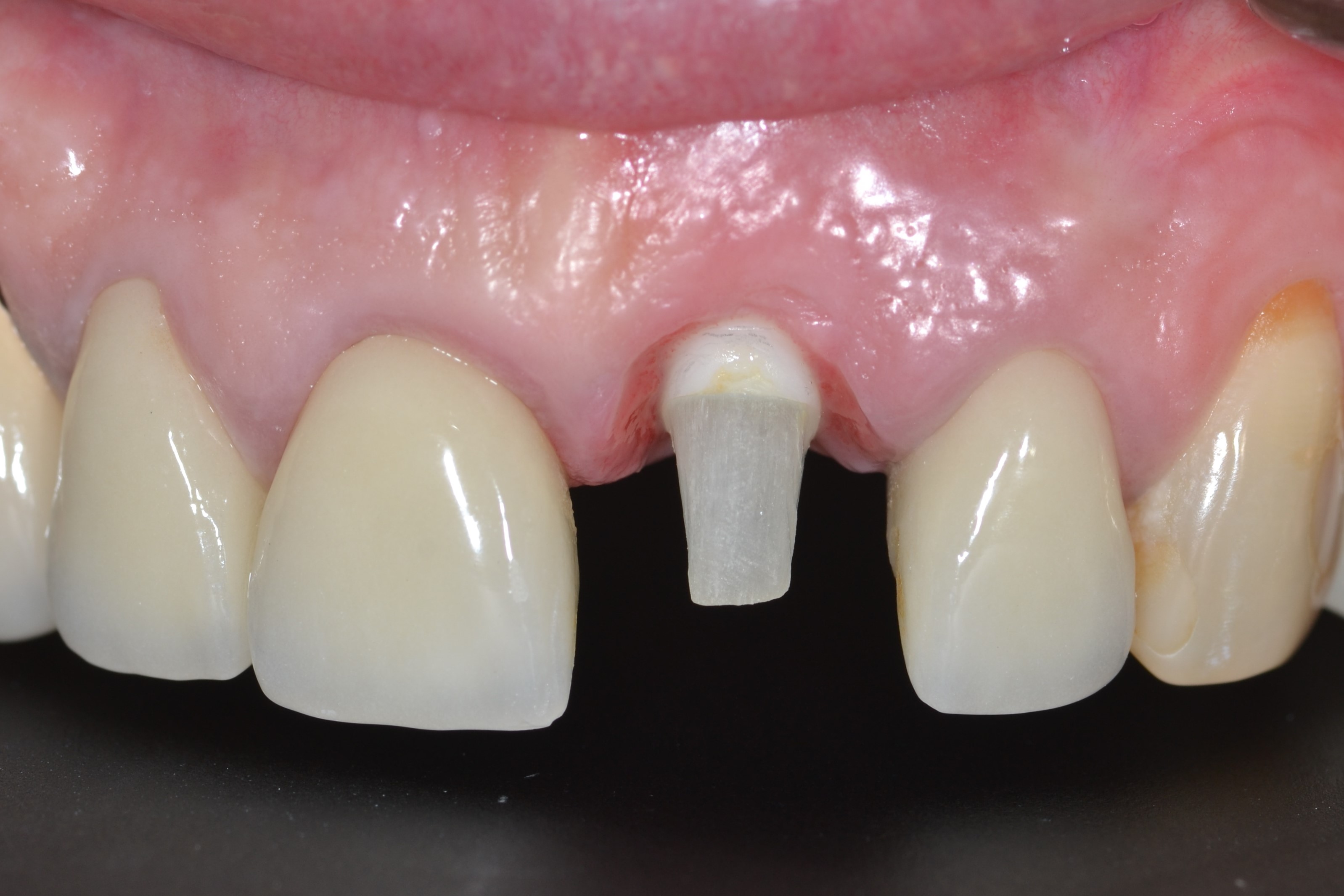
Fig.12 : vue buccale du rebord marginal montrant la présence des papilles autour de l’implant en zircone PatentTM ainsi que l’excellente muco-intégration de la zone cervicale.
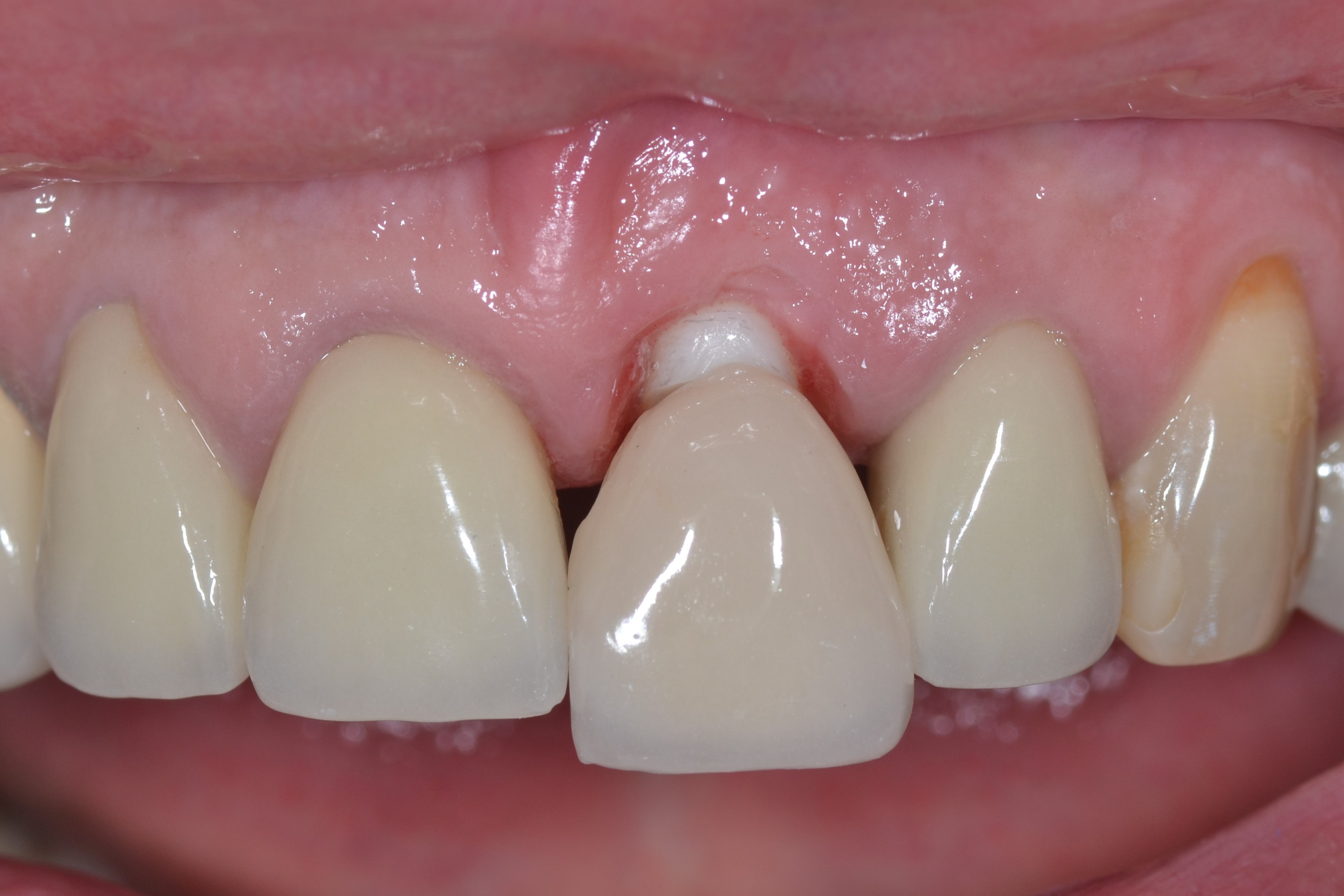
Fig.13 : vue buccale de la couronne définitive en céramique feldspathique avant collage autour du pilier PatentTM.
.
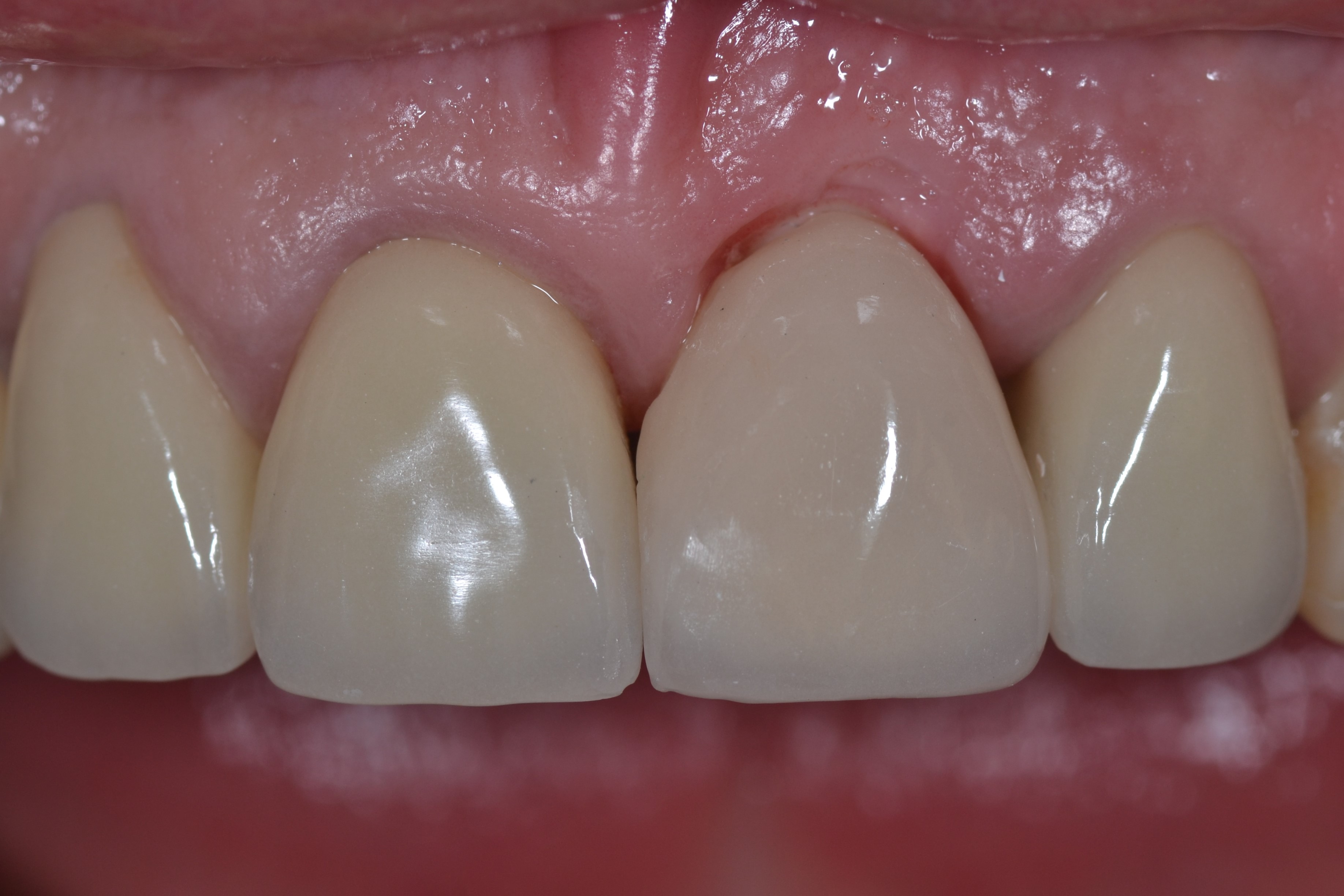
Fig.14 : couronne le jour du collage montrant un léger retrait gingival autour de la céramique à J.0.
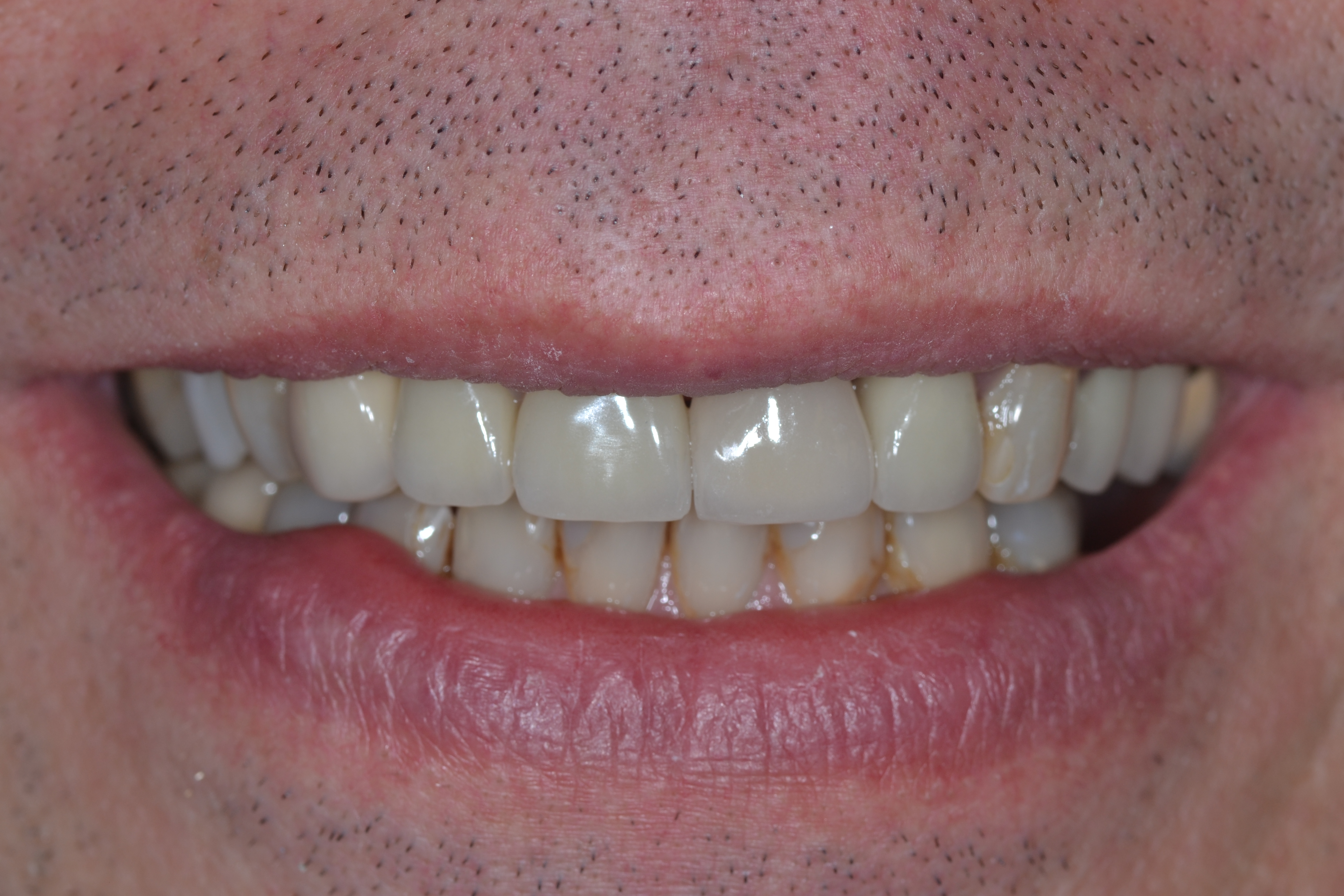
Fig.15 : sourire du patient le jour de la pose de la céramique montrant un parfait biomimétisme avec les dents naturelles.
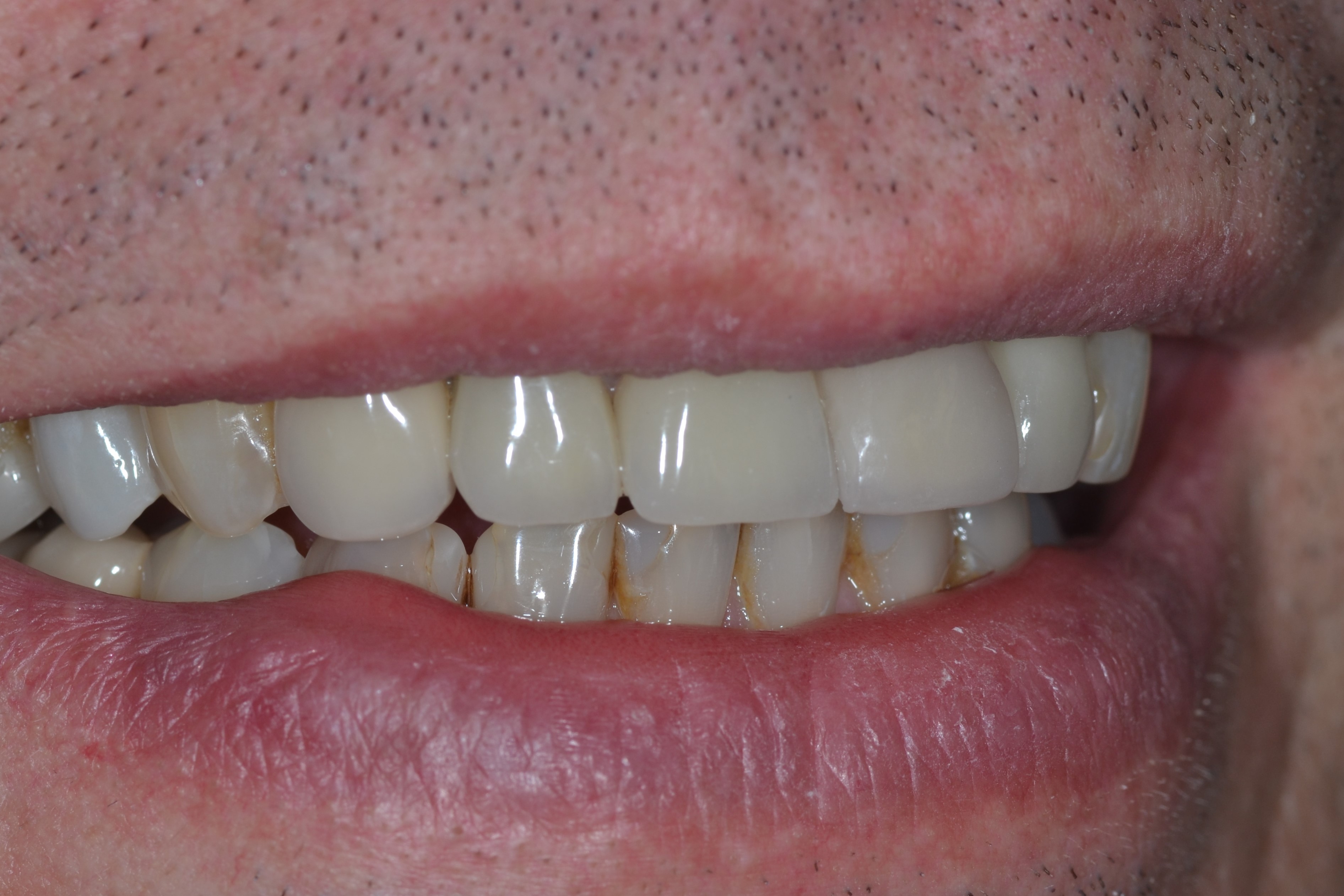
Fig.16 : la dent implantaire montre une luminosité une teinte et une saturation identique aux dents naturelles.
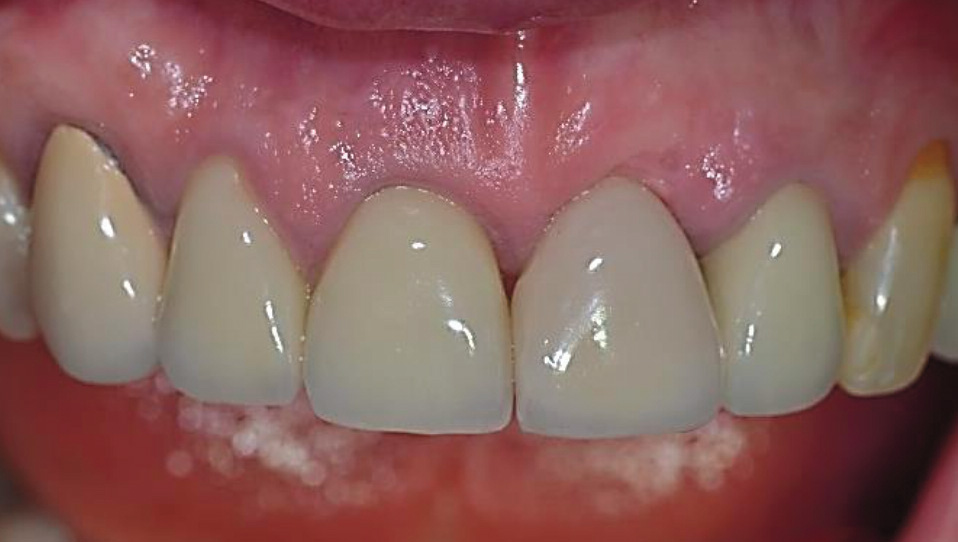
Fig.17 : à deux ans postopératoire on voit que les tissus mous se sont positionnés parfaitement au niveau de la zone marginale de l’implant PatentTM avec la présence des deux papilles et un creeping attachment au niveau du zénith du feston gingival malgré une situation avant extraction péjorative.
CONCLUSION
La prévention des maladies péri-implantaires par l’indication de ce système implantaire zircone nous a
semblé cohérente tant le comportement des tissus mous en suivi post-opératoire et à deux ans nous paraît conforme à la littérature publiée.
Dans cette perspective, les patients présentant des antécédents de maladie parodontale susceptibles de déclencher une pathologie péri-implantaire apparaissent comme des candidats potentiels pour cette alternative. Cependant, une période d’observation plus longue viendra confirmer l’hypothèse thérapeutique.
BIBLIOGRAPHIE
– T Albrektsson et al. The long-term efficacy of currently used dental implants: a review and proposed criteria of success Int J Oral Maxillofac Implants 1986 Vol. 1, No. 1 (11 – 25)
– Ericsson, I., et al. “The effect of antimicrobial therapy on peri-implantitis lesions. An experimental study in the dog. Cli n Oral Implant Res 1986, 7:320–328
– Mombelli, A., & Lang, N. P. The diagnosis and treatment of peri-implantitis.”Periodontol 2000 1994, Jun:17:63-76
– Derks J & Tomasi C. Peri-implant health and disease. A systematic review of current epidemiology J Clin Periodontol. 2015 Apr;42 Suppl 16:S158-71. doi: 10.1111/jcpe.12334
– Dreyer H et al. Epidemiology and risk factors of peri- implantitis: A systematic review. J Periodontal Res. 2018;53(5): 657–81
– Derks J et al. Effectiveness of implant therapy analyzed in a Swedish population: prevalence of peri- implantitis. J Dent Res 2016;95:43-45
– Giovannoli JL & Renverra S Péri-implantites Quintessence Publishing 2012
– Para A Péri-implantites – Approche thérapeutique Parresia 2019
– Schneider S et al. Electrochemicalremoval of biofilms from titanium dental implant surfaces Bioelectrochemistry Vol 121, June 2018, 84-94
– Monje et al. Resolution of Peri-implantitis by means of Implantoplasty as adjunct to Surgical Therapy: A Retrospective Study J Periodontal Jan 2022
– Herrera D et al. Prevention and treatment of peri-implant diseases-The EFP S3 level clinical practice guideline J Clin Periodontol 2023 Jun:50 Suppl 26:4-76.
– Capelli M et al. Implant-buccal plate distance as diagnostic parameter: a prospective cohort study on implant placement in fresh extraction sockets J Periodontol 2013 Dec 84 (12): 1768-74
– Linkevicius T et al. Crestal bone stability around implants with horizontally matching connection after soft tissue thickening: a prospective clinical trial Clin Impl Dent Relat Res 2015 Jun 17(3): 497-508
– Rocuzzo A et al. Clinicla outcome of dental implants in patients with and without history of periodontitis: a 20-year prospective study J Periodont 2022: 1-11
– Rompen E. The impact of the type and configuration of abutments and their (repeated) removal on the attachment level and marginal bone. Eur J Oral Implantol. 2012;5 Suppl:S83-90
– Glauser R 1 Schupbach P Early bone formation around immediately places two-piece tissue-level zirconia implants with a modified surface: an experimental study in the miniature pig mandible Int J Implant Dent 2022 (37°
– Brunello G et al. Two-piece zirconia implants in posterior regions: a cohort study with a follow-up period of 9 years. Clin. Oral Impl. Res.2022 33 (12) 1233-1244
– Karapataki S et al. Clinical Performance of Two-Piece Zirconia Dental Implants After 5 and up to 12 Years. Int J Oral Maxillofac Implants 2023;38:1105–1114
– Heitz-Mayfield L et al. Implant Disease Risk Assessment IDRA – a tool for preventing peri-implant disease Clin Oral Impl Res. 2020;31:397–403.