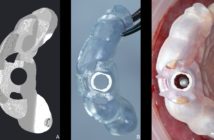
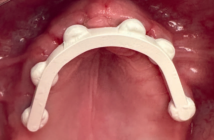
La pratique du scanner dentaire (dentascanner), longtemps considéré comme l’examen radiologique de référence en odontostomatologie (1,2), est aujourd’hui remise en question par l’arrivée sur le marché d’une technique concurrente, réputée moins irradiante : la tomographie à faisceau conique (cone beam tomography) (3). Comme pour toute pratique radiologique, le scanner a pourtant été l’objet d’une optimisation de ses protocoles dans le but de limiter l’irradiation du patient à la plus petite dose suffisante (3-13).
Après avoir rappelé les grandeurs utilisées en radioprotection, nous évoquerons les principes du scanner et du dentascanner, puis les moyens d’optimiser la pratique de cet examen. Nous détaillerons ensuite l’offre actuelle en tomographie à faisceau conique, en comparant les caractéristiques et indications principales de ce type d’exploration qui pourrait s’imposer en odontostomatologie comme une méthode de choix, à condition d’être significativement moins irradiante que le scanner (14-20).
Grandeurs et unités utilisées en radioprotection (4-11)
Dose absorbée
C’est la quantité d’énergie absorbée par unité de masse de matière irradiée. Elle s’exprime en Gray (Gy), correspondant à l’absorption d’un joule d’énergie par kilogramme de matière. Elle est directement liée aux paramètres d’exposition radiologique et est mesurée à la sortie du tube. Elle peut être exprimée par la CTDIvolumique (Volumic Computed Tomography Dose Index) ou CTDIvol, correspondant à la dose délivrée par unité de volume irradié, exprimée en mGy. En scanographie, on calcule le Produit Dose Longueur (PDL ou DLP), correspondant au produit CTDIvol par la longueur explorée, exprimé en mGy.cm, rendant mieux compte de la dose totale délivrée au cours d’un examen.
Dose efficace
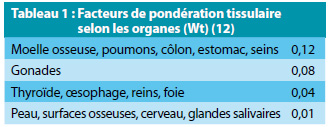
Elle permet de calculer le risque statistique théorique maximum d’apparition d’effets cancérigènes. Pour tenir compte de la susceptibilité variable des organes aux radiations, un facteur de pondération (facteur tissulaire) est appliqué pour définir pour chaque organe une dose efficace, exprimée en Sievert (Sv), telle que :
Dose Efficace = Dose Absorbée x Facteur Tissulaire
Un facteur de pondération tissulaire a ainsi été défini pour chaque organe (Tableau 1). En pratique scanographique, l’examen explorant plusieurs organes d’une même région du corps, un facteur a été proposé pour chaque région (Tableau 2) (12). Il est de 0,0021 pour la tête, utilisé en scanner dentaire pour calculer la dose efficace par examen, à partir du PDL (DLP).

Au total, l’irradiation annuelle correspond à environ 3,5mSv par an et par individu, dont 2,5mSv d’irradiation naturelle et 30 % environ provenant de l’activité humaine, incluant les voyages aériens, les séjours en altitude et le diagnostic médical.
Scanner ou tomodensitometrie
Principe du scanner et technique du dentascanner (1,2)
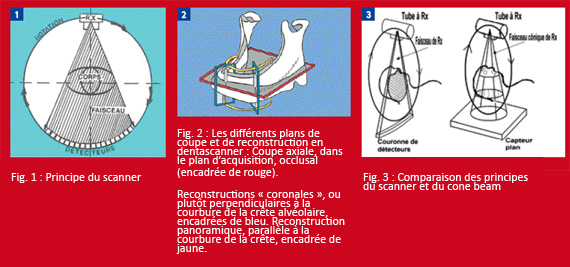
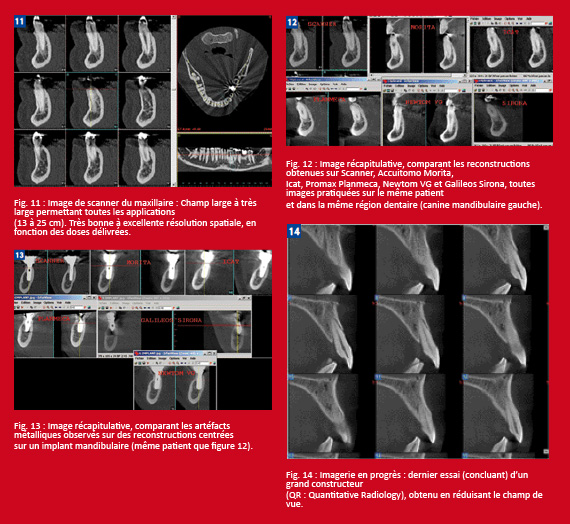
Principe du scanner (1) (Fig. 1) : L’image tomodensitométrique fait appel aux rayons X et repose sur l’absorption différentielle du rayonnement par les différentes structures anatomiques traversées. Le faisceau de rayons X est étroitement collimaté, réalisant des coupes fines (un mm d’épaisseur ou moins) du sujet traversé (ici les maxillaires). La collimation du rayon implique que le rayonnement «diffusé » soit pratiquement nul en dehors du champ d’exploration, et qu’entre autres, les organes relativement radiosensibles telle la thyroïde, soient peu ou pas irradiés. Les récepteurs du rayonnement sont constitués par des détecteurs électroniques, qui transforment le rayonnement en signal électrique, lui-même traduit en information numérique traitée par ordinateur. Technique du dentascanner (2) (Fig. 2) : Des coupes axiales (perpendiculaires à l’axe du corps) encadrées de rouge sur la figure 2, sont réalisées selon un plan parallèle au plan occlusal. Les coupes sont millimétriques ou infra millimétriques, jointives ou mieux chevauchées. Seules ces coupes, directement réalisées sur le patient, sont irradiantes. Les autres images, reconstructions bidimensionnelles (encadrées de bleu ou de jaune) ou tridimensionnelles, ne sont que le fruit de calculs informatiques.
Dosimetrie du scanner dentaire (3-13, 18)
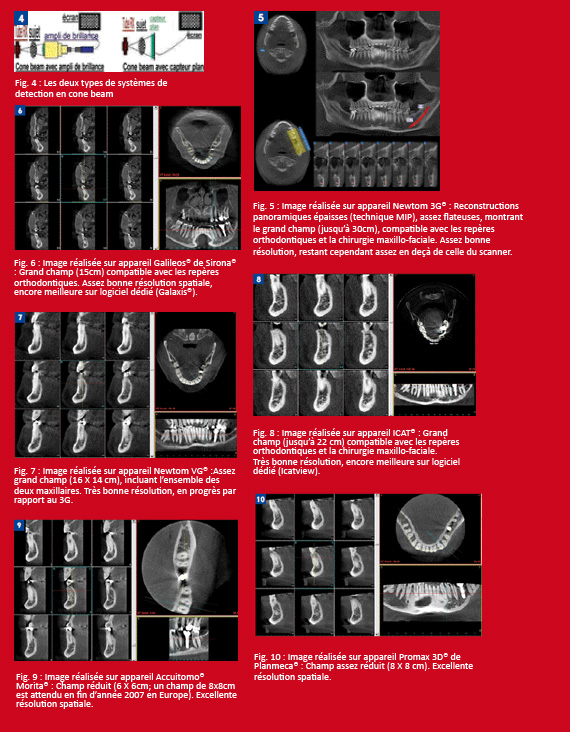
Classiquement, un scanner dentaire, n’explorant qu’une arcade, comporte la réalisation d’une soixantaine à une centaine de coupes millimétriques ou infra-millimétriques, responsable d’une dose absorbée de 100 à 600 mGy, soit 0,23 à 1,3 mSv ou 230 à 1300 μSv.
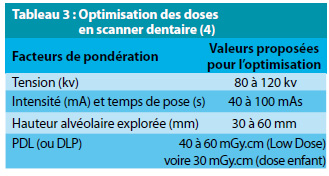
L’optimisation des doses (Tableau 3) (3,4,12,18) permet, au prix d’une perte minime en définition, non préjudiciable au diagnostic, de définir la plus petite dose suffisante, soit environ 40 à 60 mGy par arcade chez l’adulte, correspondant à une dose efficace de 84 à 106 μSv, soit, pour les deux arcades, 210 μSv sur Scanner General Electric® 64 barrettes et 554 μSv sur scanner Siemens Somatom 64, selon Ludlow(18). Ces nouveaux scanners multibarrettes permettent d’abaisser les constantes (temps de pose et surtout mA) au point de limiter la dose efficace à une fourchette comprise pour certains entre 25 et 100 μSv (3). Ces protocoles « Ultra Low Dose » s’accompagnent obligatoirement d’une dégradation de la qualité d’image, laquelle reste suffisante dans la majorité des cas, pouvant remettre en cause l’intérêt dosimétrique du « Cone beam ». Cette optimisation s’obtient en abaissant la tension du tube à 100kV (voire 80 kV chez l’enfant), l’intensité et le temps de pose afin que la dose ne dépasse pas 40 à 100 mAs. On peut jouer aussi sur la hauteur d’exploration qui ne doit pas dépasser trop largement le procès alvéolaire et les dents vers le haut ou le bas. Enfin, une protection plombée de la thyroïde est utilisée autant que possible.
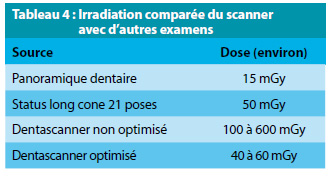
Une comparaison peut s’établir avec d’autres examens du radiodiagnostic dentaire (Tableau 4) (18). Ainsi, un panoramique dentaire Ortophos Siemens® expose en moyenne à 21 μSv. Un scanner dentaire « optimisé » expose donc à une irradiation correspondant à celle de 4 panoramiques (scanner optimisé du maxillaire seul sur appareil General Electric 64 barrettes) à 26 panoramiques (pour un scanner des deux maxillaires sur appareil scanner Siemens Somatom 64 barrettes). Cependant, est à noter le caractère minime du « diffusé » en scanographie, alors que les techniques conventionnelles, y compris la tomographie à faisceau conique, ne peuvent s’en affranchir.
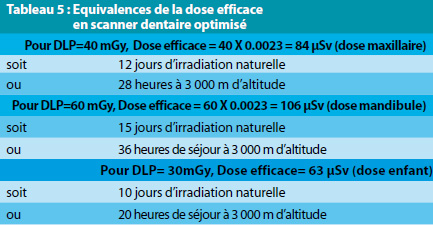
Des équivalences ont été proposées avec d’autres risques sanitaires (Tableau 5) (3,13,18). Ainsi, une dose efficace de 84 μSv correspond à 12 jours d’irradiation naturelle ou 28 heures de séjour en altitude ou au risque induit par la consommation de 25 cigarettes ou encore environ 4 risques sur un million d’être victime d’un cancer mortel. Le risque est à peu près multiplié par deux pour un scanner des deux maxillaires. A titre de comparaison, la dose efficace d’un panoramique dentaire, estimée à 21 μSv (18), correspond à celle de 3 jours d’irradiation naturelle ou 7 heures à 3 000 m d’altitude ou à un risque sur un million d’être victime d’un cancer mortel.
Des règles d’optimisation de la pratique du scanner dentaire peuvent être proposées (4) :
- Les indications du scanner dentaire : implantologie, rapports des dents incluses avec le canal mandibulaire, exploration des sinus et de leurs rapports avec les dents et avec une éventuelle pathologie apicale sous-jacente, pathologie tumorale, kystique et osseuse traumatique sont les indications les plus justifiées du scanner dentaire chez l’adulte.
- Un radiologue entraîné est à préférer, pour l’obtention d’un examen d’emblée réussi.
- L’optimisation des constantes (kV, mAs, hauteur explorée…) est indispensable ainsi qu’une protection plombée de la thyroïde autant que possible.
Le scanner dentaire, apparaît donc, chez l’adulte, s’il est bien indiqué et réalisé selon des règles d’optimisation, comme un examen dont l’apport médical justifie une irradiation somme toute limitée et respectant les organes relativement radiosensibles (tels la thyroïde, la moelle osseuse et les gonades).
Tomographie à faisceau conique (cone beam)
La tomographie à faisceau conique (Cone Beam Computed Tomography-CBCT- ou plus proprement Cone Beam Volumic Tomography-CBVT) est de plus en plus souvent proposée en imagerie dento-maxillo-faciale (3,4,14-20), du fait notamment des doses d’irradiation plus basses qu’elle délivre comparativement à celles exigées par le scanner non optimisé, tel qu’il est encore pratiqué en général (4). Les constructeurs proposent des appareils de plus en plus sophistiqués, dont la qualité d’image rivalise avec celle du scanner.
Principe de la tomographie à faisceau conique (Fig. 3 et 4)
Le faisceau de rayons X, de forme conique, traverse l’objet à explorer avant d’être analysé après atténuation par un système de détection. Le tube et le système de détection tournant autour du sujet (180 à 360° selon les constructeurs), plusieurs centaines d’analyses (prises de vues) sont réalisées dans les différents plans de l’espace, permettant après transmission des données à un ordinateur, la reconstruction volumique d’un cube contenant l’objet (ici, les maxillaires). Le volume étudié est composé de voxels dont le côté est de la taille d’un pixel, mesuré en mm (Fig. 3).
Le système de détection et de transmission des données diffère selon les machines. Le premier type de système utilisé comprend essentiellement un amplificateur de brillance (Newtom3G®, Galileos Sirona®). Le second type de système utilisé est le capteur plan (Accuitomo Morita®, Icat®, Promax de Planmeca®, Newtom VG®). La comparaison des deux systèmes (Fig 4) suggère un chemin plus court et plus simple du signal pour le système à capteur plan, qui pourrait pour certains expliquer en partie la meilleure résolution observée avec les machines employant ce type de détecteur.
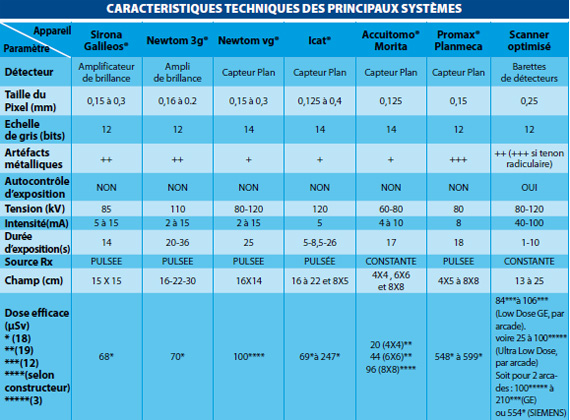
Caractéristiques techniques des principaux systèmes
La taille du pixel (et du voxel) à l’acquisition est en rapport avec la résolution spatiale (définition), qui dépend d’autres facteurs, tel le nombre de lignes affichées par millimètres : tous les systèmes revendiquant au moins deux paires de lignes par mm, ce facteur n’apparaît donc pas discriminant. D’autres éléments sont à prendre en compte : le type de détecteur, le champ de vue ou d’exploration (plus un champ est limité, meilleure est la définition, pour un nombre de pixels donné). Enfin, le système informatique d’analyse, comprenant entre autres le logiciel d’exploitation et le système d’affichage (ordinateur, carte vidéo, résolution de l’écran…) apparaît déterminant dans la définition apparente de l’image. C’est pourquoi nous avons eu pour règle de juger la définition relative à partir du format Dicom® des images natives de chaque appareil, que nous avons toutes traitées par la même chaîne informatique comprenant un logiciel de reconstruction (Simplant Master 10.01®) et un ordinateur identiques. Dans ces conditions seules, les images peuvent être comparées quant à leur définition.
Cependant, le sujet lui-même peut être plus ou moins « opaque » ou source d’artéfacts, notamment métalliques (couronnes, implants déjà en place et surtout tenons intra-radiculaires), mais aussi cinétiques, si le patient a tendance à bouger pendant la réalisation des clichés : ainsi l’examen d’ un sujet jeune, sans traitement dentaire et immobile, donne de meilleures images que celui d’un patient âgé, porteur de prothèses et impatient.
L’échelle de gris concerne le nombre de nuances de gris (du blanc au noir) que le système permet d’afficher, soit la résolution en densité ou en contraste. L’échelle de Hounsfield, utilisée en scanner, comptant 4 000 niveaux de densité, une échelle de 12 bits apparaît suffisante, permettant d’afficher théoriquement 4 096 (2 puissance 12) niveaux de gris. En outre, l’oeil humain ne permettant de distinguer sur une même image qu’environ 16 nuances de gris, on comprend que le passage de 12 à 14 bits de l’échelle de gris ne peut concerner qu’un plus grand choix de « fenêtres de densités », ce qui nous a semblé d’un apport plutôt relatif dans le rendu de l’image.
Enfin, rappelons que seul le scanner permet la mesure réelle des densités, les techniques « cone-beam », apparentées à la tomographie ne permettant qu’une approche relative des densités, à limiter aux structures denses, tels l’os et les dents, l’étude des tissus « mous », demandant une beaucoup plus grande précision, restant réservée au tomodensitomètre (scanner).
L’importance des artéfacts métalliques semble inversement corrélée à l’épaisseur de coupe et du voxel. Plus ceux-ci sont fins plus les artéfacts métalliques seront sensibles et gênants.
L’autocontrôle d’exposition permet théoriquement d’adapter la dose émise à l’«opacité» (densité, épaisseur) du sujet, autorisant l’ajustement des doses au patient, surtout utile chez l’enfant. Seul les scanners proposent un contrôle d’exposition efficace, avec affichage de la dose délivrée en mGy.
La durée d’exposition : plus elle est courte, plus les artéfacts cinétiques, dus aux mouvements du patient lors de la réalisation de l’examen, seront limités. Tous les appareils « cone beam » devraient ainsi comporter un système de contention efficace, du fait de la durée relativement longue de l’exposition, comparativement au scanner.
Le type de source à Rx, constante ou pulsée. Dans ce dernier cas, la durée d’exposition est réduite, ce qui permettrait pour certains de limiter la dose délivrée. En fait, ceci semble plus complexe et une source continue de rayons serait, pour d’autres, moins irradiante, car elle éviterait les pics transitoires du mode pulsé.
Le champ d’exploration (champ de vue) : C’est la largeur de l’image. La hauteur d’exploration concourt aussi au volume exploré, dont dépendent le nombre de structures étudiées mais aussi la dose délivrée. Si un champ limité (Morita®, Planmeca®) est suffisant pour les indications courantes de l’imagerie 3D (Implantologie, rapports de structures incluses), les bilans orthodontiques et la chirurgie maxillo-faciale exigent des champs plus grands.
Du champ de vue dépend aussi le « volume » informatique par examen : on parle aussi de « poids » informatique, exprimé en octets ou en bits. Plus l’image est grande et définie et plus son « poids » informatique est important. Ainsi, un examen global en définition maximale (pixels de 0.15mm) va de 250 mégaoctets (Mo) pour le Promax de Planmeca® à 400 Mo pour le Galileos de Sirona® et 750 Mo pour le Newtom VG. Pour ces raisons, l’examen n’est souvent exploité pour l’affichage qu’avec une définition limitée (pixels de 0.3 mm), permettant la réduction à environ 256 Mo par examen pour le Galileos®. De tels « volumes » imposent l’utilisation d’ordinateurs de dernière génération, armés de mémoire vive importante (2 Gigaoctets) et d’une carte graphique puissante (au moins 256 Mo de mémoire vidéo). La compression des données utile à l’envoi des données par Internet, permettant de réduire l’étude à quelques Mo, exige une définition préalable excellente. Dans ce domaine, le scanner apparaît supérieur, se contentant pour l’étude d’une arcade à un volume de 40 à 60 Mo pour les données Dicom® (format informatique sans perte, consensuel pour l’échange des données en imagerie médicale) facilement réduit à 3 à 10 Mo après compression.
La dose Efficace (micro Sievert ou μSv) dépend directement des constantes radiologiques, tension (kV), intensité (mA) et durée d’exposition (s) ainsi que du volume exploré. C’est, comme nous l’avons vu, la dose calculée à partir de la dose délivrée (ou absorbée), exprimée en Grays (ou Gy) et tenant compte de la sensibilité relative aux rayons X des tissus traversés. Les doses efficaces apparaissent assez disparates et parfois éloignées des caractéristiques du constructeur. On privilégiera évidemment les appareils délivrant des doses limitées.
Cependant, les organes irradiés par un scanner ou une étude « cone beam » des maxillaires apparaissent en définitive assez peu radio sensibles, comparativement à la thyroïde, aux gonades et à la moelle osseuse, qui présentent des facteurs de sensibilité tissulaire beaucoup plus élevés. Il nous semble donc qu’un scanner des maxillaires, réalisé selon les règles connues d’optimisation des doses (4), reste le plus souvent justifié chez l’adulte dans la mesure où il n’est pas fréquemment pratiqué sur le même patient. Cependant, pour les sujets jeunes et surtout l’enfant, le « cone-beam » pourrait s’imposer, en particulier pour les études de volume limité, comme celle d’une dent incluse ou d’une implantation d’un ou deux éléments. Ainsi, certains systèmes offrent la possibilité d’explorations localisées à un maxillaire, voire à une zone réduite, permettant des doses encore plus limitées (comme le propose Morita®).
Conclusions
Au terme de ce panorama succinct plusieurs conclusions s’imposent :
L’étude des densités est à réserver au scanner (tomodensitomètre), surtout pour les parties molles, moins bien étudiées par les techniques « cone-beam », mais aussi pour les structures denses tels une greffe à contrôler, l’os et les dents. C’est pourquoi un scanner est à proposer systématiquement en cas de lésion suspecte de malignité, surtout si les parties molles sont concernées. Le scanner reste par ailleurs indiqué d’une manière générale chez l’adulte, pour une étude étendue, non localisée, à condition que sa pratique soit optimisée (Low Dose).
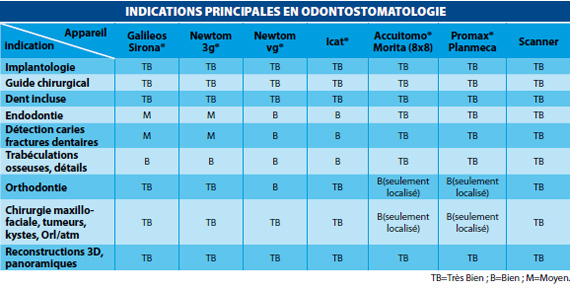
Tous les systèmes « cone beam » sont cependant assez bons pour les indications essentielles de l’imagerie tridimensionnelle comme l’implantologie et la mise en évidence des rapports de structures incluses (dents, odontomes, kystes). Ils seraient à préférer au scanner chez l’enfant et l’adulte jeune, surtout si l’étude est localisée et si l’irradiation proposée est signicativement plus basse que sur scanner.
Les systèmes à grand champ d’exploration ( Sirona®, Newtom®, Icat® et Scanner) sont plus intéressants pour l’orthodontie et la chirurgie maxillo-faciale.
Les systèmes à champ limité (Morita®, Planmeca®) seraient plus performants pour l’endodontie et l’analyse de détails tels la trabéculation osseuse, la mise en évidence de fracture dentaire.
Cependant, les constructeurs nous sembleraient bien inspirés d’offrir, à côté de l’étude globale des maxillaires, la possibilité d’explorations localisées à un maxillaire, voire à une zone réduite, pour l’étude tridimensionnelle, par exemple, d‘une dent incluse ou d’une région à implanter, ce qui permettrait l’utilisation de doses encore plus limitées et donc une irradiation globale de la population encore plus basse. C’est dans cette optique que les techniques « cone beam » pourraient s’imposer dans l’avenir, en proposant des explorations de taille plus réduite, donc toujours moins irradiantes et d’encore meilleure qualité.
Bibliographie
Bibliographie 1. Bellaiche N. Le praticien et le scanner crânien. Ed.Guerbet, Paris, 1988
2. Bellaiche N., Missika P. La tomodensitométrie dans le bilan pré-opératoire en implantologie orale. Information Dentaire, 1991; 32 :268-89
3. Fourcart J.M. La radioprotection en odontologie, Ed. CdP, 2ème édition, Paris, 2007.
4. Bellaiche N. Scanner dentaire et dosimétrie. La lettre de Stomatologie 2006 (n° 30) 14-16
5. Gambini D.J., Granier R. Manuel pratique de radioprotection, Paris, 2002
6. Beauvais-March H. Les niveaux de référence diagnostique : un outil pour l’optimisation des expositions à des fins médicales. Contrôle (ASN) 2002 ;148 :68-72
7. Cordolani Y.S., Bubayle P., Jouan E. Explorations radiologiques en odonto- stomatologie. Dosimétrie et estimation du risque. Encycl Med Chir, Stomatologie-Odontologie I, 22-010-D10, 1996
8. Lisbonna A. Dosimetrie des Explorations Diagnostiques en Radiologie. Société française de physique médicale 2003
9. European guidelines on quality criteria for computed tomography. Eur 16262, May 1999
10. Commission internationale de Protection radiologique (CIPR). Publication 60. Recommandation 1990 de la CIPR. Oxford : Pergamon Press, 1990
11. Commission européenne. European guidelines on radiation protection in dental radiology. Bruxelles : Office des publications officielles de l’Union Européenne, 2003
12. Commission internationale de Protection radiologique (CIPR). Rapport 102, Elsevier, 2007.
13. Cohen B.L. Catalog of risks extended and updated. Health physics, 1991; 61(3): 317-35
14. Ludlow J.B., Davies-Ludlow L.E., Brooks S.L., Howerton W.B. Dosimetry of 3 CBCT devices for oral and maxillofacial radiology:CB Mercuraray, Newtom 3G and i-CAT. Dentomaxillofacial Radiology 2006 ; 35: 219–226
15. Guerrero M.E., Jacobs R., Loubele M., Schutyser F., Suetens P., Van Steenbergue D. State-of-the-art on cone beam CT imaging for preoperative planning of implant placement. Clinical Oral Investigations 2006;10:(no.1)1-7
16. Loubele M., Maes F., Schutyser F., Marchal G., Jacobs R., Suetens P. Assessment of bone segmentation quality of cone-beam CT versus multislice spiral CT : a pilot study. Oral surgery oral medicine oral pathology oral radiology and endodontics. 2006; 102:(no. 2) 225-234
17. Cavezian R., Pasquet G., Bel G., Baller G. Imagerie dento-maxillaire : approche radio-clinique, 3e édition, Masson. 2006
18. Ludlow J.B. Dosimetry of Cone Beam and Multi-Row-Detector CT Units for Dento-alveolar and Maxillofacial Imaging.August.30.2007
19. Hirsch E., Wolf U., Heinicke F., Alves Garcia Silva M. Dosimetry of the new Cone Beam CT (VERAVIEWEPOCS 3D) compared to the Accuitomo in different FOVs. A paraître
20. Bellaiche N. Tomographie a faisceau conique (cone beam) : Les différents systèmes, leurs caractéristiques principales et indications. La lettre de stomatologie 2007 (n°33)10-15
Norbert Bellaiche
- Radiologue
- Diplômé de Radiologie maxillo-faciale
- Chargé de cours aux facultés de Cochin-Port Royal,
- La Pitié-Salpétrière et Créteil