Depuis 50 ans, le titane représente le matériau de choix en ce qui concerne les dispositifs chirurgicaux implantaires pour les réhabilitations fixes en dentisterie. Nous apprécions ses qualités mécaniques, augmentées de nos jours par l’utilisation d’alliage de titane comme en orthopédie.
En revanche, sa biocompatibilité dépend de son absence de réponses immunitaires et inflammatoires et donc de sa capacité d’inertie dansla cavité orale. Cette biocompatibilité est en relation avec la résistance relative à la corrosion. Une couche d’oxyde de titane (TiO2) de 10 um se forme sur la surface de l’implant en sortant de son emballage stérile et avant son insertion dans l’alvéole. Les implants, une fois mis en fonction, sont alors soumis à de rudes conditions comme des variations de température, de pH, d’attaques microbiennes pouvant rompre cette couche de passivation de l’implant. (1) Cette bio-corrosion (1) peut être alors : (Fig. 1a, b et c)
- chimique : en fonction de l’acidité du PH Un défaut d’adaptation de la couronne et un débordement de ciment peuvent augmenter l’inflammation.
- galvanique étant donné la diversité des matériaux métalliques dans la cavité orale ou composant la suprastructure prothétique sur implants.

Fig. 1b : contrôle radiographique montrant une péri implantite avec une perte osseuse importante autour de l’implant et autour de la dent 17.

Fig. 1c : dépose de l’implant montrant un défaut d’adaptation de la CCM (semi précieux) scellée sur le pilier implantaire en titane.
- mécanique lorsque les connexions implantaires sont peu stables et occasionnent des frictions du pilier sur l’implant.
De récentes études nous confirment que la présence de bactéries, ainsi que des particules de titane rentrent dans l’étiopathogénie des maladies péri-implantaires.(2,3) Ces particules de titane vont occasionner une réaction immunologique de défense vis à vis de corps étrangers se situant dans l’environnement péri implantaire. La connaissance de ces mécanismes biologiques doit nous faire prendre conscience des conditions dans lesquels nos implants en titane peuvent perdurer dans la bouche de nos patients. (Fig. 2a, b et c)

Fig. 2a, b et c : cas clinique à 6 ans de recul clinique avec une stabilité osseuse marginale et une bonne santé des tissus mous péri implantaires.
Par ailleurs, la pollution de notre environnement, la présence de nombreux allergènes dans notre alimentation, les produits cosmétiques font apparaitre de plus en plus de patients avec réactions d’intolérances ou d’hypersensibilité aux métaux en implantologie et en orthopédie. Les patients présentant un terrain allergique et des maladies auto immunes sont également des patients à haut risques immunologiques lorsque nous posons l’indication d’implants dentaires. Les implants en céramique zircone présentant une inertie électro-chimique peuvent alors apparaitre comme une véritable alternative.
PRÉSENTATION D’UN CAS CLINIQUE
Patiente Mme G., 38 ans Patiente en consultation avec les symptômes suivant : une asthénie, des insomnies, des brûlures des muqueuses et de la langue , un goût métallique qui sont apparus 2 mois suite à la pose de 4 implants. Dans la discussion lors de notre première consultation, la patiente a toujours présentée des réactions cutanées de type rougeurs et démangeaisons avec des bijoux fantaisies. (Fig. 3a et b)


Fig. 3a et b : Les 4 implants ont été posés en 1 temps chirurgical et les tissus mous
ne présentent aucun signe d’inflammation et de saignement au sondage. En sites 45, 46 et 36, 37

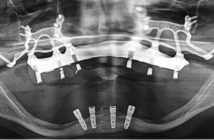
Fig. 3c : radio panoramique récente que nous donne la patiente ne montrant aucune perte osseuses péri implantaire, ce qui est confirmé à l’examen 3D.
LES DIFFÉRENTES POSSIBILITÉS DE DIAGNOSTIC D’UNE ALLÉRGIE DE TYPE IV
Tout le monde s’accorde pour indiquer que la prévalence des hypersensibilités ou allergies aux métaux dentaires est en augmentation à l’heure actuelle (4) d’où la nécessité d’utiliser des diagnostics fiables. Vu le caractère « cellulaire » – ou retardé – de l’allergie de type IV, les tests sanguins sur lymphocytes sont d’une grande fiabilité́, en comparaison au patch tests réalisé couramment par les allergologues. Actuellement, il existe des examens biologiques en laboratoire qui indiquent clairement si les matériaux et métaux sont bien tolérés sur le plan immunologique. Il s’agit principalement du test Melisa. Le test MELISA est un test utilisé pour déterminer si l’allergie aux métaux est responsable de l’un des symptômes qui se sont développés et décrits par le patient. Les patients souffrant d’une hypersensibilité́ aux métaux peuvent présenter de nombreux symptômes locaux associés àun système immunitaire hyperactif, tels que des douleurs localisées, un gonflement, des réactions allergiques cutanées, des douleurs articulaires et musculaires, une défaillance de l’implant, des infections apparemment récurrentes autour du site de l’opération, et d’éventuelles réactions systémiques comme la fibromyalgie, la fatigue chronique et des troubles cognitifs. MELISA est un test sanguin scientifiquement prouvéet cliniquement validéqui détecte l’allergie de type IV à plusieurs métaux en même temps. (5) La perte d’ostéointégration d’un implant est un événement indésirable et souvent multifactoriel. Actuellement, il semble que les défaillances d’implants puissent être classées selon des facteurs biologiques, mécaniques, iatrogènes et aussi liés au patient. (6,7) Cependant, tous les échecs ne peuvent pas être expliqués et il est concevable que l’hypersensibilité au titane puisse jouer un rôle dans de tels cas. (8) Cette possibilité a été mise en évidence et une étude clinique présente des défaillances d’implants chez des patients allergiques au titane. (9) Il est probable que l’incidence de la réaction allergique aux implants en titane soit sous-déclarée en raison d’un manque de reconnaissance en tant que facteur étiologique possible de l’échec de l’implant. C’est pourquoi l’hypersensibilité au titane ne devrait pas être exclue comme raison de l’échec des implants.
TOUS LES IMPLANTS EN TITANE CONTIENNENT DU NICKEL
Harloff et al. (10) ont utilisé l’analyse spectrale comme outil de diagnostic pour analyser différents alliages d’implants en titane afin de déterminer le pourcentage des composants et des ajouts d’alliage qui sont connus pour provoquer des allergies. Harloff et al. démontrent que tous les échantillons de matériaux d’implants étudiés contenaient un pourcentage faible mais constant de composants qui ont et́é associés àdes allergies. Par exemple, les faibles teneurs en nickel sont liées au processus de fabrication et sont complètement dissoutes dans la grille de titane. (Fig. 4)

Fig. 4: présence de composants et de traces de nickel (en rouge) dans les implants en titane Pur (Grade 4) et Alliage de titane (grade 5)
Par conséquent, ils peuvent pratiquement être classés comme « impuretés ». Dans certaines circonstances, ces petites quantités peuvent suffire à̀déclencher des réactions allergiques chez les patients souffrant des allergies correspondantes, comme une allergie au nickel, au palladium ou au chrome. Cette présence de traces de nickel a également et́évalidée par Hartmann et al. (11) En étudiant l’étiologie, le diagnostic et le traitement de l’hypersensibilité,́ on peut conclure que les cas d’allergie au titane sont susceptibles d’augmenter(12) . Une explication àcela peut être la présence d’agents sensibilisants connus (nickel, chrome et cobalt) dans le métal, résultant du processus de production. Ces métaux traces peuvent être insignifiants d’un point de vue métallurgique, mais peuvent être suffisants pour déclencher des réactions allergiques chez les patients sensibles(13) . Actuellement, il n’y a pas encore une compréhension complète de l’interaction biologique du titane et, par conséquent, des réactions d’hypersensibilité́ ou d’allergie ne peuvent être exclues comme raison de l’échec d’un implant. La présence systématique de traces de nickel dans les implants en titane associée à une prévalence élevé́ d’allergie au nickel explique parfois un résultat de test négatif au titane, mais par contre très positif au nickel. Un résultat positif au nickel peut justifier la dépose d’implants en titane en présence de symptômes cités dans notre cas clinique.
LE CHOIX DES IMPLANTS EN ZIRCONES : UNE ALTERNATIVE AU TITANE ?
Les qualités de la céramique zircone en tant que matériau de restauration prothétique nous démontrent au quotidien une colonisation bactérienne extrêmement faible (14) , et des tissus mous qui sont alors une barrière à l’infection sousjacente. Ce matériau n’est pas un conducteur thermique, ni électrique et grâce à sa grande inertie (15) , il présente une excellente stabilité chimique avec un relargage ionique quasi inexistant, ce qui participe grandement à sa biocompatibilité observée vis à vis des cellules du parodonte et pourraient expliquer l’absence de cas d’allergie ou d’hypersensibilité aux céramiques(16) . Les implants en zircone peuvent apparaître comme une véritable alternative au titane chez nos patients et surtout ceux présentant un terrain allergique , des maladies auto immunes, des facteurs de risques parodontaux et des intolérances aux métaux (17) . Nous devons également prendre en compte la tendance actuelle en odontologie vers des restaurations non métalliques, et l’aspect esthétique de nos restaurations sur le long terme. La nouvelle génération d’implant en céramique à base de céramique zircone corrige la faiblesse des premières générations et offre une résistance à la fracture compatible avec les contraintes mécaniques de la mastication. Ce sont des matériaux durs, résistants à la pénétration et rigides.
résistants à la flexion dans lesquels les fractures sont initiées par des fissures à partir de défauts structuraux. Le facteur qui caractérise cette propriété de résistance à la propagation brutale de fissure, la ténacité, est le module K1C qui est linéairement corrélé à la résistance à la flexion (Fig. 5). Sa valeur élevée, de l’ordre de 10, permet au praticien de déterminerson choix de produit et la possibilité de le retoucher en bouche si c’est un implant monobloc (18).
Le zirconium est un élément chimique, de symbole Zr avec un numéro atomique 40. Le zirconium est un métal cependant lors de son oxydation il devient une céramique, l’oxyde de Zirconium ou zircone. La zircone a une structure poly-cristalline et un aspect opaque. Pour renforcer ce réseau cristallin, on parle de stabilisation par l’incorporation d’oxyde d’Yttrium (yttria) ou d’alumine. Deux types de zircone composent les implants céramiques présents sur le marché : le principal est l’Y-TZP (Yttria stabilized Tetragonal Zirconia Polycristals), l’autre l’ATZ (Alumina Toughened Zirconia ), qui sert également pour la confection de forets. (18) La grande majorité de ces implants a été conçue sous forme d’implants « monobloc » c’est-à-dire en une seule pièce, le pilier étant associé à la partie endosseuse filetée. Exemple : Z-systems, White Sky Bredent, Ceralog, Zibone Cette géométrie présente un avantage mécanique et également biologique pour la stabilité des tissus périimplantaires. (19) Certains systèmes proposent désormais des implants en 2 pièces. Cette forme rend la planification similaire au traditionnel système d’implants en titane. Cependant, la fiabilité́de l’adhésion des pièces en céramique et l’usinage d’un filetage interne dans une céramique sont des challenges. Une étude de Jank et Hochgatterer de 2016 sur un suivi de 347 implants posés en 2 pièces à 4 ans rapporte un taux de succès cumulés de 96,7 %. (20) Ex : Z systems, Ceralog, Nobel Pearl (Fig 6, 7 et 8).
RÉSOLUTION DU CAS CLINIQUE : REMPLACEMENT DE 45/46 ET 35/36
1èr ÉTAPE : Diagnostic de l’hypersensibilité ou allergie de Type 4 par le Test Melisa. Lors de ce test, nous notons dans la bouche du patient tous les allergènes potentiels métalliques ainsi que le matériau zircone.
Un indice au-delà de 2 nous donne une indication sur la mobilisation des lymphocytes T autour d’un allergène potentiel et le fait que le patient soit hypersensible à un ou plusieurs métaux. Le test révèle une forte allergie au nickel et au palladium et légère à l’aluminium. (Fig. 1a et b) Les implants utilisés sont en alliage de Titane Ti6Al4V et nous prenons la décision avec le patient de déposer les 4 implants.
2eme ÉTAPE : dépose des implants en alliage de titane A l’aide d’inserts de piézochirurgie et des ROG sont réalisées simultanément avec des particules d’allogreffe (Biobank) et membrane de collagène (Bio Gide) (Fig. 2a et b).
3ème ÉTAPE : pose des implants en zircone A 5 mois, pose de 2 implants en zircone monoblocs (Zsystems) de diamètre 4 mm et long 10 mm en 1 temps chirurgical avec des modeleurs ajourés en Peek. (Fig. 3a et b).
4ème ÉTAPE : restauration des implants en zircone Restauration des d’implants en zircone avec des couronnes scellées en zircone céramique solidaires 45/46 et 36/37. (Fig. 4a et b).
DISCUSSION
Suite à la dépose des implants en titane et après la disparition des symptômes décrits par notre patiente lors de la première consultation, nous avons pu envisager une solution alternative avec des implants en zircone que nous avions également testé avec le test lymphocytaire Melisa (Index=1). La patiente a pu retrouver une vie normale alors que plusieurs confrères lui avaient demandé de consulter un psychiatre. Selon une étude de Sicilia en 2008 (21) qui fait référence, celui-ci rapporte 0,6 % d’allergie au titane sur 1500 patients. Cependant, selon la littérature en orthopédie et en dermatologie les taux d’allergie sont plus proche de 6 %. ( 22, 23) D’autres composants métalliques comme le nickel étant également impliqué dans ces phénomènes immunologiques et souvent plus que le titane, nous devrions avoir une indication de l’implantologie en zircone proche de 20 %. Sans compter l’engouement que suscite le matériau zircone auprès de nos patients. Il nous faudra alors poser l’indication du matériau implantable lors de notre première consultation en fonction de l’état général de notre patient, son anamnèse et un examen clinique. Un bilan d’allergologie sera demandé en cas de suspicion d’allergie avec un test épicutané (patch test) (4) . Nous devrons alors faire le choix de l’implant en céramique dès lors que le patient présente un terrain allergique, des problèmes dermatologiques, une maladie auto immune (24).
CONCLUSION
De nombreux confrères gardent à l’esprit les échecs mécaniques de la première génération des implants en céramique à base d’alumine développé par le Pr Sammy Sandhaus (Cérasand, 1968) qui présentaient une haute biocompatibilité tissulaire. Cet implant en alumine était un implant monobloc dont nous avons gardé le concept sur l’implant en zircone dans les années 2000 à 2010. En fonction des différentes situations cliniques, l’implant en zircone monobloc n’a pas atteint toutes les possibilités du titane en ce qui concerne les protocoles chirurgicaux et prothétiques. L’implantologie en zircone après 20 ans d’existence ne peut se développer que si les implants en 2 parties permettent d’égaler les implants en titane. C’est un challenge que relève peu à peu l’industrie avec l’étroite collaboration des cliniciens. De nos jours, nous pouvons compter sur les implants en zircone pour éviter les risques d’échecs immunologiques liés à l’allergie aux métaux de type IV(25) . L’implant en zircone représente une véritable alternative fiable aux implants en titane et doit faire partie de notre arsenal thérapeutique en implantologie.
BIBLIOGRAPHIE
- Mombelli A, Hashim D, Cionca N. What is the impact of titanium particles and biocorrosion on implant survival and complications? A critical review. Clin Oral Implants Res 2018;29 (suppl18):s53
- T.G. Wilson, Jr.,P.Valderrama, M.Burbano, J.Blansett, R.Levine, H.Kessler, and D.C. Rodrigues. Foreign Bodies Associated With Peri-Implantitis Human Biopsies. J Periodontol • January 2015
- Safioti LM, Kotsakis GA, Pozhitkov AE, Chung WO, Daubert DM. Increased Levels of Dissolved Titanium Are Associated With Peri-Implantitis – A Cross-Sectional Study.J Periodontol. 2017 May;88(5):436-442.
- Evrard, Waroquier, et Parent, « Allergies to dental metals. Titanium : a new allergen. » Rev Med Brux. 2010 Jan-Feb;31(1):44-9.
- Valentine-Thon E, Müller K, Guzzi G, Kreisel S , et al. LTT-MELISA is clinically relevant for detecting and monitoring metal sensitivity. Neuro Endocrinol Lett 2006; 27: 17–24.
- Duyck J, Naert L. Failure of oral implants: Aetiology, symptoms and infuencing factors. Clin Oral Investig 1998; 2: 102–114.
- Esposito M, Thomsen P, Ericson LE, Lekholm U. Histopathologic observations on early oral implant failures. Int J Oral Maxillofac Implants 1999; 14: 798– 810
- Deas DE, Mikotowicz JJ, Mackey SA, Moritz AJ. Implant failure with spontaneous rapid exfoliation: case reports. Implant Dent 2002; 11: 235–242
- Stuart Campbell, St John Crean and Waqar Ahmed. Titanium allergy: fact or fiction? FACULTY DENTAL JOURNAL January 2014 • Volume 5 • Issue 1
- Thomas Harloff, Wolfgang Hönle, Ulrich Holzwarth, Rainer Bader, Peter Thomas, Alexander Schuh. Titanium allergy or not? “Impurity” of titanium implant materials. Health. Vol.2, No.4, 306-310 (2010)
- Hartmann D, Letulé V, Schneider JJ, Flaig MJ. Metal implant sensitivity : clinical and histological presentation Hautarzt. 2016 May;67(5):373-9.
- Papadopoulos NG, Agache I, Bavbek S, et al. Research needs in allergy: an EAACI position paper, in collaboration with EFA. Clin Transl Allergy 2012; 2: 21
- Schedle A, Ortengren U, Eidler , et al. Do adverse effects of dental materials exist? What are the consequences, and how can they be diagnosed and treated? Clin Oral Implants Res 2007; 18: 232–256
- Scarano A, Piattelli M, Caputi S, Favero GA, Piattelli A. Bacterial adhesion on commercially Pure titanium and zirconium oxide disks: an in vivo human study. J Periodontol 2004; 75 (2): 292-6.
- Callister WD. Sciences et génie des matériaux, 5ème édition. Paris: Dunod ; 2001.
- Sterner T, Schütze N, Saxler G, Jakob F, Rader CP. Effects of clinically relevant alumina ceramic, zirconia ceramic and titanium particles of different sizes and concentrations on TNF-alpha release in a human macrophage cell line. Biomed Tech (Berl). 2004 Dec;49(12):340-4.
- Stejskal V, Reynolds T, Bjørklund G . Increased frequency of delayed type hypersensitivity to metals in patients with connective tissue disease. J Trace Elem Med Biol. 2015; 31: 230–236.
- P.DUCHATELARD. La zircone est-elle une alternative au titane en implantologie orale ? L’INFORMATION DENTAIRE n° 39 – 13 novembre 2019
- Borgonovo AE, Censi R, Vavassori V, Arnaboldi O, Maiorana C, Re D – Zirconia Implants in Esthetic Areas: 4-Year Follow-Up Evaluation Study. Int J Dent. 2015;2015:415029.
- Jank S. and Hachgatterer G. . Success Rate of Two pieces Zirconia implants: A retrospective statistical Analysis. Implant Dentistry; Volume25, Number 2- 2016
- Sicilia A, Cuesta S, Coma G, et al. Titanium allergy in dental implant patients: A clinical study on 1500 consecutive patients. Clin Oral Implants Res 2008;19:823–835.
- De Graaf NPJ, Feilzer AJ, Kleverlaan CJ, Bontkes H, Gibbs S, Ruste- meyer T. A retrospective study on titanium sensitivity: Patch test materials and manifestations. Contact Dermatitis 2018;79:85–90.
- Hallab N, Merritt K, Jacobs JJ. Metal sensitivity in patients with orthopaedic implants. J Bone Joint Surg Am 2001;83:428–436.
- Georges Tawil, DDS,Peter Tawil, DDS /Carla Irani, MD, Zirconium Implant as an Alternative to Titanium Implant in a Case of Type IV Titanium Allergy: Case Report .JOMI Volume 35, Number 3, 2020 , 639-644
- Oliva X, Oliva J, Oliva JD. Full-mouth oral rehabilitation in a titanium allergy patient using zirconium oxide dental implants and zirconium oxide restorations. A case report from an ongoing clinical study. Eur J Esthet Dent 2010;5:190–203.