Comme nous l’expliquons le plus simplement du monde à nos patients, l’implant est un système qui simule une fausse racine dentaire et se place comme celle-ci dans le tissu osseux DONC, il nous faut de l’os.
Nous savons depuis longtemps qu’il nous en faut même pas mal autour de nos implants pour pérenniser ceux-ci, 2 mm d’os autour des implants semble la norme, et ne parlons pas du tissu mou. (1)
Nous allons nous contenter dans cet article de parler de tissu dur.
Suite à différentes problématiques infectieuses, traumatiques ou même physiologiques (le temps), nous pouvons perdre de l’os et du coup rendre la pose implantaire impossible dans l’état, il faut donc reconstruire ce tissu et nous avons très grossièrement, 3 techniques qui s’offrent à nous : l’autogène, l’allogène ou la réhabilitation osseuse guidée (ROG).
La reconstruction par os autogène selon par exemple la méthode de F. Khoury, semblait être jusqu’à présent le « Gold Standard » mais les protocoles de ROG semblent être très intéressants aussi (15) pour un gain horizontal ou vertical mais peut-être plus clinicien dépendant … ?
La régénération osseuse guidée dite « ROG » est issue des principes de la régénération tissulaire guidée, fondés sur l’exclusion cellulaire par utilisation de membranes. C’est en 1957 que Murray (2) et son équipe ont parlé les premiers de régénération osseuse en utilisant une cavité c’est-à-dire une notion d’exclusion cellulaire pour créer de l’os sur un os iliaque de chien.
C’est Dahlin et coll (3 et 4) qui en 1988 ont su créer de l’os autour d’implant en utilisant pour la première fois une membrane de téflon chez le lapin, cette membrane positionnée entre le défaut osseux et le périoste permis de créer une cavité qui sera colonisée par des cellules ostéo progénitrices et va exclure le tissu conjonctif et les cellules épithéliales qui migreraient plus rapidement, les cellules ostéo progénitrices ont alors tout loisir de créer de l’os dans cette cavité crée artificiellement.
En 1994, SImion et coll (7) ont les premiers utilisés une membrane PTFE renforcée en titane pour des défauts osseux verticaux, la réhabilitation osseuse fut faite autour d’implants posés simultanément, le gain osseux fut de 4 mm en utilisant uniquement le caillot sanguin, ni d’os autogène ni de substitue osseux.
Par la suite c’est Buser et coll. 1993 (5), et Fugazzotto et coll. 2003 (6) qui ont établies les principes toujours actuels de la ROG :
• le maintien de l’espace nécessaire à la régénération osseuse, favorable à la néo angiogenèse.
• le maintien du caillot sanguin indispensable à la régénération osseuse.
• l’exclusion cellulaire : seulement les cellules à pouvoir ostéogénique sont présentes dans l’espace cicatriciel formé par la membrane ce qui empêche la colonisation du site par les cellules épithéliales et conjonctives.
Les concepts de la ROG sont :
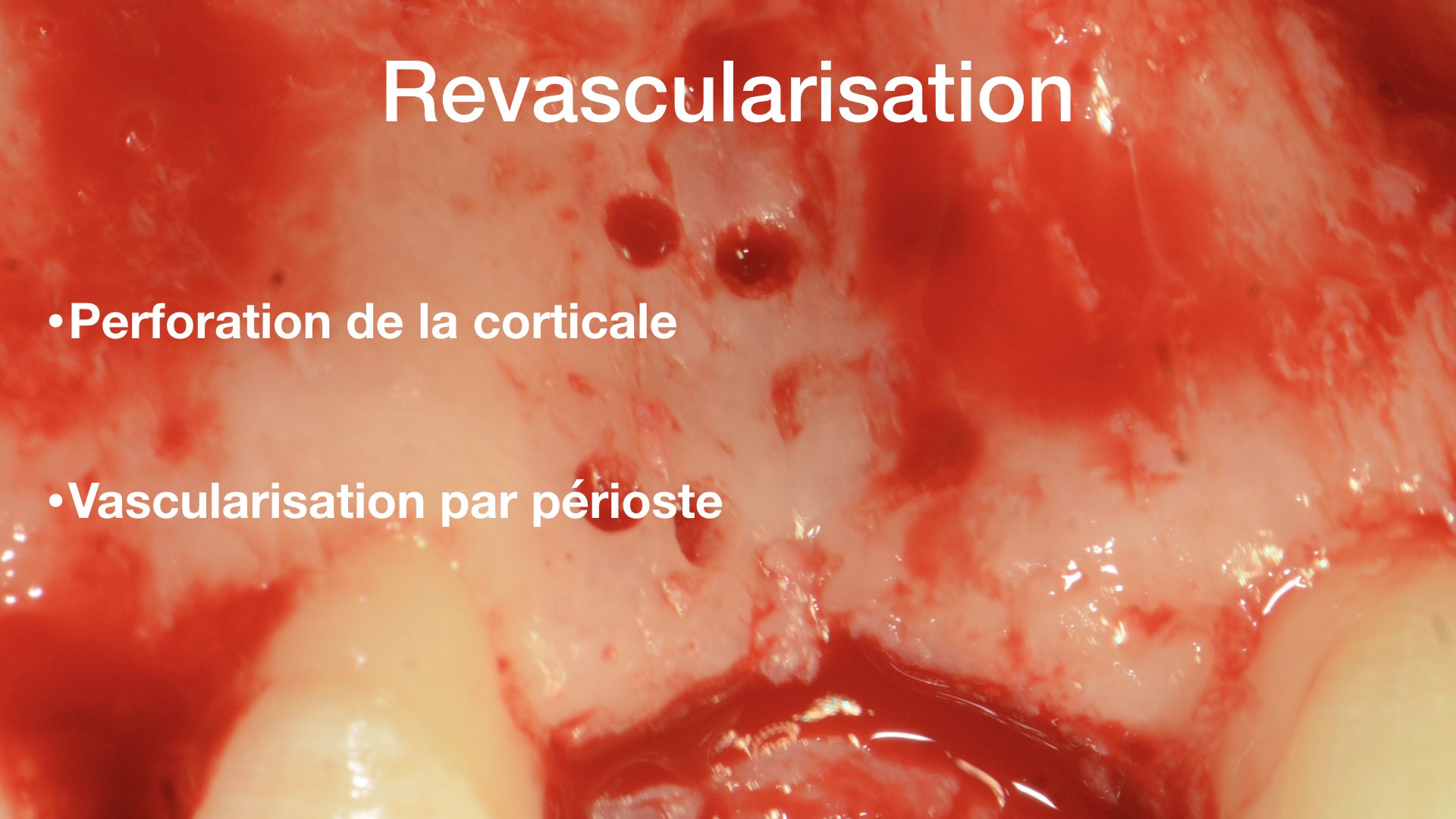
• la revascularisation du greffon, condition essentielle pour sa nutrition et sa régénération
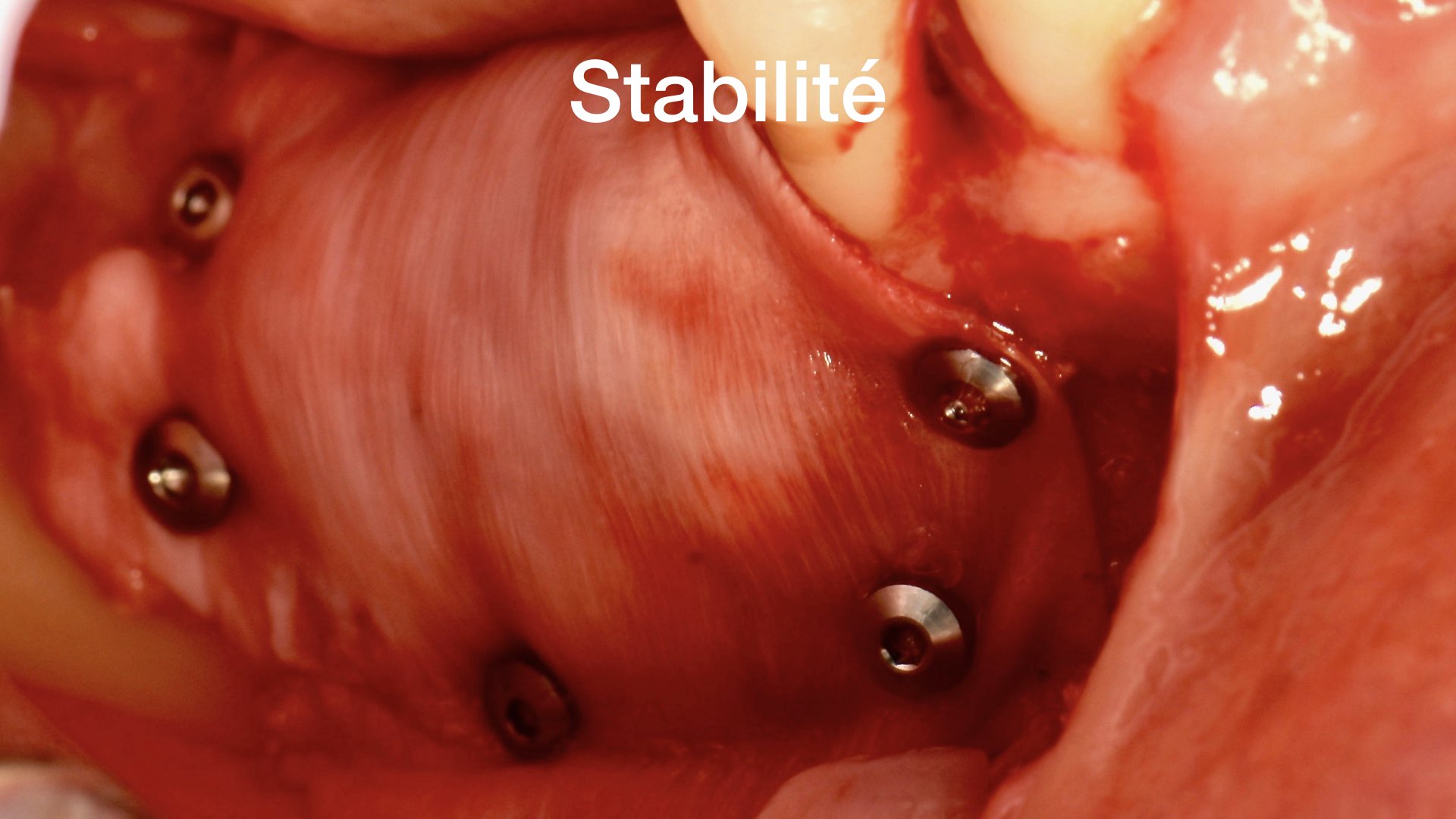
• la stabilité du greffon et protection du caillot sanguin : pas de MICROMOUVEMENT
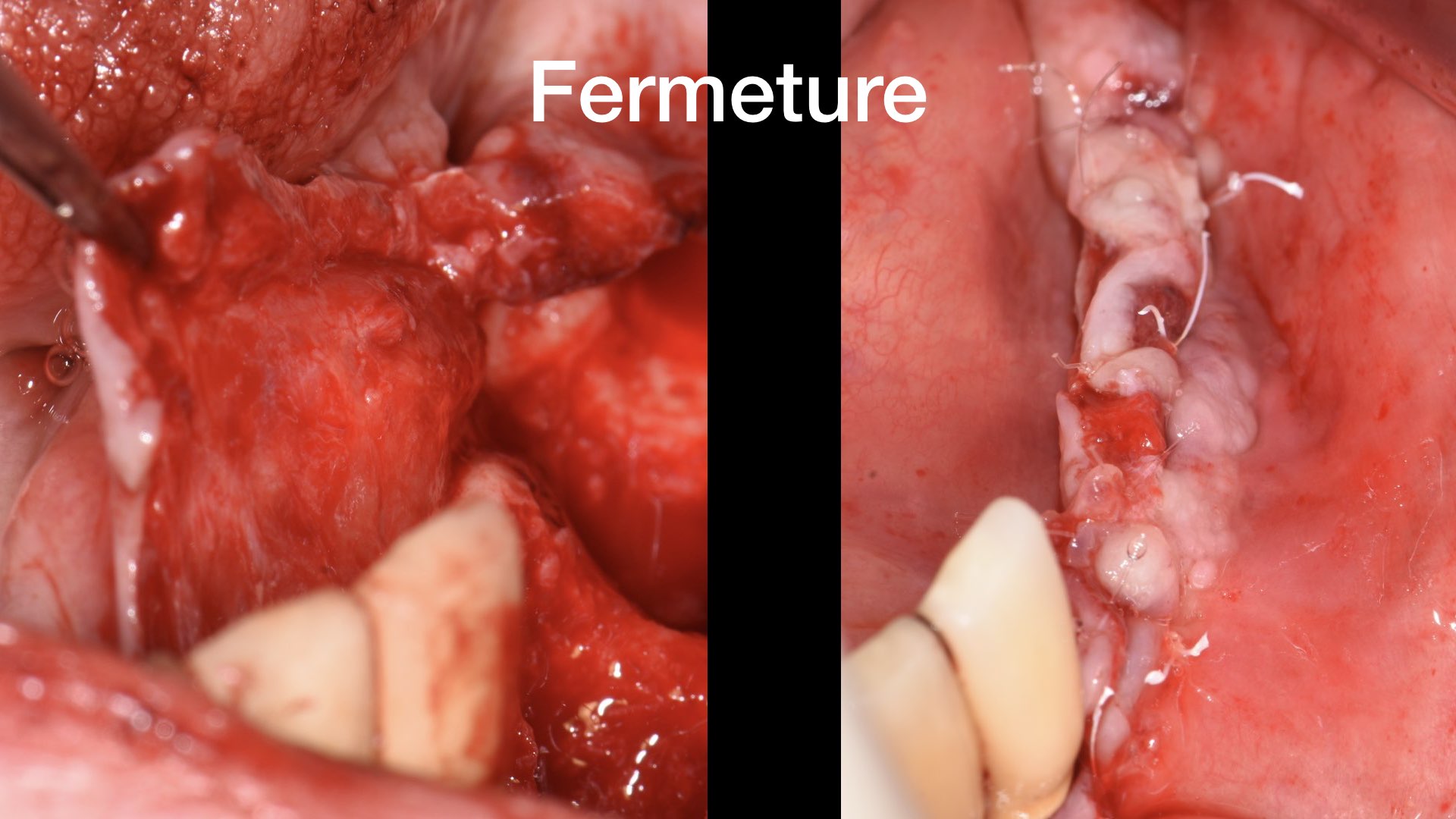
• la fermeture étanche et sans tension de la plaie.
Tinti (1995) (8), Simion (2001) (9), puis Urban (2009) (10)
pour ne citer qu’eux, ont amélioré, protocolisé les méthodes de ROG pour arriver à des gains verticaux
pouvant aller jusqu’à 12 mm.
L’évolution de cette méthode passa par l’incorporation de biomatériaux de type DBBM xénogreffe (Deproteinized Bovine Bone Mineral (DBBM)) mélangés à l’os autogène dans un ratio de 1 :1.
L’os autogène va être incorporé sous forme particulaire, ce qui permettra une adaptation au défaut bien plus importante et simple, une angiogenèse facilitée et apportera des facteurs de croissance (BMP- 2 et TGF-B1).
Les 3 propriétés majeures de l’os autogène sont :
– ostéoconducteur : échafaudage pour la formation osseuse
– ostéogénique : cellules mésenchymateuses (moins dans os cortical)
– ostéoinducteur : facteurs de croissance : BMP, TGFB1 et 2, OSF-1….
Les particules d’hydroxyapatite d’origine bovine (DBBM) vont être associées aux particules d’os autogène et vont permettre de diminuer le volume d’os prélevé, de stabiliser l’os néoformé (11,12) c’est-à-dire de maintenir le volume osseux dans le temps et réduire sa résorption.
Pour les membranes, nous nous attarderons essentiellement dans cet article sur les membranes d-PTFE perforées ou non, qui restent les membranes ayant les meilleurs résultats lors de défaut verticaux (13).
Dans un premier temps, nous allons décrire et suivre le protocole idéal défini par Urban pour un défaut
osseux vertical.
PHASE PRÉ OPÉRATOIRE
• Sélection du patient : ASA 1 ou 2 sans affection systémique évolutive ou maladie parodontale non maitrisée
• Avulsion ou dépose d’implant 2 mois avant
• Ne pas garder de dents « suspectes » en distale d’une ROG verticale
• Détartrage et motivation à l’hygiène
• Arrêt complet du tabac
• ATB à commencer 2 jours avant
• Prévoir une sédation per os (un patient stressé lors de la chirurgie augmentera le risque d’erreur de la part du chirurgien)
• Analyse de la Vitamine D et supplémentation si nécessaire
Il va falloir évaluer la motivation du patient car ces interventions ne sont clairement pas simples en per et post opératoire et le patient doit être averti des suites ainsi que des échecs partiels possibles .Il doit évidemment présenter une bonne hygiène buccale avant mais aussi après la chirurgie.
La première étape est le parage de la zone opératoire ; j’utilise pour ma part de la bétadine jaune pour la zone cutanée péri buccale ainsi que pour le nettoyage intra buccal du défaut osseux et des dents adjacentes.
Suite à l’anesthésie locale ou loco régionale, nous allons faire une incision qui sera supra périostée dans un premier temps.
L’incision crestale sera légèrement décalée en vestibulaire au maxillaire et pourra être plus médiane à la mandibule, elle sera ensuite sulculaire et s’étendra à 2 dents du site à greffer (Fig. 4).
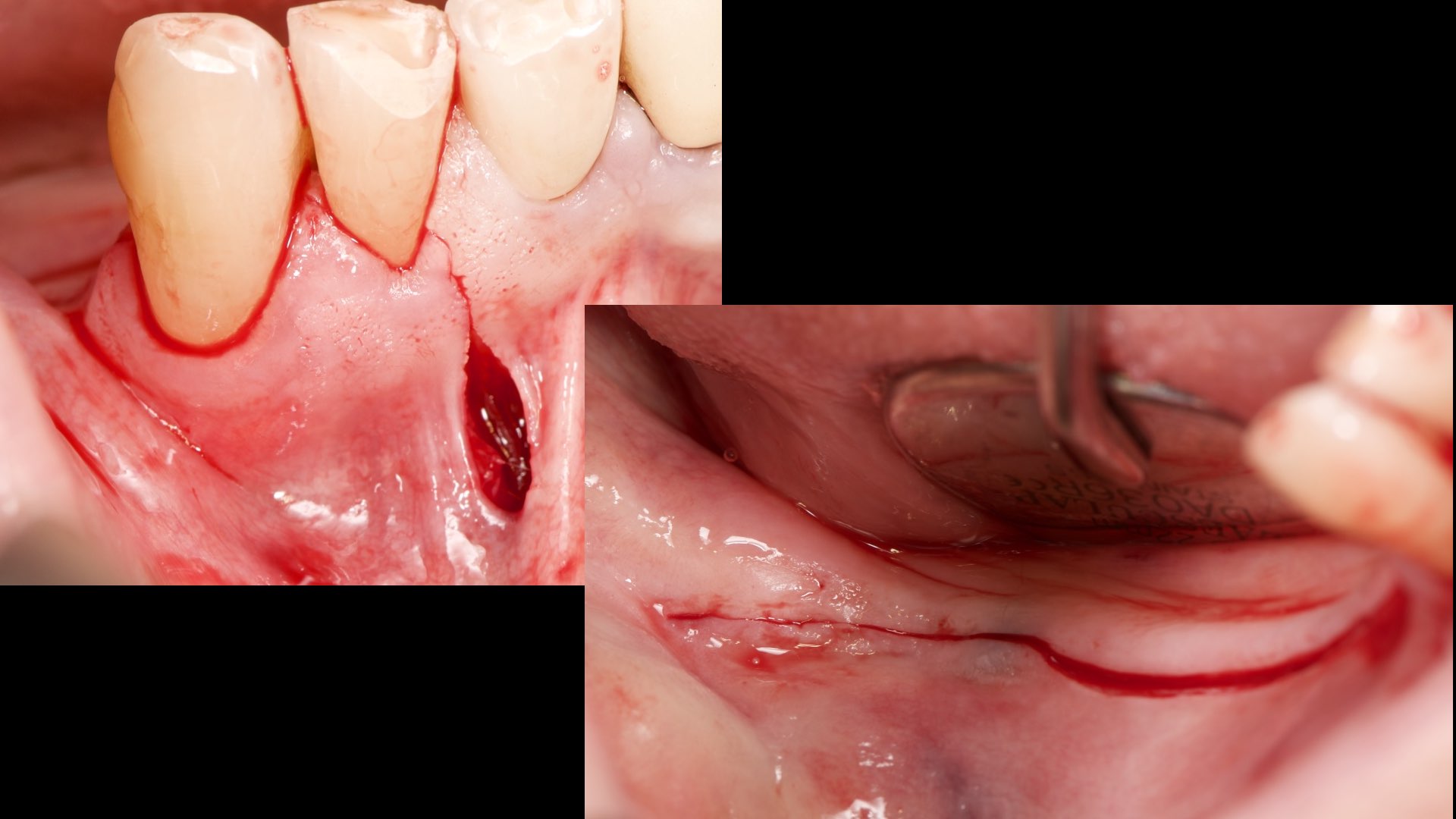
Puis, 2 décharges de 3-4 mm au-delà de la LMG et plutôt arciformes « C-shape » seront faites.
Après avoir changé de lame, nous pourrons faire l’incision périostée suivant le trajet de la première incision.
Pour le décollement muco périosté, il sera d’abord vestibulaire puis on isolera le trou mentonnier si zone mandibulaire postérieure (Fig. 5).
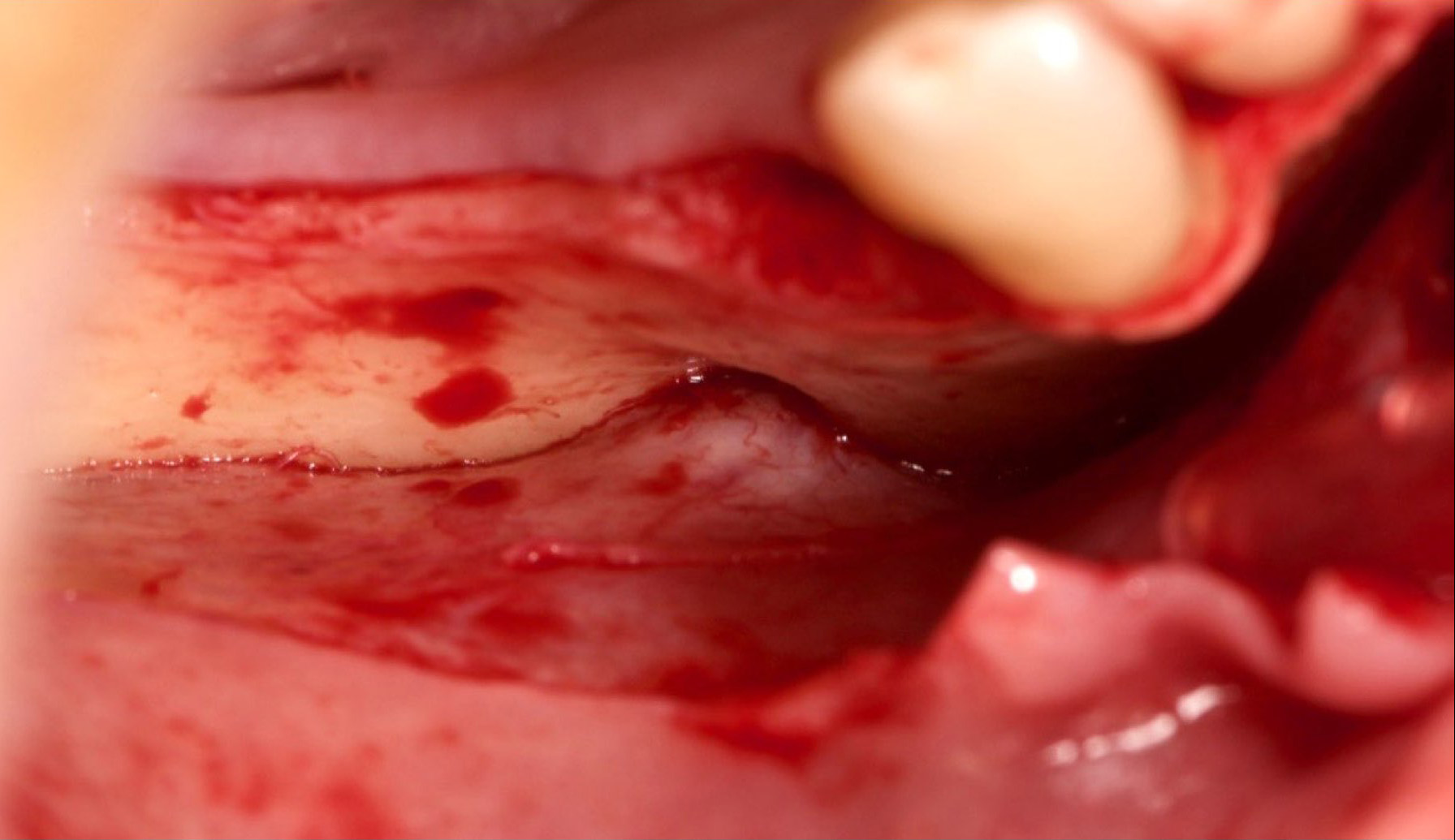
Puis, faire une mini décharge palatine ou linguale de 6 mm de long au niveau distal de la 1ère dent (Si défaut > 4 mm), ensuite décollement lingual ou palatin.
Nous finirons par le surfaçage des racines des dents bordant l’édentement avec curettes de Gracey.
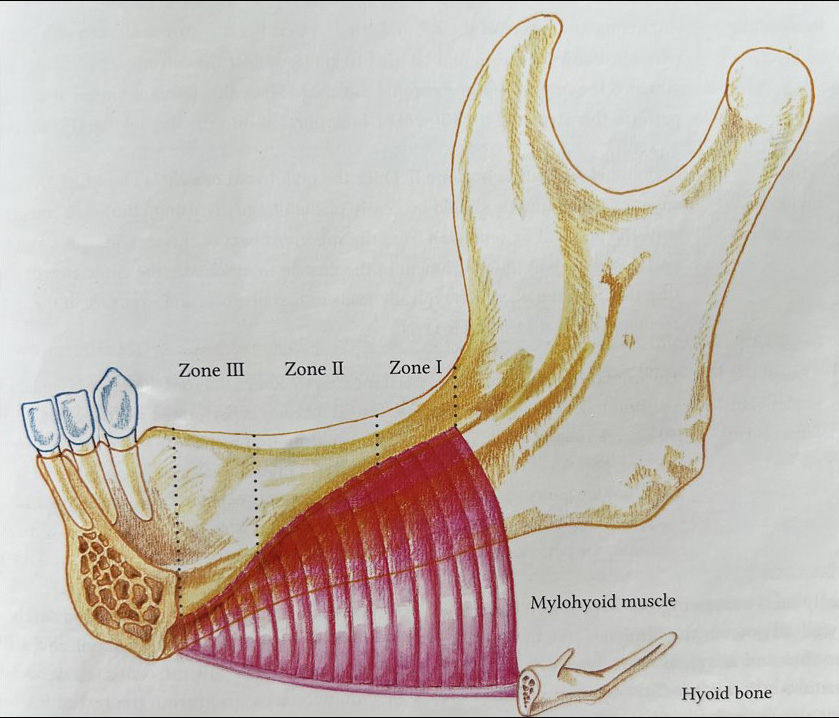
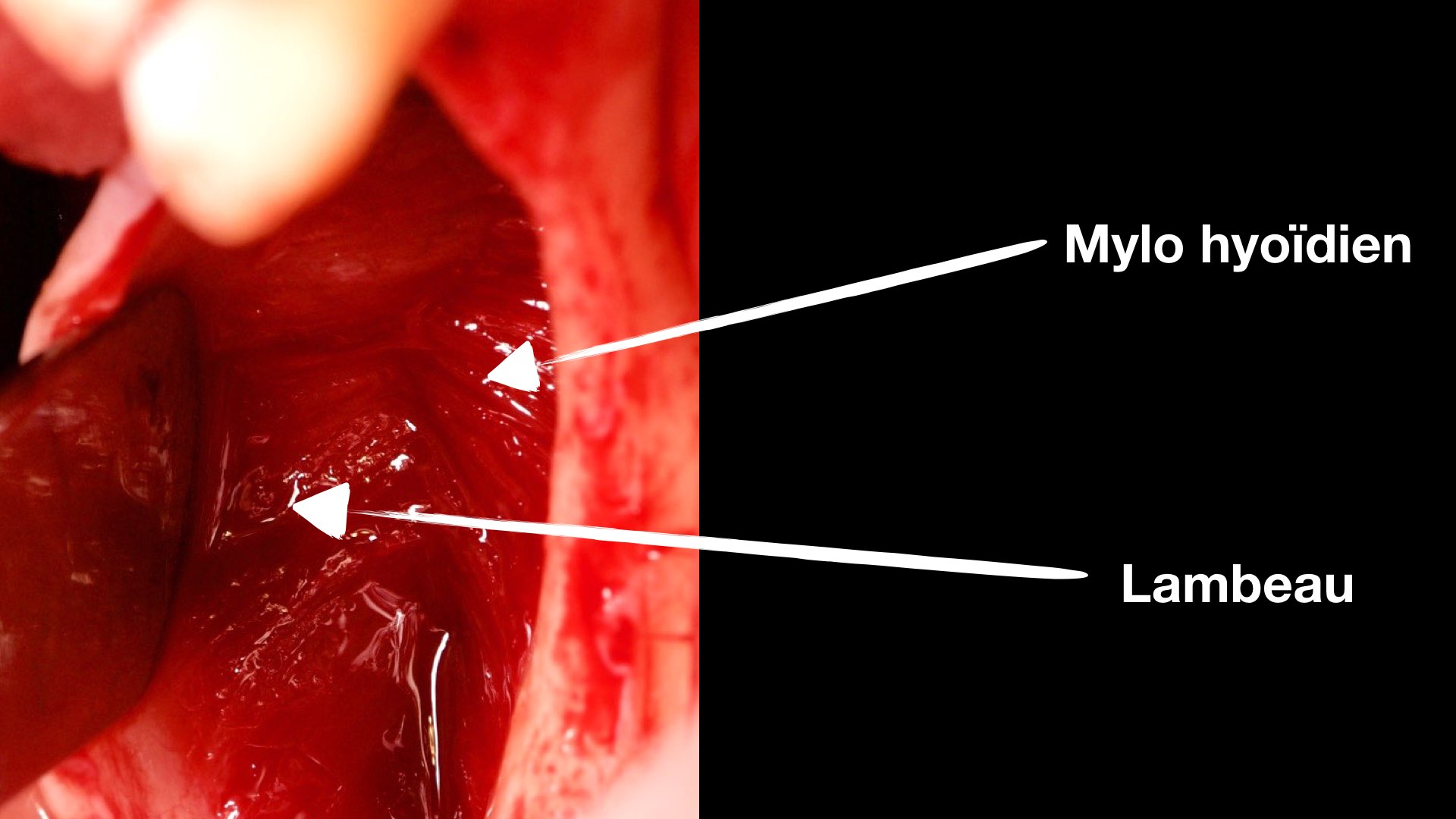
Dès cette étape réalisée, nous allons pouvoir libérer le lambeau lingual (Fig. 6 et 7) suivant 3 zones :
• zone 1 : on décolle le coussinet rétromolaire en direction coronale.
• zone 2 : quand on arrive à l’insertion du mylo hyoïdien, on sépare le lambeau du muscle sans le
disséquer en poussant les tissus avec décolleur ou Mini-Me en direction linguale.
• zone 3 : décharge linguale
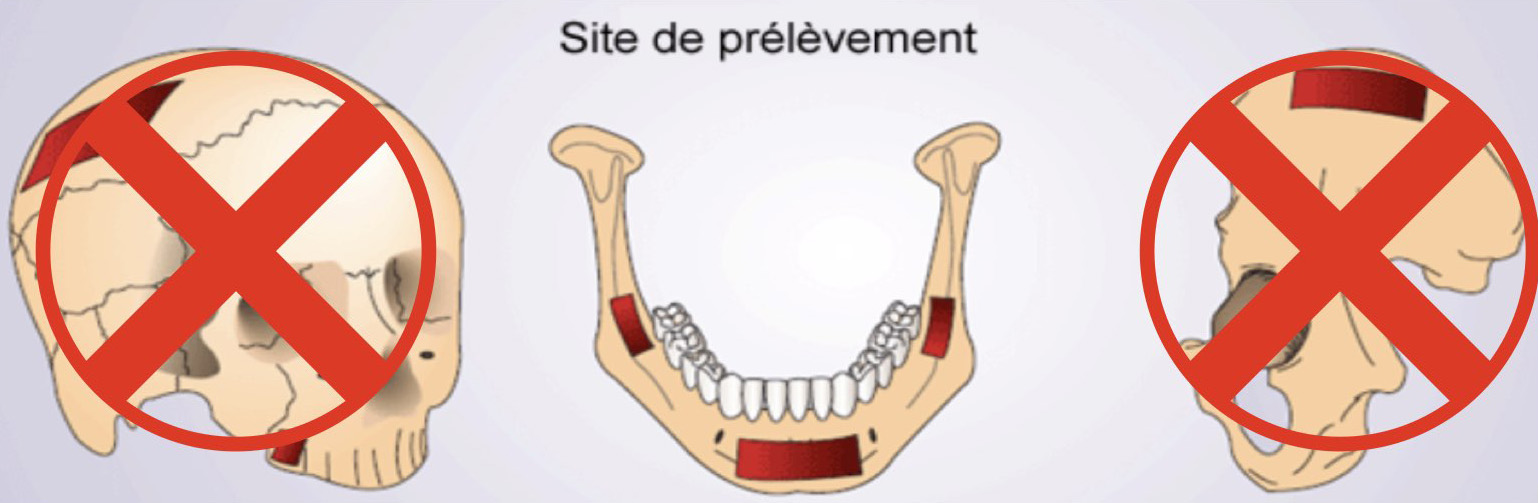
Le prélèvement d’os autogène se fera en intra buccal (Fig. 8) (14) à l’aide de Bonescraper ou Micross mais
nous pourrons aussi utiliser des tarauds et les broyer avec un moulin à os (Fig. 9 et 10).
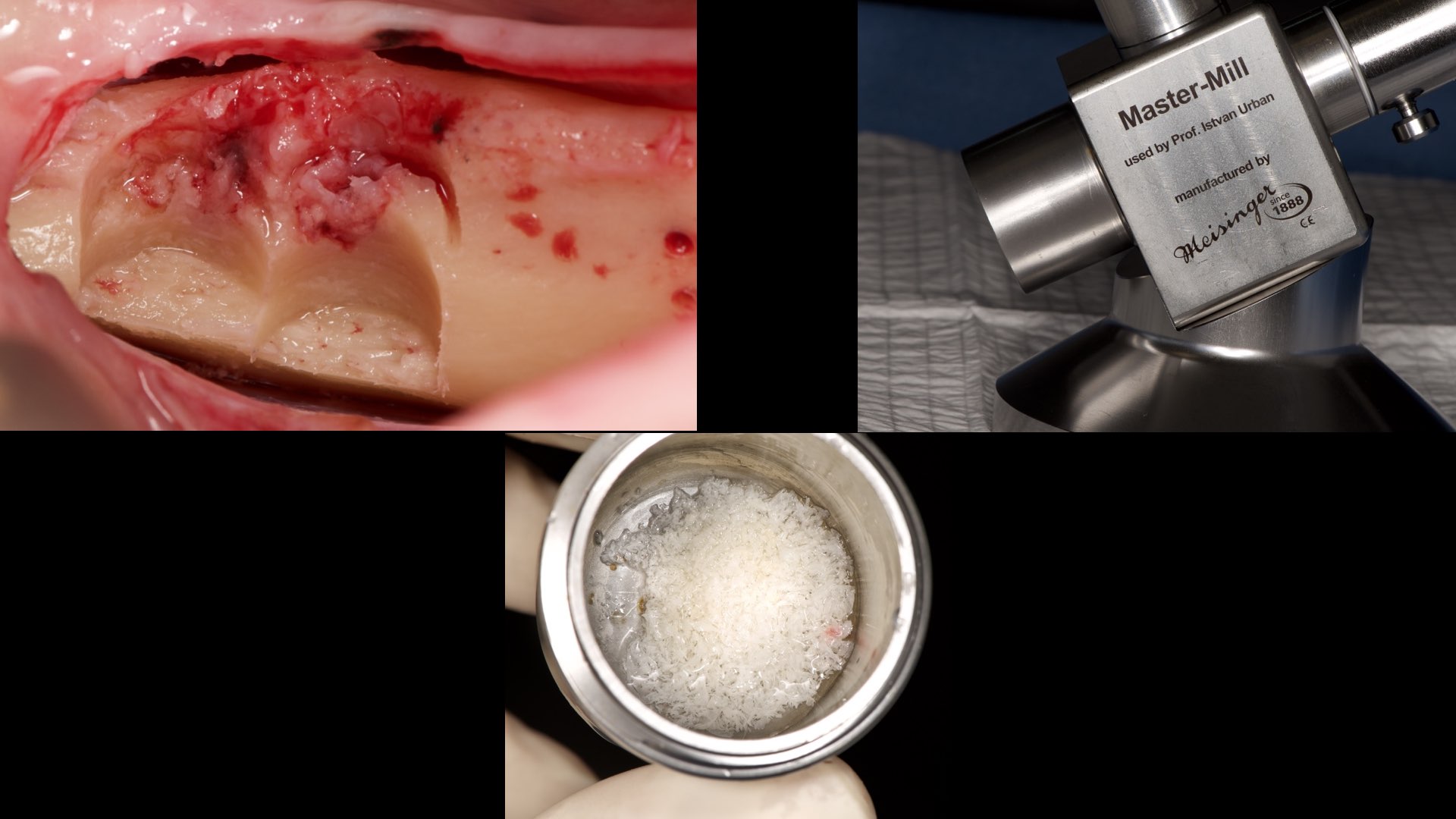
L’os autogène ainsi récupéré sera mélangé à de la xénogreffe dans un rapport 50-50 et jusqu’à 60-40.
La membrane PTFE sera ensuite découpée pour être à distance des dents de 1,5 à 2 mm dans le sens
horizontal mais laissée complète dans le sens vertical pour l’instant.
Elle pourra être pré-courbée pour lui donner déjà une « forme » adaptée au défaut.
La fixation de la membrane est une étape clé de la ROG, elle ne devra permettre aucun mouvement à la
membrane et bien la plaquer autour du défaut.
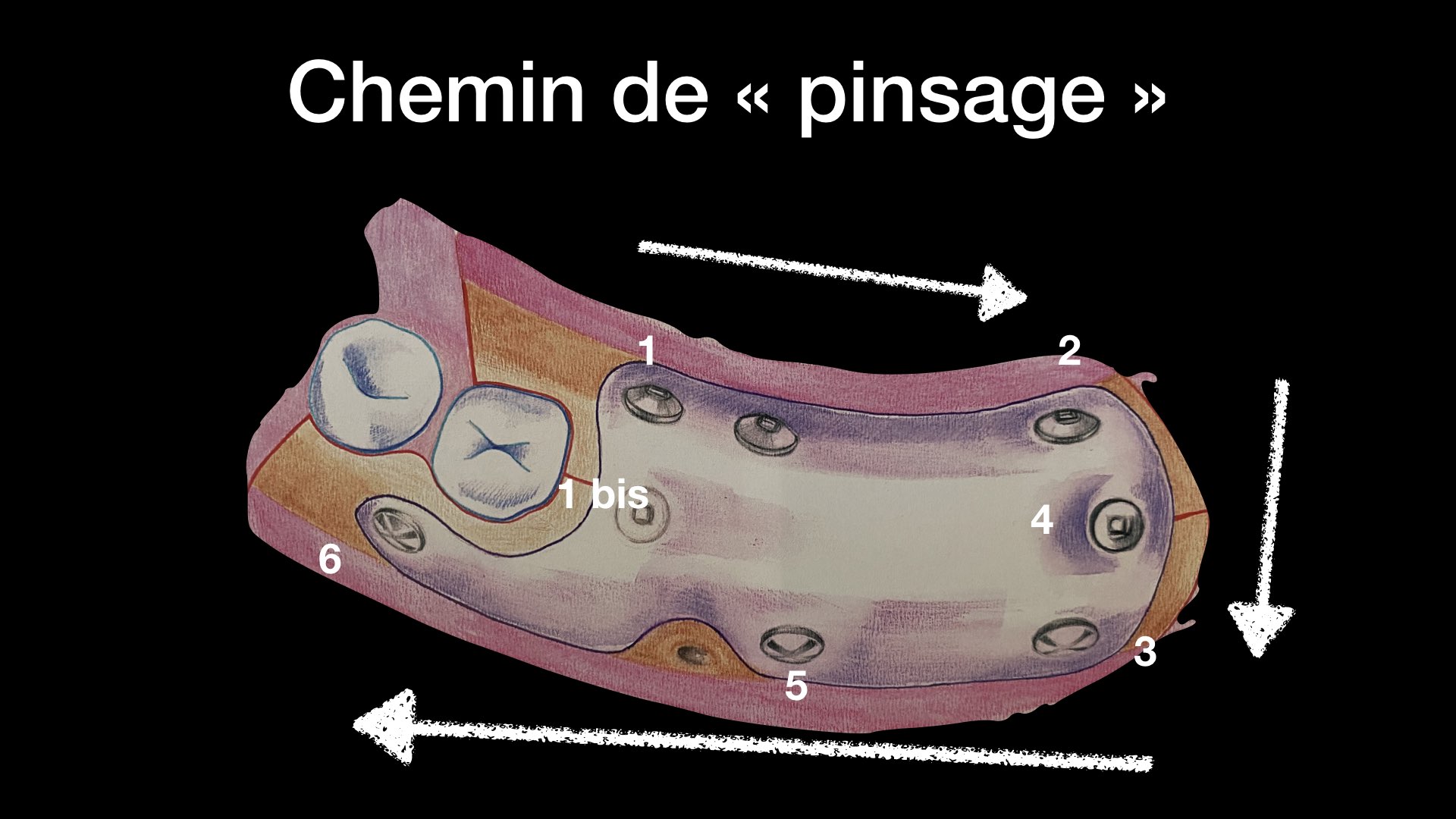
La fixation commencera en mésio lingual ou palatin puis distale, elle se fera soit avec des pins (3 mm) ou
des micro vis (3 mm).
A ce stade, les perforations de la corticale osseuse seront réalisées ce qui permettra un apport sanguin et facilitera l’angiogenèse, par contre ne pas les faire avant car le saignement pourrait gêner les étapes antérieures.
Nous passons à l’étape d’embossage, c’est-à-dire le comblement par le mélange os autogène/xénogreffe du défaut osseux.
Il ne faut pas hésiter à remélanger car les particules de xénogreffe ont tendance à se concentrer au fond de la cupule utilisée.
L’apport se fera par petite quantité afin de pouvoir tasser le mélange au fur et à mesure (en garder un peu), ce n’est qu’ensuite que la membrane sera fixée en vestibulaire en commençant par la fixation distale puis venir en mésiale mais laisser une trappe par laquelle nous ferons un dernier apport osseux. La fixation sera fine lors de l’impaction du pins mésio vestibulaire.
Veillez à ce que la membrane ne fasse pas de plicature sinon n’hésitez pas à l’inciser et la suturer pour effacer ces plis (Fig. 11).
Pour fermer tout cela, il va falloir libérer le lambeau vestibulaire, nous commençons donc par une incision du périoste et uniquement du périoste de notre lambeau vestibulaire, à 2-3mm de la LMG en fonction de l’épaisseur des tissus mous, d’une décharge à l’autre. Il faut respecter une distance de sécurité de 10 mm du trou mentonnier.
Utiliser une lame 15C retournée pour couper des faisceaux restants (cordes de guitare) une à une, puis
étirer les fibres avec Mini-Me ou décolleur au niveau d’incision.
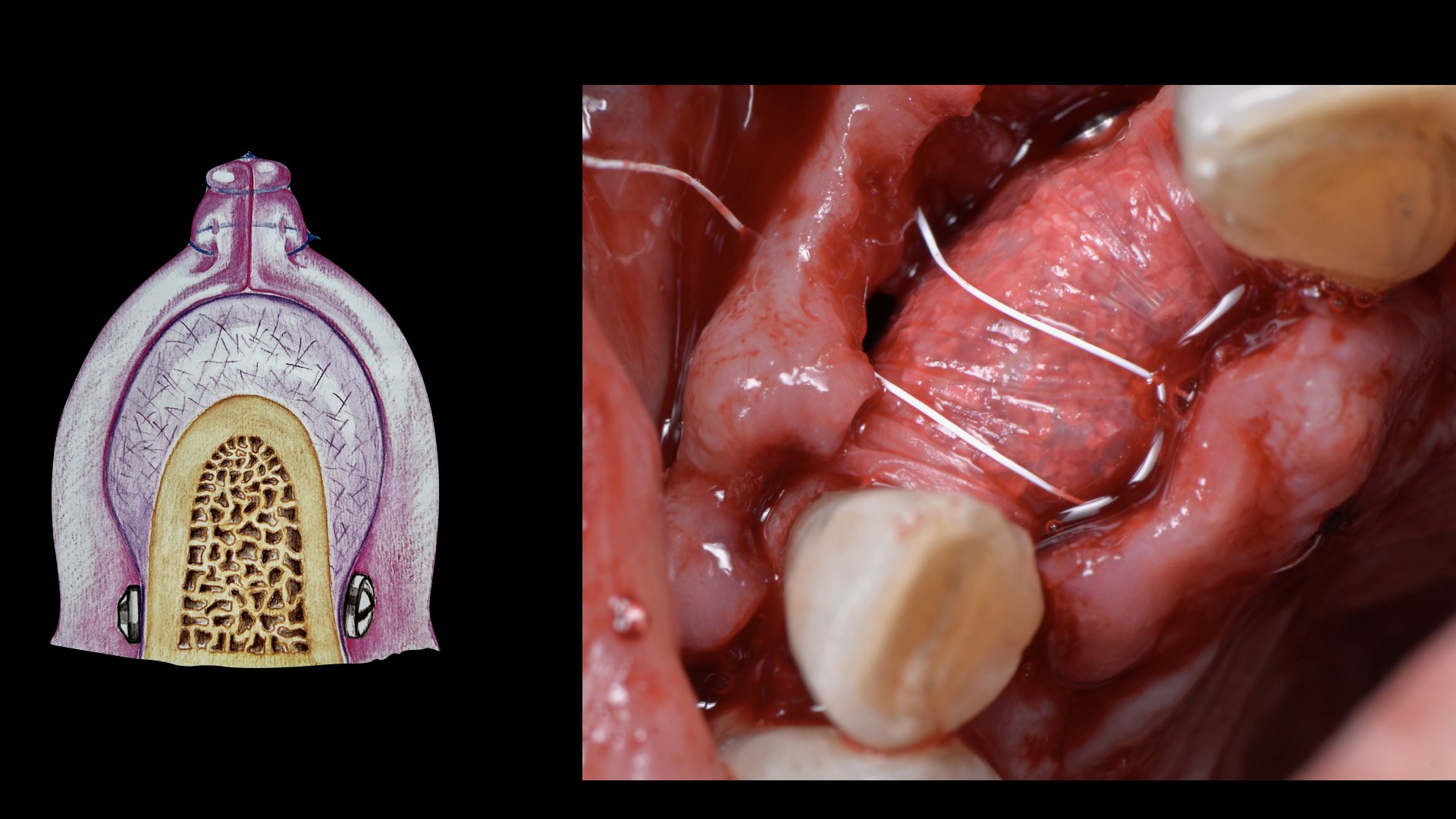
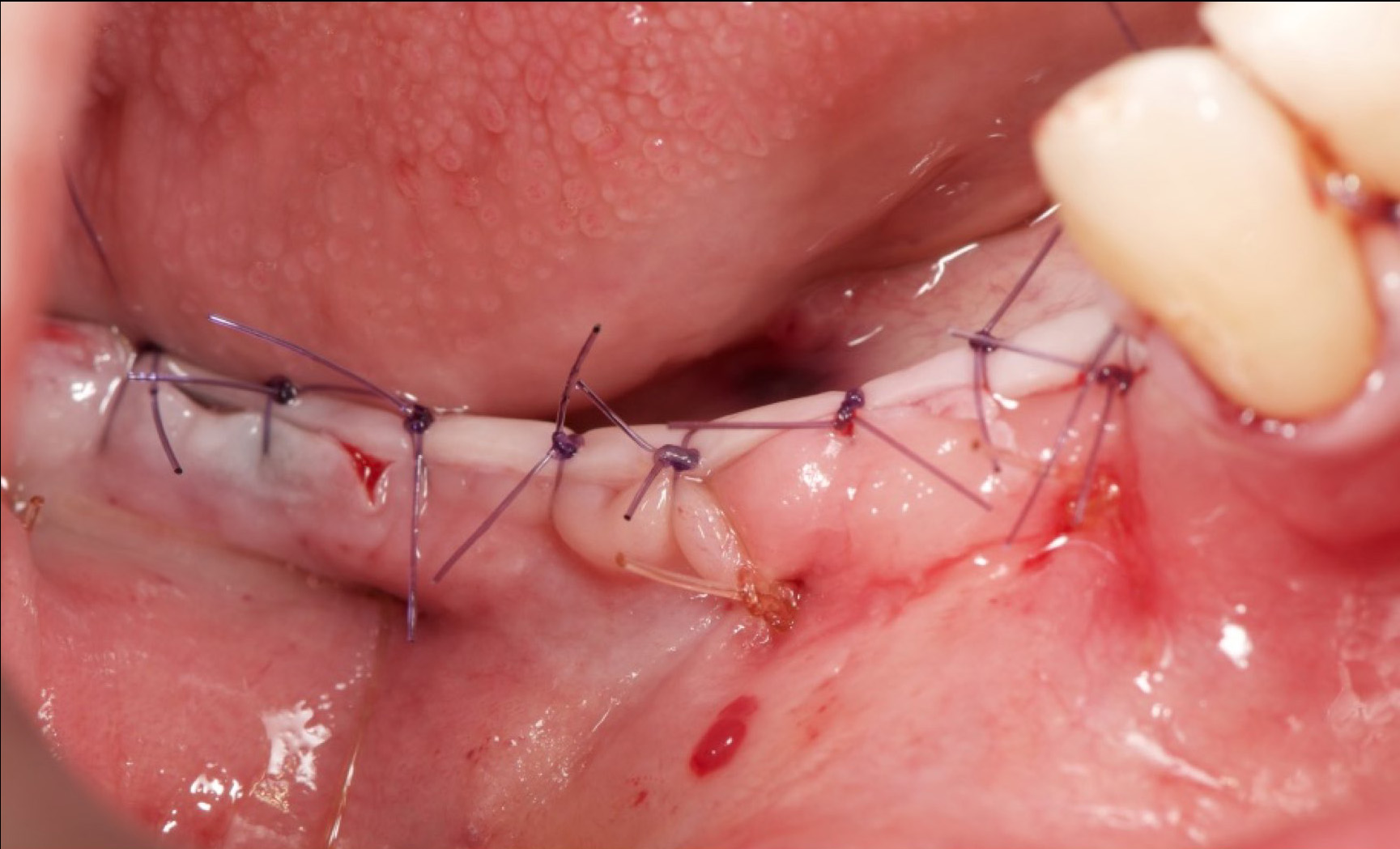
Les sutures sont réalisées en deux plans : des matelassiers horizontaux (PTFE 3 ou 4-0 ou alors Monocryl 3-0) pour créer une surface de contact d’au moins 3 mm d’épaisseur, alternés avec des sutures simples interrompues (Monocryl 5-0) (Fig. 12 et 13).
Ce protocole a clairement changé mon activité quotidenne au cabinet pour gérer tant des défauts horizontaux que verticaux mais soyons sincère, ma courbe d’apprentissage fut longue et semée d’embûches.
Ces échecs ont découlé d’erreurs de ma part pour la grande majorité des cas, et comme l’a dit un grand
homme « la pire erreur n’est pas dans l’échec, mais dans l’incapacité de dominer l’échec ». Donc après
avoir ravalé son ego, le plus important dans ces cas d’échec fut de reprendre toute la chronologie de la
chirurgie, de relever les erreurs et d’en comprendre l’impact, d’où l’importance d’iconographier ses cas et
surtout ses premiers cas.
Au travers de quelques cas d’échec, nous allons relever les erreurs les plus courantes identifiées selon
moi dans ce genre de chirurgie.
CAS CLINIQUE 1
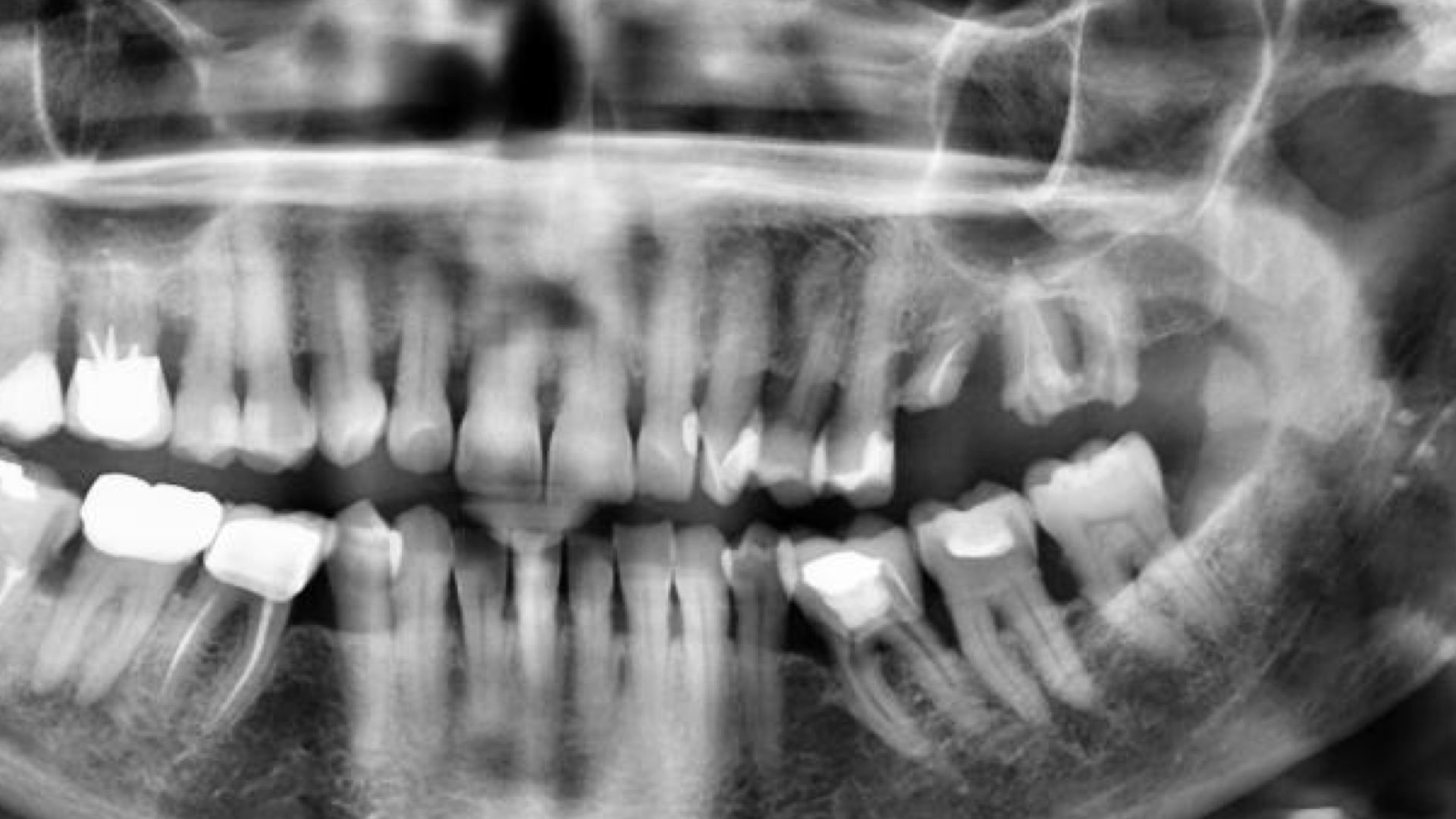
Une patiente se présente au cabinet pour une réhabilitation du secteur 2, elle présente une alvéolyse au niveau des dents 26 et 27 qui sont à l’état de racines résiduelles. La pose d’implant dans ce contexte semble compromise car nous avons un défaut osseux vertical.
La solution de réhabiliter le tissu dur à ce niveau fut prise avant de poser 2 implants.
Le choix de la ROG avec membrane non résorbable associée à un comblement sinusien, fut pris en accord avec la patiente assez réticente à une greffe osseuse autogène devant associer un deuxième site opératoire de prélèvement.
Lors du choix thérapeutique, une erreur capitale a été faite ; la 25 était condamnée et la patiente n’était prête à perdre ni sa 26, ni sa 27 et encore moins sa 25 mais clairement le pic osseux en distal de 25 était défavorable à une ROG. J’ai fait un compromis dont les conséquences furent néfastes pour le résultat.
Clairement, ce type de chirurgie ne peut être faite avec des compromis, même si cela est toujours beaucoup plus facile à dire à posteriori que lors de la 1ère ou de la 2ème consultation (Fig. 14).
Lors des incisions crestales et de décharge (Fig. 15), nous aurions dû anticiper le fait de devoir peut-être extraire la 25, j’ai malheureusement fait une incision de décharge en mésial de 24, et du coup en prenant le risque d’avoir une décharge à 1 dent de l’édentement en cas d’avulsion, ce qui fut évidemment le cas.
Notons aussi que l’incision crestale était trop médiane voir clairement trop palatine, ce qui fut problématique pour l’affrontement des tissus conjonctifs des 2 lambeaux palatin et vestibulaire.
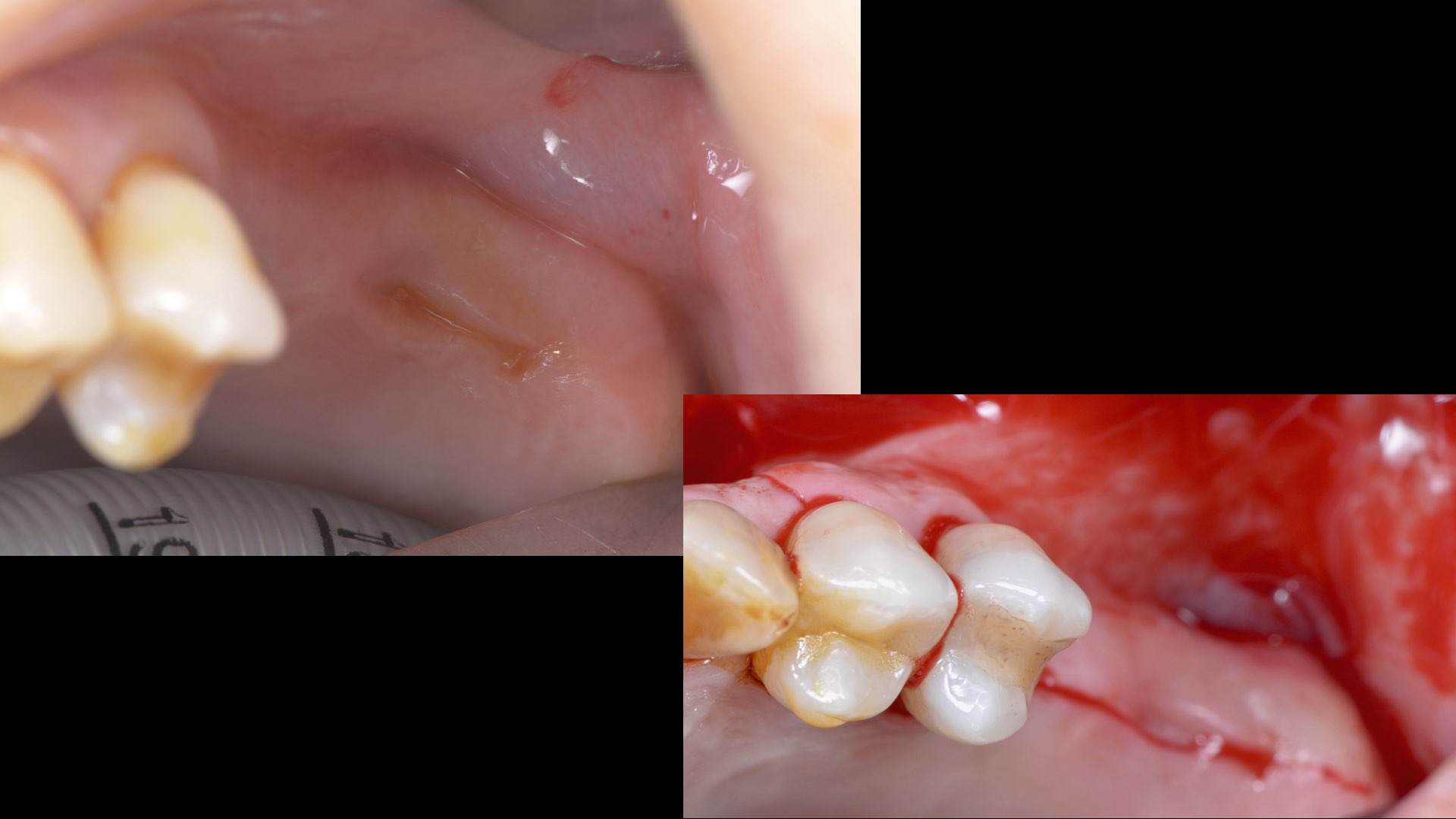
Apres le décollement muco périosté, nous avons pu évaluer le défaut osseux en distal de 25, celui-ci était un défaut en V assez profond qui nous obligea à extraire la 25 en per opératoire : cela eu pour conséquence de mettre la décharge à 1 dent de la ROG et de ne pas avoir les 6-8 semaines de cicatrisation préconisées par I. Urban avant toute réhabilitation osseuse.
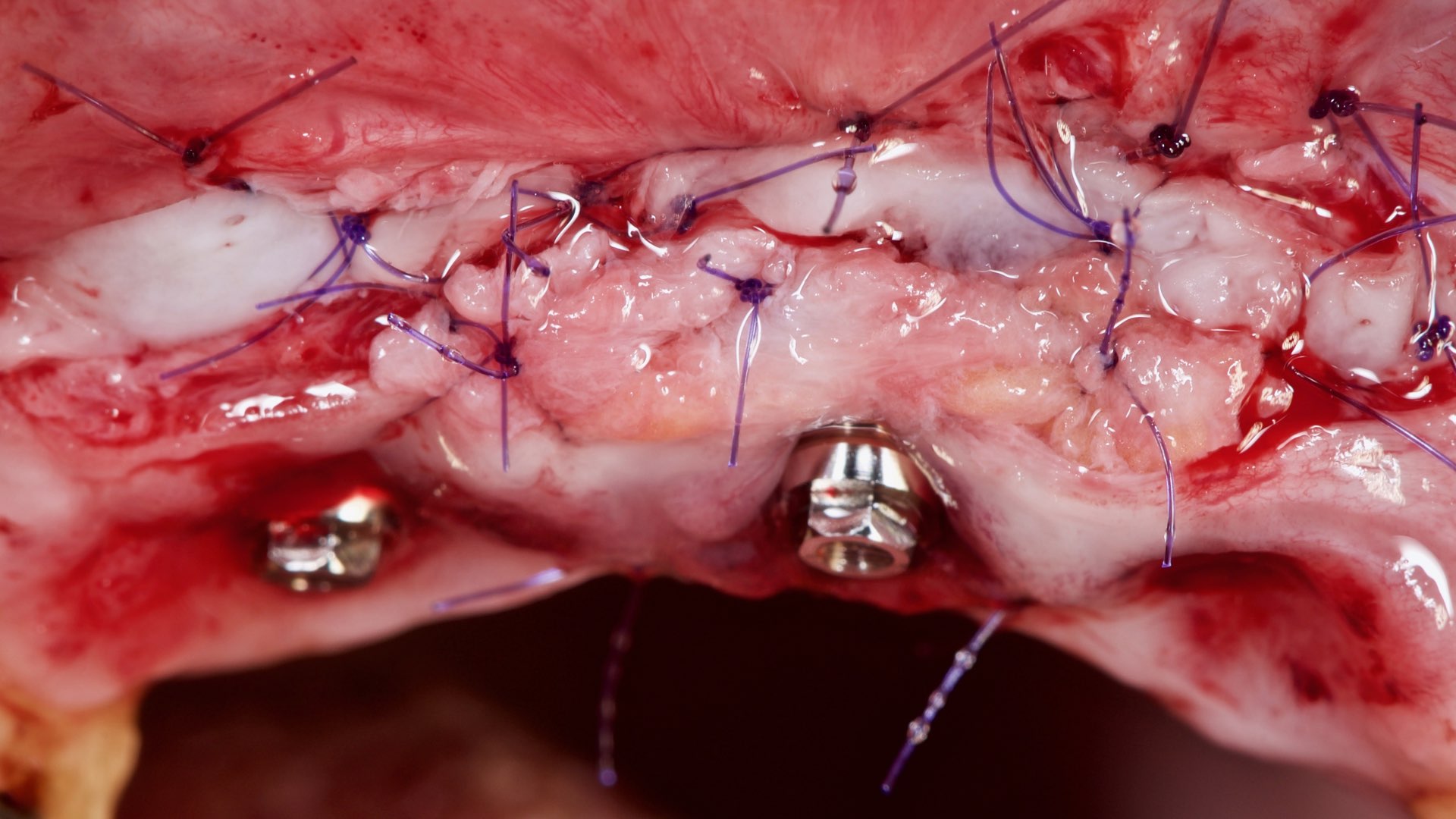
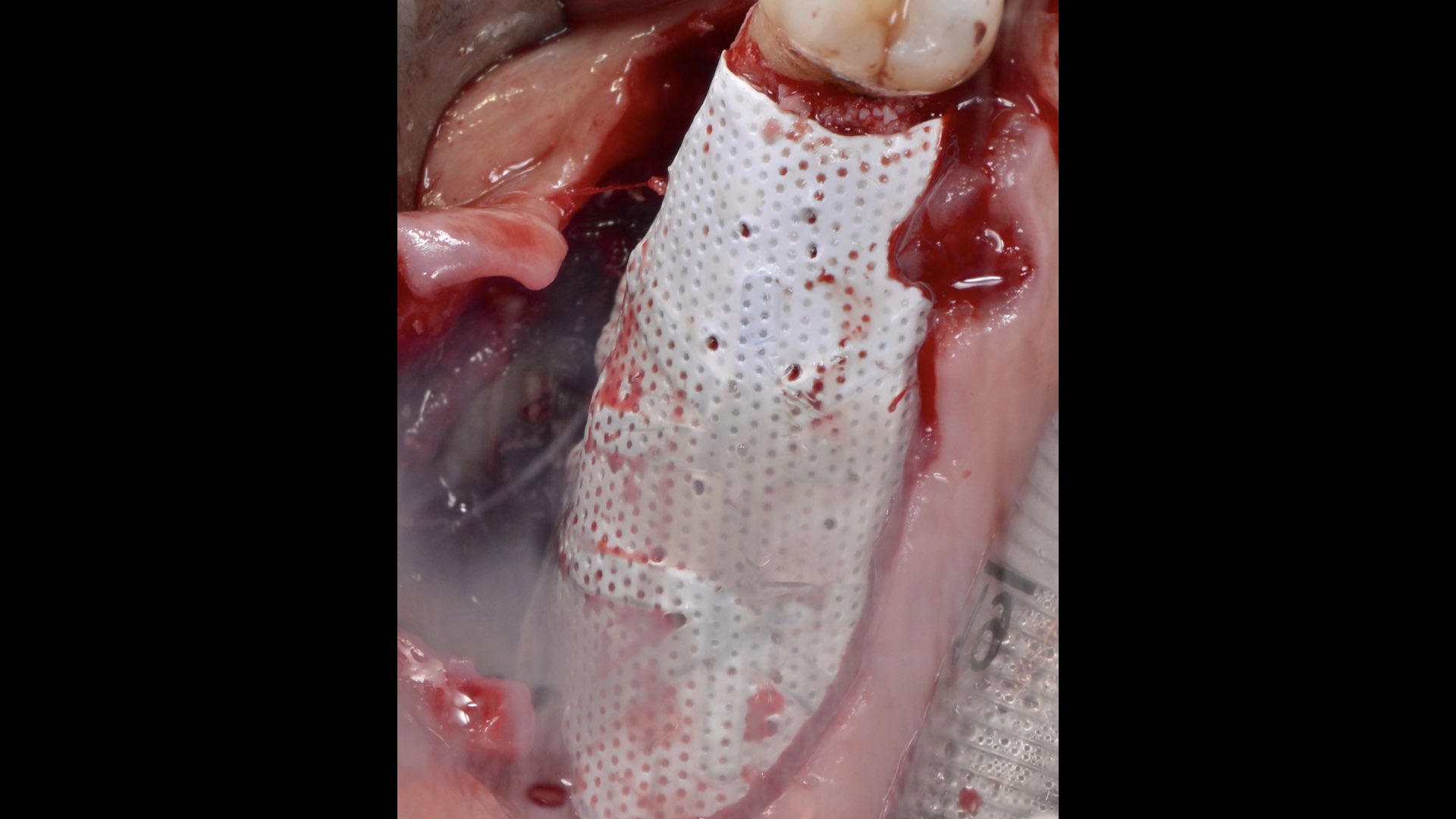
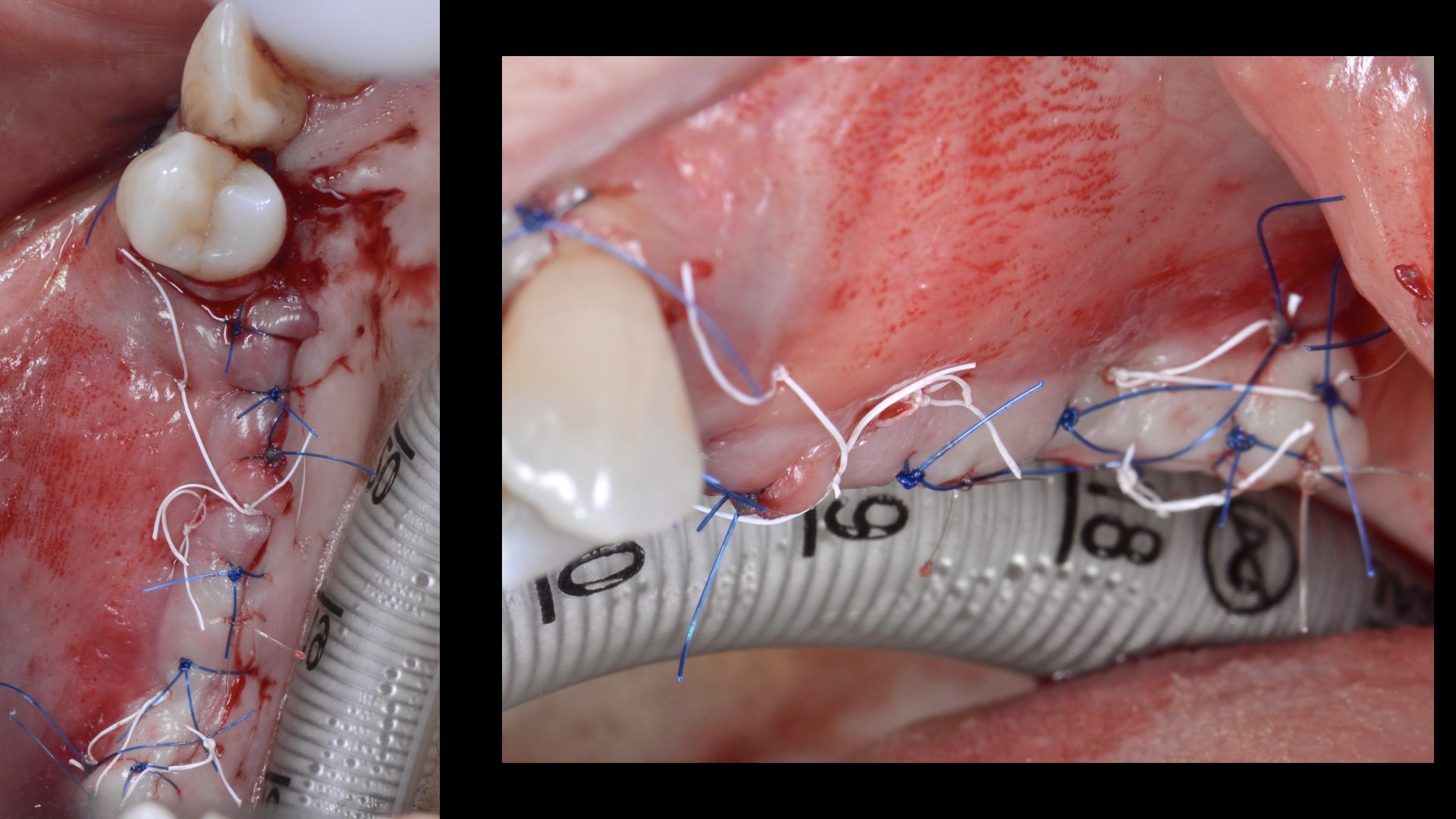
Nous avons quand même réalisé la ROG avec une membrane PTFE et réalisé la fermeture hermétique (Fig.
16 et 17).
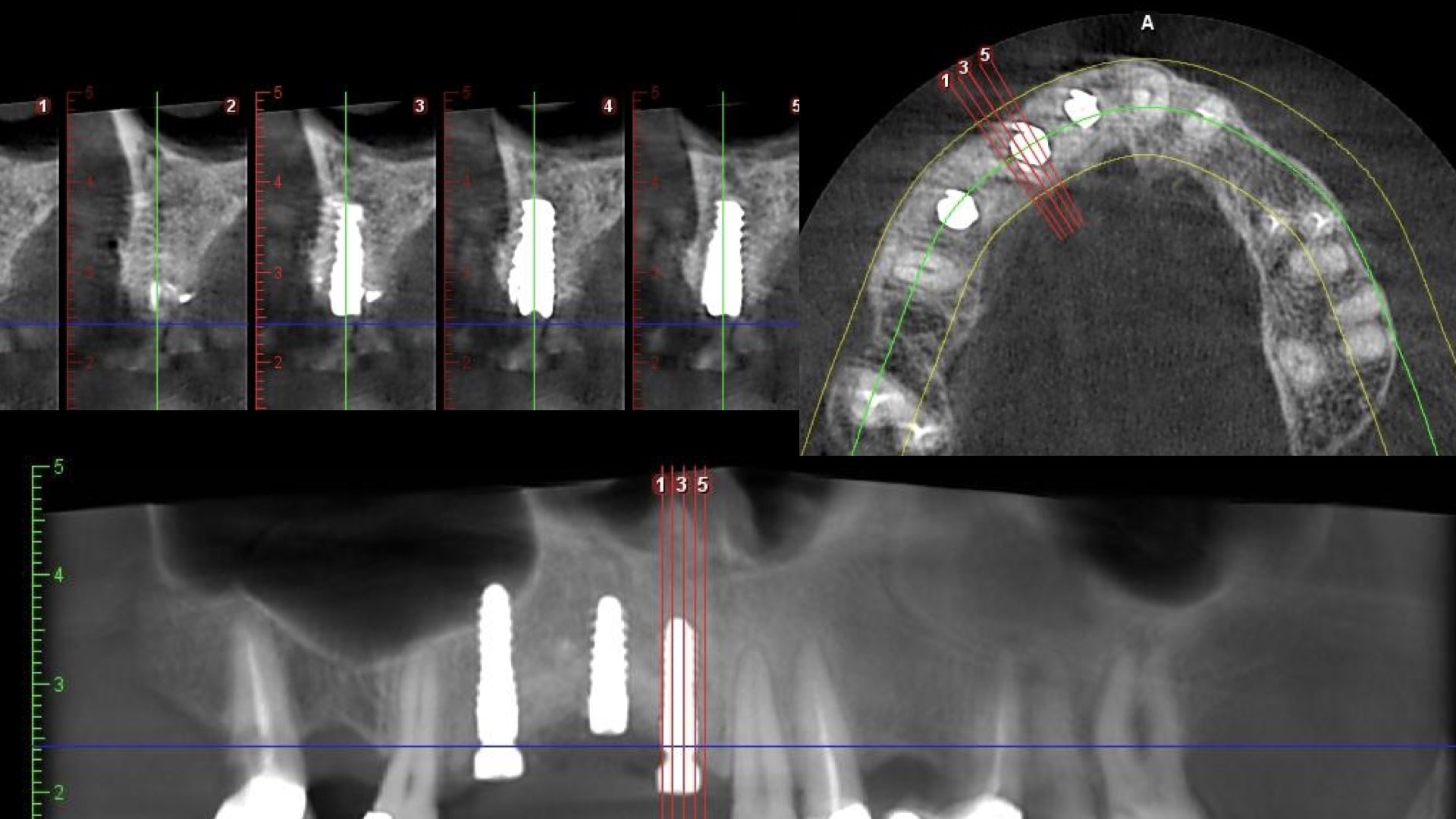
Le scanner de contrôle montre aussi un matériau de comblement sinusien pas assez tassé au niveau de la
paroi médiane du sinus (Fig. 18).
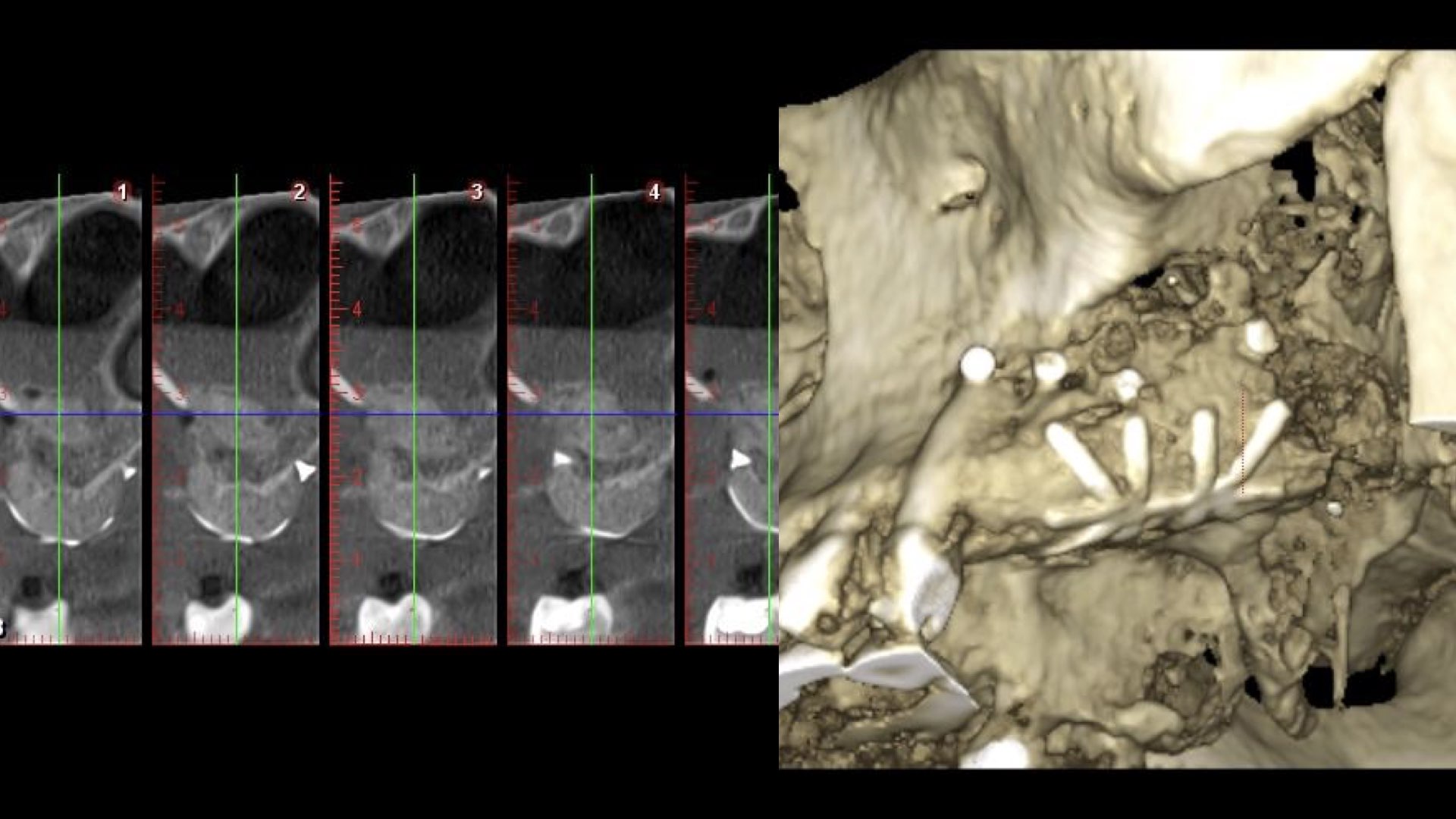
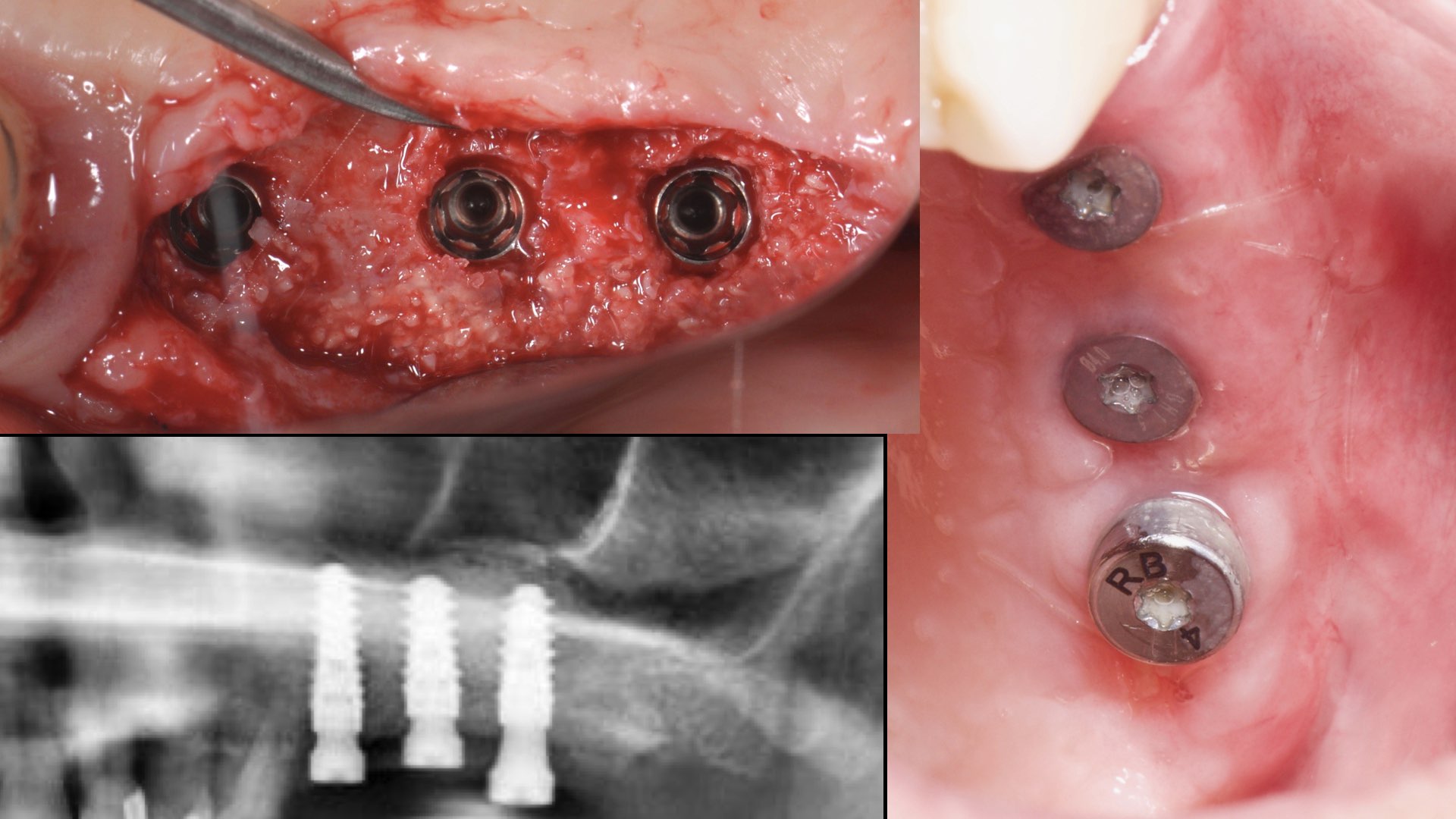
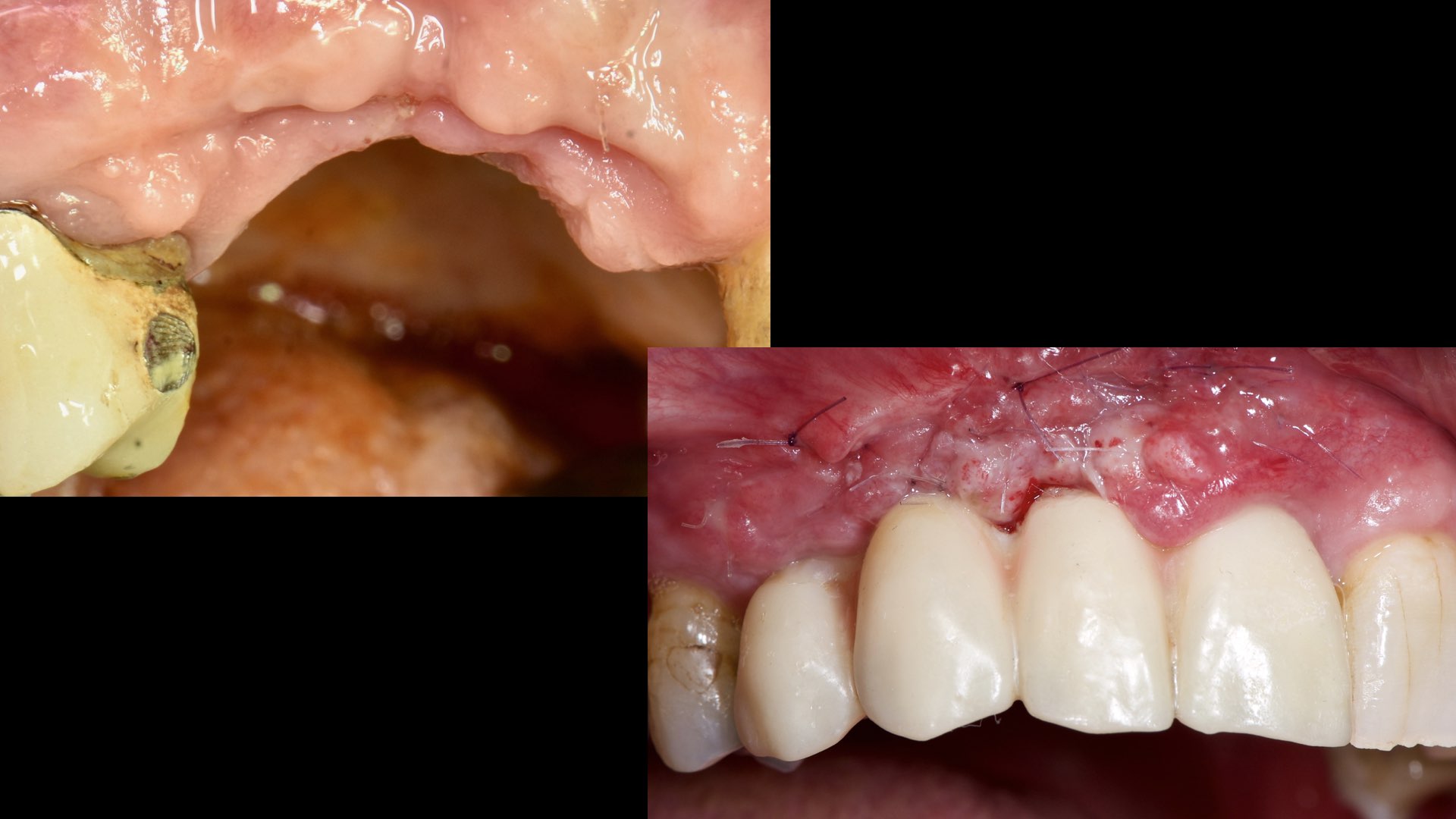
La conséquence de ces erreurs fut une réouverture du site à 7 semaines (ouverture > 3mm) mais sans signe clinique d’infection. Nous avons déposé la membrane à 8 semaines après une reprise d’ATB (3G Amoxicilline/j pdt 7 jours et un nettoyage soigneux de la zone par la patiente pour palier à tout risque de surinfection. Le fait d’avoir une exposition assez tardive et non infectée a permis de conserver le tissu ostéoide qui s’était formé et finalement d’avoir un gain osseux suffisant pour poser 3 implants (Fig. 19), avec un aménagement des tissus mous grâce un lambeau positionné apicalement et greffe de conjonctif sur la partie en demi épaisseur exposée.
CAS CLINIQUE 2
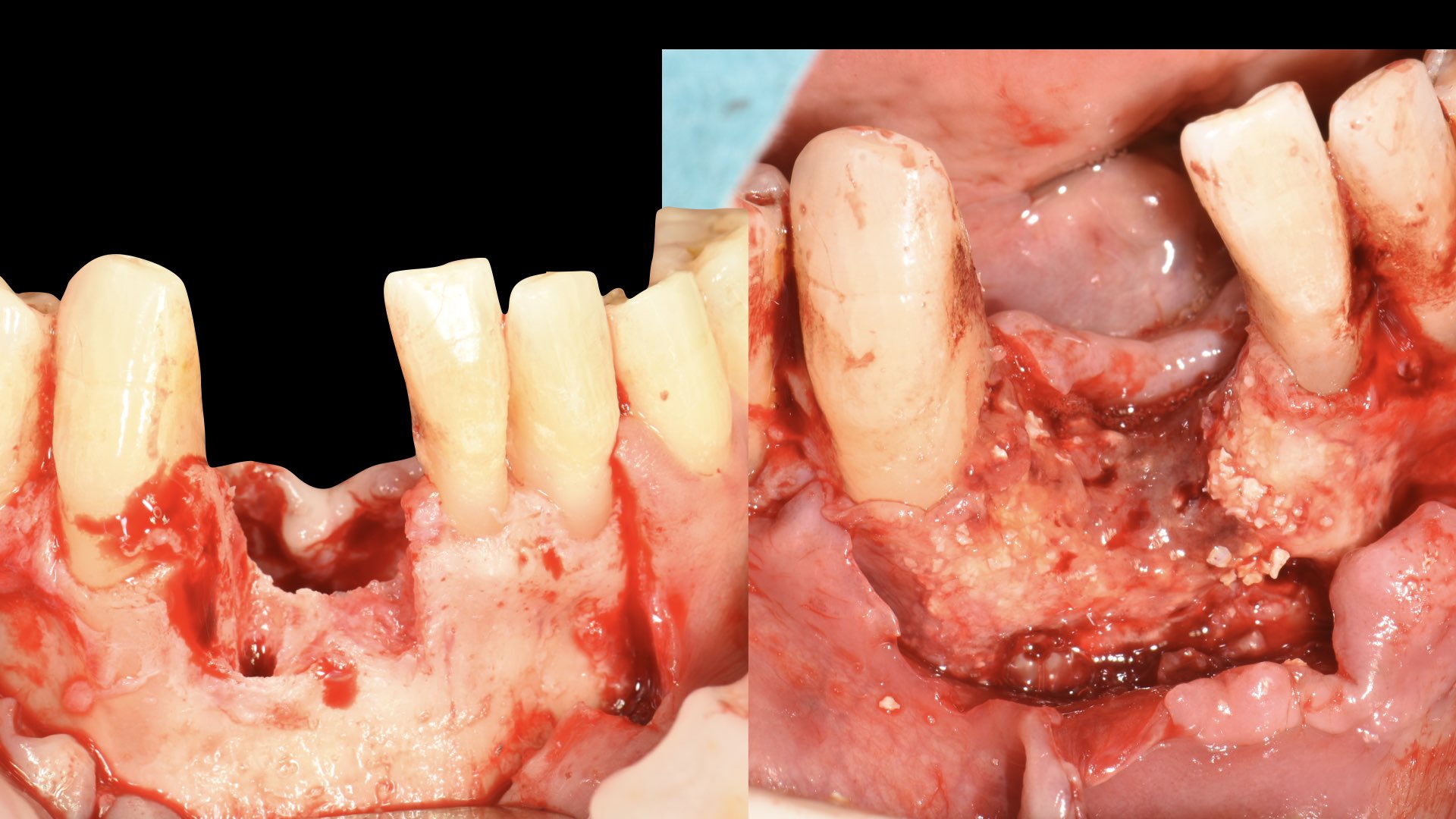
Nous avons repris un patient du cabinet, implanté il y a quelques années en secteur 11- 12 – 13. Un défaut de gencive kératinisée et des implants trop antérieurs ont entrainé une péri implantite, vue et prise en charge bien trop tard. Le patient présente, après dépose des implants, un défaut osseux vertical majeur (Fig. 20 et 21).
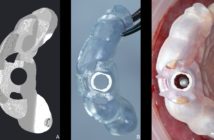
Nous avons à l’époque pris la décision d’une ROG avec une grille titane de 2 mm (IPP Pharma) avec un mélange d’os autogène prélevé au niveau de la ligne oblique externe avec des tarauds et broyé au moulin à os (Meisinger), avec une xénogreffe (Bio Oss) à 50-50 (Fig. 22).
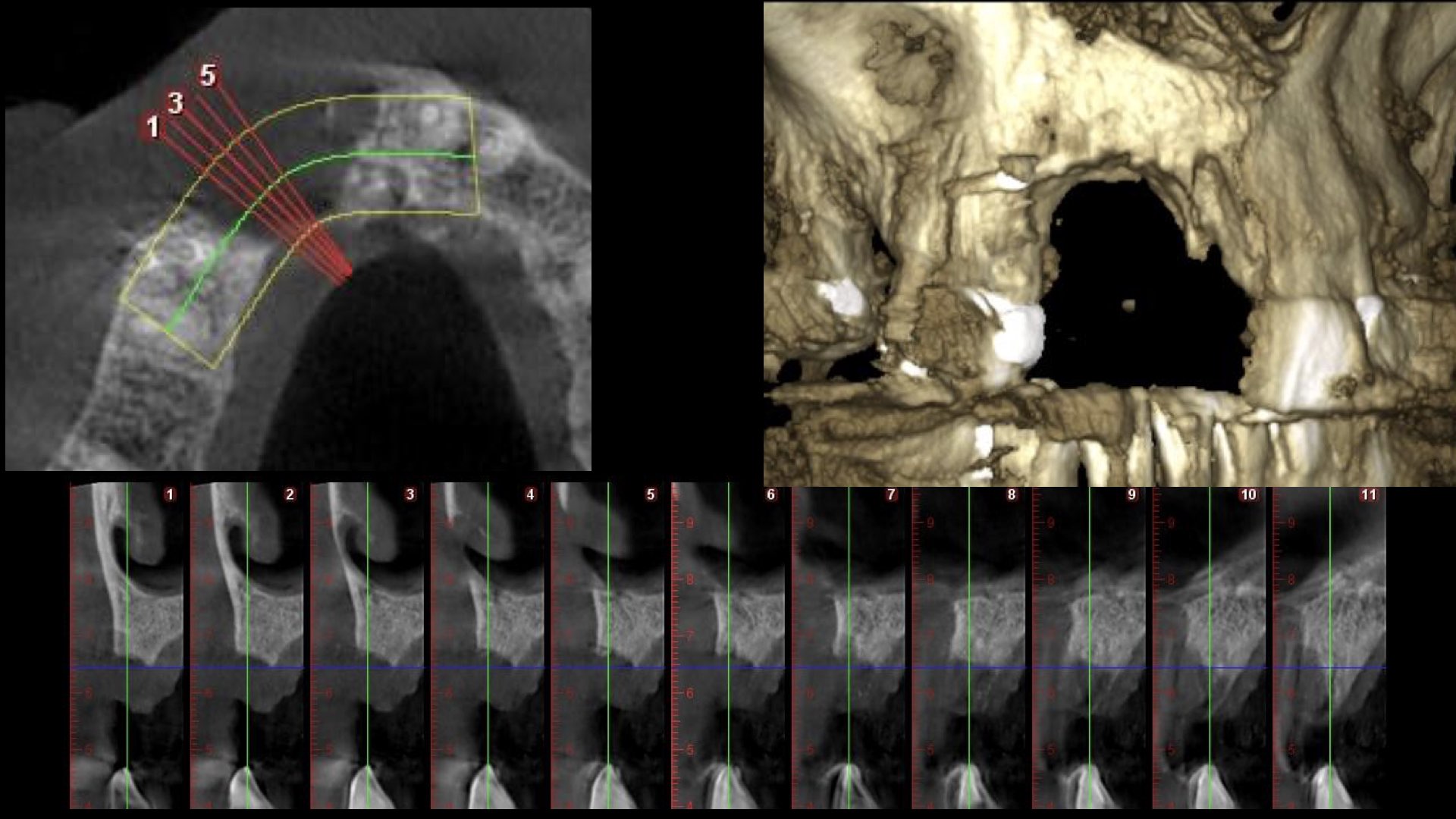
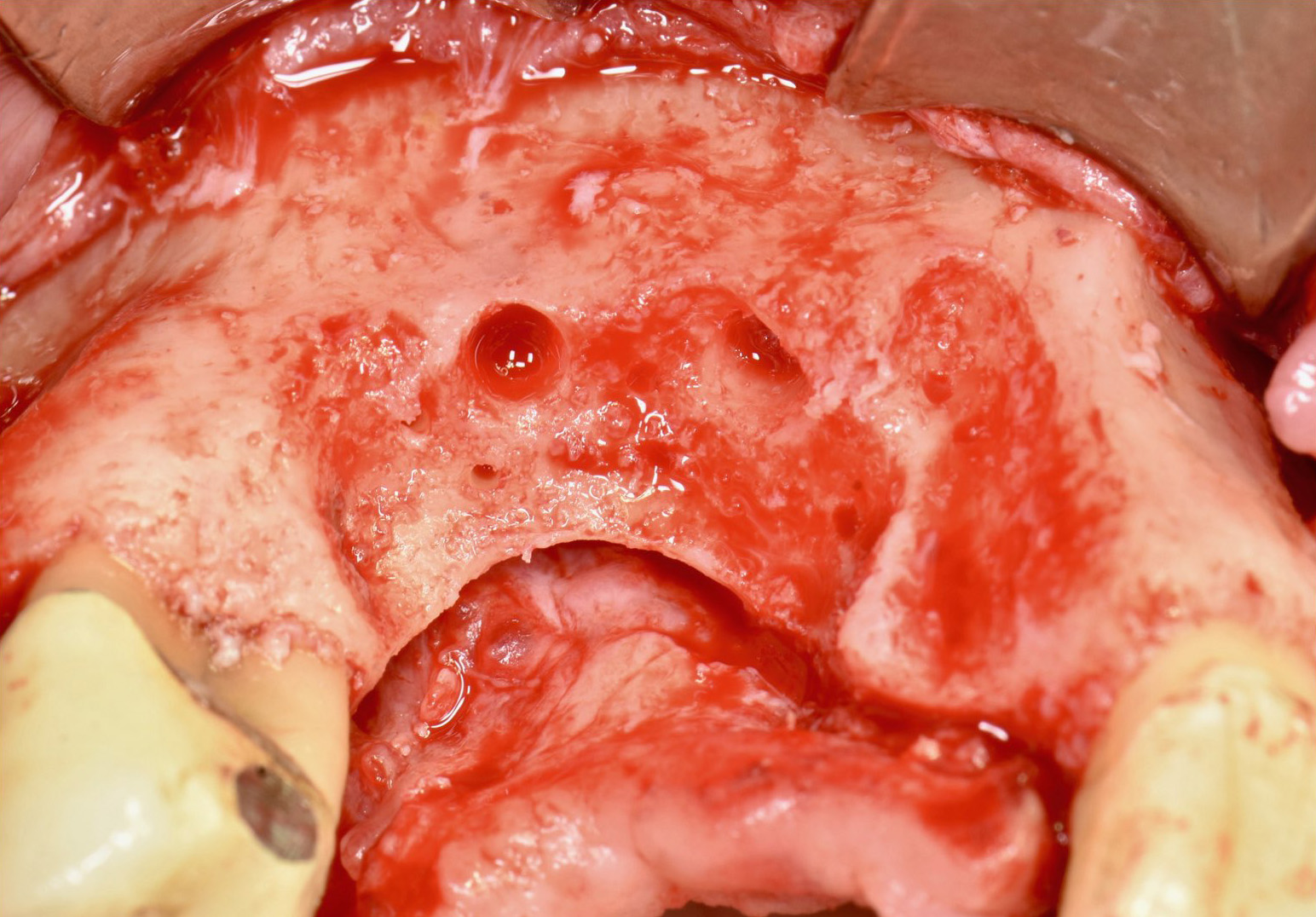
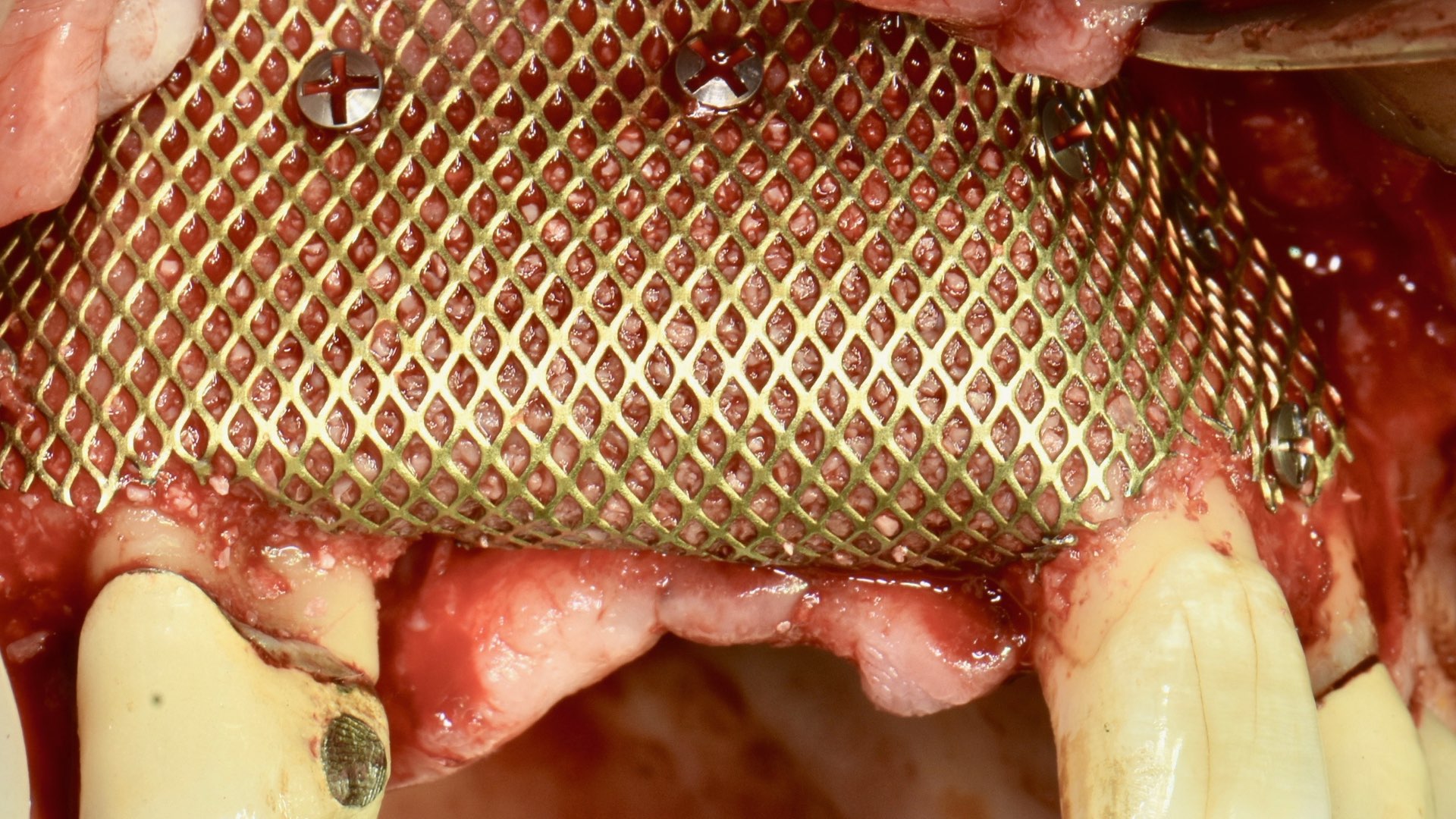
Dans ce cas, encore plusieurs erreurs (Sic !), tout d’abord je n’aurais pas dû garder la 24 présentant une vieille
couronne mal ajustée, elle sera extraite dans un 2ème temps. Comme dans le premier cas, ceci est dû à un compromis que j’ai fait dans un contexte particulier : expliquer au patient qu’il faut déposer des implants, posé 6 ans plus tôt et de surcroît extraire une dent bordant cette perte osseuse…et pourtant j’aurais dû l’imposer. La vie n’est pas si facile mais nous ne devons pas faire de compromis surtout dans ce type de chirurgie, je ne l’ai malheureusement compris que plus tard.
Ensuite, la temporisation fut faite avec une prothèse partielle amovible, erreur magistrale mais en l’ayant évidée et utilisant un matériau d’aménagement tissulaire type Viscogel, je pensais ne pas prendre de risque, la figure 23 nous prouve le contraire.
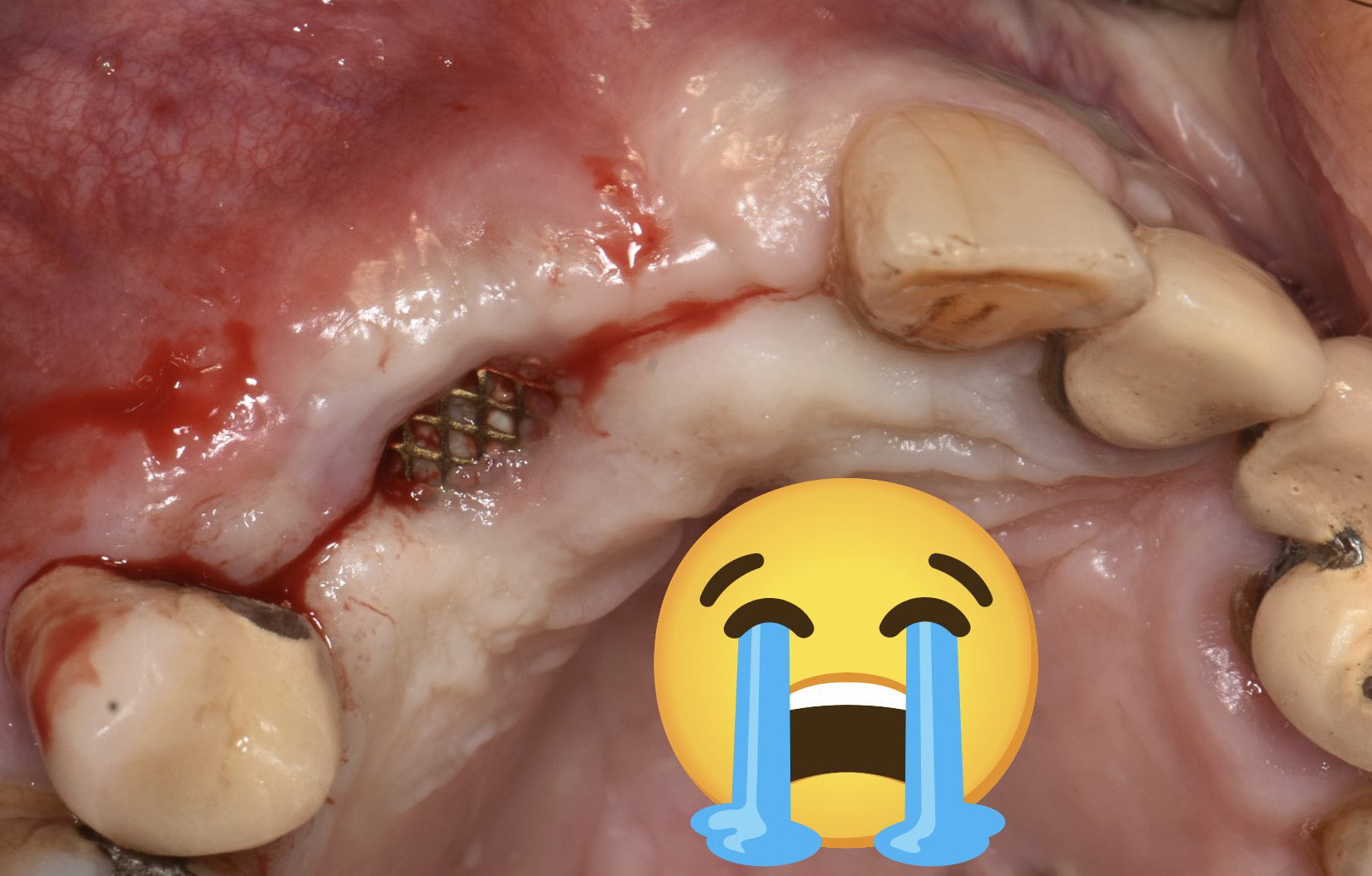
L’utilisation d’une grille titane a un défaut majeur, comme les PTFE perforées mais en pire, en cas d’ouverture du site même sans infection le tissu ostéoide sous-jacent est contaminé immédiatement et même en déposant la grille, nous avons perdu du tissu osseux en regard de l’ouverture. Nous avons réalisé une petite sausage à cet endroit et nous avons quand même pu poser 3 implants après avoir extrait la dent 24 (Fig. 24).
Après un aménagement des tissus mous consistant à une strip technique associée à une greffe de tissu conjonctif pour palier à la position plus apicale de l’implant 12, le résultat reste convenable (Fig. 25 et 26).
CAS CLINIQUE 3
Un dernier cas de défaut antérieur mandibulaire, zone difficile compte tenu des tensions musculaires importantes. Le défaut fut traité par une PTFE non perforée sur le site de 41 42 (Fig. 27).
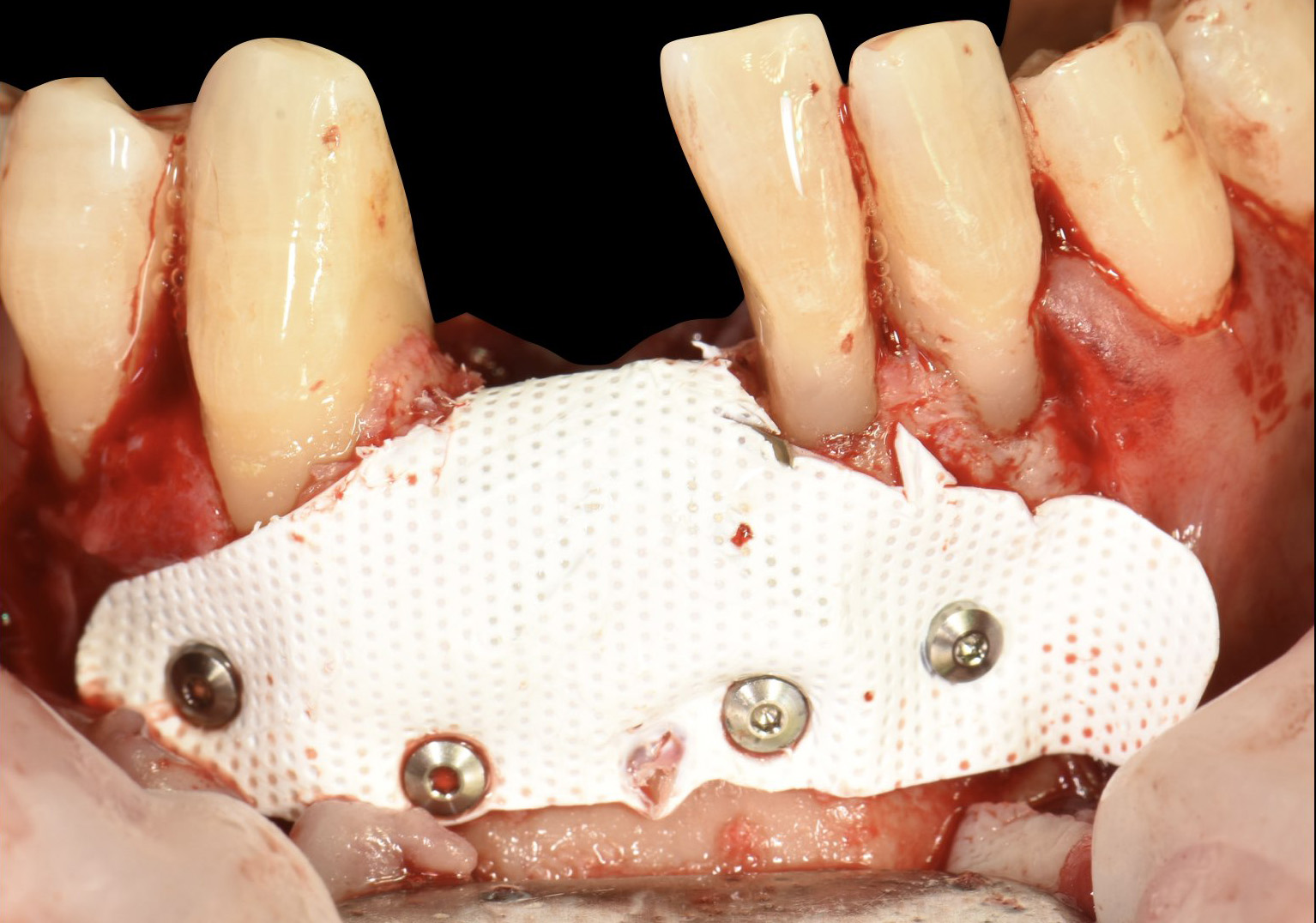
Une première erreur fut de ne pas mettre la membrane à distance de la 43 et ensuite le temps de chirurgie fut bien trop long. Cette erreur je l’ai comprise assez tard mais clairement, une chirurgie de ROG verticale ne doit pas dépasser un temps de 1H15 à 1H30 mn, ici le temps opératoire fut de plus de 2H.
La conséquence fut une ouverture du site assez rapidement et une surinfection du site (Fig. 28). La dépose a été faite immédiatement et le tissu ostéoide nécrosé a été cureté.
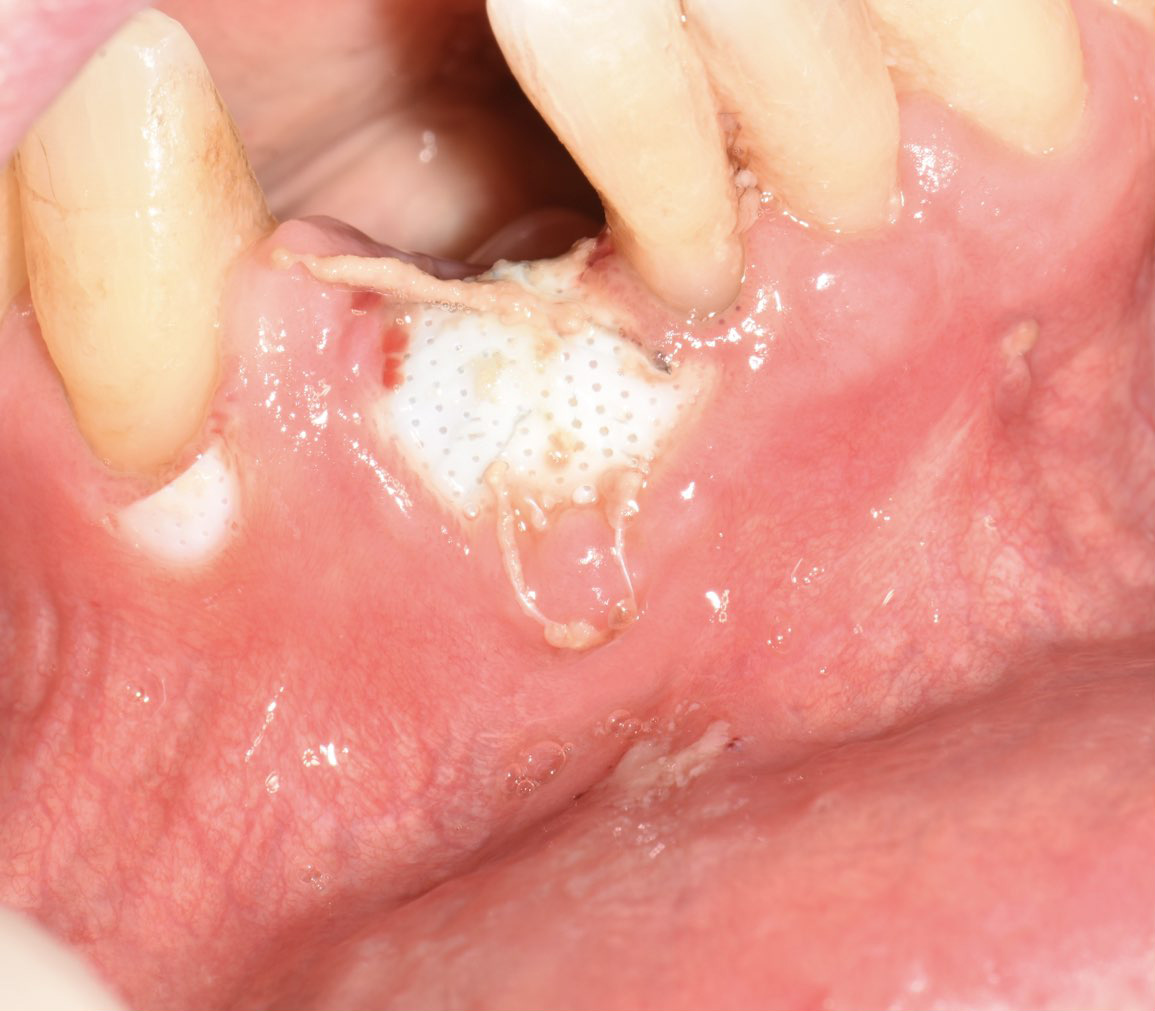
Le gain fut peu important mais nous avons quand même pu poser un implant et transvisser dessus 2 incisives 41/42 (Fig. 29).
L’équipe de Fontana et Simion (Fontana 2011) a élaboré une classification guidant la conduite à tenir en cas de complications.
– CLASSE I
– Exposition de moins de 3 mm sans infection
– Application topique de chlorhexidine, maintenance hebdomadaire avec détartrage local. Dépose de la membrane à 6/8 semaines, mise en place d’une membrane collagénique et fermeture en première intention
– CLASSE II
– Exposition de plus de 3 mm sans infection
– Même prise en charge que classe 1 en essayant de garder la membrane exposée jusqu’à 6/8 semaines.
– CLASSE III
– Exposition associée à une infection aiguë (pus et/ou oedème et/ou douleurs)
– CLASSE IV
– Infection aiguë sans exposition.
Les classes III et IV sont traitées par une dépose immédiate de la membrane, curetage de l’infection, et
antibiothérapie générale.
CONCLUSION
Ces erreurs peuvent paraitre évidentes et elles le sont mais il ne faut jamais oublier que sur les premiers cas, le stress per opératoire peut faire perdre certains repères et nous amener à faire des erreurs qui, dans ce type de chirurgie, seront clairement la cause d’échec partiel ou total.
L’utilisation d’une checklist en per opératoire peut être intéressante pour n’omettre aucun détail, chronométrer son temps de chirurgie et demander à notre assistante de nous informer sur l’avancée de la chirurgie, prendre des photos même si clairement cela rend la chirurgie plus difficile, cela vous permet de revoir le fil de l’intervention et mettre à jour les erreurs commises.
BIBLIOGRAPHIE
1 – Zero Bone Loss Concepts 1st Edition by Tomas Linkevicius (Author), Ph.D. Puisys, Algirdas (Contributor), Rolandas Andrijauskas (Contributor)
2 – Murray G, Holden R, Roachlau W. Experimental and clinical study of new growth of bone in a cavity. Ann J Surg 1957 95: 385-387
3 – Dahlin C, Linde A, Gottlow J, Nyman S. Healing of bone defects by guided tissue regeneration. Plast Reconstr Surg 1988;81: 672-6.
4 – Dahlin C., Lindhe A., Sennerby L., Lekholm U., Nyman S., Generation of new bone around titanium implants using a membrane technique: an experimental study in rabbits. Int. J. Oral Maxillofac. Implants. 1988 ; 4 : 19-25
5 – Buser,D., Dula,K., Belser,U.C., Hirt,H.P. end Berthold,H. (1990). Localized ridge augmentation using guided bone regeneration.I. Surgical procedure in the mandibule. International Journal of Periodontics and Restorative Dentistry 15, 10-29
6 – Fugazzotto Paul A. Régénération Osseuse Guidée avec matrice osseuse bovine et membranes résorbables et non résorbables.PDR 2003, N°6; Vol 23. 599:605
7 – Simion M, Trisi P, Piattelli A : Vertical ridge augmentation using a membrane technique associated with osseointegrated implants.Int J Periodontics Restorative Dent 1994;14:496–511.
8 – Tinti C, Parma-Benfenati S, Polizzi G. Vertical ridge augmentation: what is the limit? Int J Periodontics Restorative Dent. 1996; 16:220–229.
9 – Simion M., Jovanovic S.A., Tinti, C. & Benfenati, S.P. (2001). Long-term evaluation of osseoinegrated implants inserted at the time or after vertical ridge augmentation. A retrospective study on 123 implants with 1-5 years follow-up. Clinical Oral Implants Res 12, 35-45.
10 – Urban IA, Jovanovic SA, Lozada JL. Vertical ridge augmentation using guided bone regeneration (GBR) in three clinical scenarios prior to implant placement: a retrospective study of 35 patients 12 to 72 months after loading. Int J Oral Maxillofac Implants. 2009 May-Jun;24(3):502-10.
11 : Urban IA, Lozada JL, Jovanovic SA, Nagursky H, Nagy K. Vertical ridge augmentation with titanium-reinforced dense-PTFE membranes and a combination of particulated autogenous bone and anorganic bovine bone-derived mineral: a prospective case series in 19 patients. Int J Oral Maxillofac Implants 2014;29:185-193.
12 : Buser D, Ingimarsson S, Dula K, Lussi A, Hirt HP, Belser UC. Long-term stability of osseointegrated implants in augmented bone: a 5-year prospective study in partially edentulous patients. Int J Periodontics Restorative Dent 2022;22:109-117.
13 : Effect of Different Membranes on Vertical Bone Regeneration: A Systematic Review and Network Meta-Analysis. Zhang M, Zhou Z, Yun J, Liu R, Li J, Chen Y, Cai H, Jiang HB, Lee ES, Han J, Sun Y. Biomed Res Int. 2022 Jul 14;2022:7742687.
14 : Antoun H, Abillama F, Daher F. Site de prélèvements osseux et reconstructions alvéolaires pré-implantaires. Implant 2000;66(4):257-368
15 : Milinkovic I., & Cordaro L. (2014) : Are there specific indications for the different alveolar bone augmentation procedures for implant placement? A systematic review. International Journal of Oral and Maxillofacial Surgery, 43(5), 606–625.