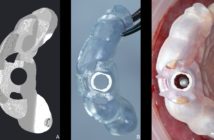
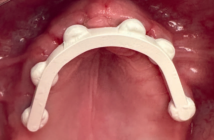
Si les étapes de pré-désinfection et de nettoyage sont facilement identifiées dans l’ensemble des étapes de la stérilisation, les moyens de les mettre en oeuvre ne sont pas toujours bien décrits. Rappelons que l’ensemble de la chaîne de stérilisation et soumise à une obligation de résultat, et qu’il peut alors exister plusieurs outils de nettoyage par exemple pour parvenir à un nettoyage optimal. Ces étapes sont néanmoins incontournables pour garantir la sécurité et l’efficacité des pratiques : d’une part lors des manipulations, et d’autre part en termes d’efficacité car on ne stérilise bien que ce qui est propre.
Mots-clés : ultra-sons, laveur-désinfecteur, porte-instrument dynamique, bac de prédésinfection
La pré-désinfection et le nettoyage ont tous deux des objectifs communs : majorer la sécurité des pratiques lors des manipulations d’instruments inhérentes à la chaîne d’asepsie, et faciliter l’atteinte de l’état stérile comme défini par la norme NF EN 556-1[1].
La pré-désinfection
C’est la seule étape de la chaîne de stérilisation dont on peut se passer, à la seule condition que les instruments soient pris en charge immédiatement en laveurdésinfecteur, sans manipulation supplémentaire. Dans tous les autres cas, la pré-désinfection doit être mise en oeuvre. Concernant les bacs de pré-désinfection, aucune norme ne s’y réfère. aussi, il existe une liberté de choix dans le bac, qui peut être guidée par des considérations pratiques : parmi celles-ci, le bac peut être double afin d’avoir une partie suffisamment large pour les cassettes d’instruments et une partie plus petite pour la petite instrumentation ; il peut être muni d’un panier à mailles facilitant l’égouttage ; il peut être muni d’un système de vidange ; il peut être facilement transportable sur un chariot à roulettes ; il peut être conçu en un matériau compatible avec le passage en laveur-désinfecteur[2,3]. dans tous les cas, il devra être placé au plus près du soin pour éviter toute manipulation supplémentaire. Concernant la solution utilisée pour la pré-désinfection, certaines normes sont à respecter. ainsi, ces produits doivent présenter des normes de bactéricidie (NF EN 13727+a2 / NF EN14561)[4,5] également en présence de substances interférentes (NF t 72170 ou 171), et des
normes de fongicidie (NF EN 13624 / NF EN 14562)[6,7]. D’autres paramètres pratiques pourront participer au choix de l’utilisateur, tels que la facilité de dilution ou le temps d’action par exemple[3]. Concernant le renouvellement du bain ainsi que la durée de trempage, il convient de respecter rigoureusement les instructions d’utilisation du produit données par le fabricant, qui ont été validées par les tests de conformité aux normes d’application affichées [3,8]. Un rinçage à l’eau claire devra suivre la phase de pré désinfection, et précéder la phase de nettoyage.
Le nettoyage
De manière générale, le nettoyage peut se faire manuellement, de façon automatisée, ou en combinant les deux méthodes. Certaines souillures incrustées (ciments de scellement par exemple) ne permettent pas un passage efficace en laveur automatique sans avoir décroché les salissures manuellement auparavant. afin de faciliter cette étape, un traitement dans un bac à ultra-sons (par phénomène de cavitation) peut être intéressant, en gardant en tête que ce procédé n’est qu’une aide au nettoyage et qu’il ne peut s’y substituer totalement [9]. Il est important de rappeler aussi que le traitement aux ultra-sons est inadapté et inefficace pour les instruments en plastique qui vont absorber l’énergie des ultra-sons et inhiber le phénomène de cavitation. L’opérateur pourra porter son choix vers une cuve à ultra-sons aux dimensions adaptées à ses instruments et/ou cassettes ainsi qu’à l’espace de travail dont il dispose, avec de préférence un système de vidange intégré et un minuteur à arrêt automatique. La cuve devrait pouvoir offrir une fréquence idéalement située entre 35 et 45kHz ainsi qu’une fonction chauffage, car la cavitation est optimale entre 45° et 55° [10]. Des tests permettant de s’assurer de l’efficacité de sa cuve à ultrasons existent, tels que le Sonocheck©, le Procyon©, ou encore le Wash-check uS© par exemple[3].
- Le nettoyage manuel
Le nettoyage manuel peut tout à fait permettre d’atteindre un état de propreté compatible au passage en autoclave. S’il présente certains avantages comme le contrôle ponctuel facilité des salissures incrustées, il présente toutefois de plus nombreux inconvénients, tels que le manque de reproductibilité, la perte de temps qu’il représente, des problèmes de gestion des processus et de contrôle de qualité quand la masse d’instruments à traiter s’accroît, ce qui peut faciliter un risque de contamination pour l’opérateur. de plus, un rinçage et un séchage manuels seront effectués, ce qui accroît le temps de traitement. Le nettoyage automatisé devrait être préféré.
Si toutefois l’opérateur choisit un nettoyage manuel, il pourra porter son choix sur l’utilisation d’un produit à usage multiple, à savoir un produit qui sera utilisable tant pour la pré-désinfection, pour le nettoyage manuel, que pour le traitement en cuve à ultra-sons. Ceci participera à réduire les risques de mésusage des produits au cabinet dentaire, à la condition qu’ils respectent les normes de bactéricidie et de fongicidie demandées, décrites plus haut[3]. Il est recommandé de procéder au nettoyage manuel en étant muni de gants en caoutchouc épais, et d’équipements de protection individuelle comme des lunettes de protection et un masque [11].
- Le nettoyage automatisé
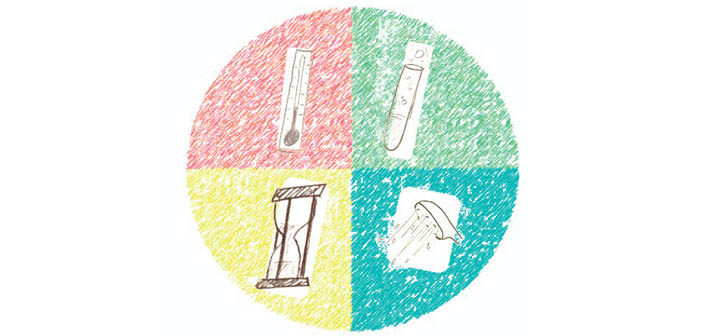
Il permet un gain de temps en offrant du temps masqué à l’opérateur, une standardisation et une reproductibilité des résultats, et une baisse de risques liés à la manipulation. de plus, l’efficacité du nettoyage qui est offert est souvent bien meilleure, car le nettoyage automatisé permet plus facilement le respect des paramètres du cercle de Sinner, garants d’un nettoyage efficace : action chimique, action thermique, action mécanique, temps d’action[12] (fig. 1).
Un thermolaveur n’assurera que les fonctions de nettoyage, voire de séchage, mais n’aura pas d’action désinfectante et ne permettra donc pas de se soustraire à l’étape de pré-désinfection en cas de traitement immédiat des instruments dès la fin du soin, sans manipulation supplémentaire, contrairement à un laveur-désinfecteur [13]. Ce dernier assurera le nettoyage, la désinfection et le séchage grâce à des cycles spécifiques alliant température et temps de traitement. Il est recommandé de se tourner vers ce type d’appareil afin de permettre un traitement efficace des dispositifs médicaux, et de garantir une désinfection de haut niveau pour les dispositifs médicaux thermosensibles ne supportant pas une montée en température jusqu’à 134°C. Le laveur-désinfecteur doit respecter la norme NF EN ISO 15883[14] et être accompagné d’un contrat de maintenance. Il est préférable de s’assurer que ce contrat contienne les qualifications opérationnelles (QO), les qualifications des performances (QP) initiales ainsi que les éventuelles requalifications périodiques nécessaires dès lors qu’un paramètre pourrait être amené à modifier les performances de l’appareil. La Société Française des Sciences de la Stérilisation (SF2S) recommande une requalification annuelle [15]. La mise à disposition d’un système de contrôle de cycle et de traçabilité est fortement recommandée. Quelle que soit la méthode employée, l’état de propreté, la corrosion et le fonctionnement de chaque instrument doivent être
visuellement contrôlés, et ce systématiquement avant le conditionnement [3,9,11]. Si les étapes de rinçage et de séchage ne sont pas assurées par le traitement automatisé, elles devront impérativement être réalisées manuellement.
Nettoyage des porte-instruments dynamiques (PID)
L’utilisation des PId en bouche ainsi que le phénomène de « backflow » qui se produit lors de l’arrêt de leur fonctionnement entraîne inévitablement des salissures externes et internes et une rétro-contamination [16,19].
L’architecture interne complexe des PId rend leur nettoyage difficile, alors même qu’il est nécessaire à permettre une stérilisation efficace[11,18,20]. Leur traitement par trempage dans une solution désinfectante n’est pas recommandé à cause de risques de corrosions[19,21] et parce que des bulles d’air dans les lumières internes des PId pourraient réduire l’activité des désinfectants [22]. Aussi, leur traitement est recommandé sans délai dans des automates assurant le nettoyage externe et interne, voire la désinfection des PId, et à ce titre, respectant la norme NF EN ISO 15883, qui précise dans sa partie NF EN ISO 15883-2 que les PId devraient être mis en rotation interne lors de leur traitement
afin de fournir un nettoyage complet et efficace[14,16,19]. Il est recommandé pour des raisons d’ergonomie que ces appareils assurent également la lubrification contrôlée et le séchage des PID selon des paramètres réglés par le fabricant. En effet, ils éviteront un relargage d’eau ou d’huile pendant la phase obligatoire de stérilisation pouvant compromettre l’intégrité du conditionnement, et donc la bonne réalisation de la stérilisation.
Si le traitement n’est pas effectué immédiatement, il convient de nettoyer/désinfecter extérieurement les PID à l’aide d’une lingette détergente/désinfectant, de les emballer dans une de ces lingettes, et de les déposer dans une boîte fermée hermétiquement [9]. Ceci permettra de maintenir un état humide et d’éviter le séchage des souillures internes avant le traitement en automate, facilitant ainsi leur retrait. Il est clairement admis que le nettoyage manuel des PId n’est pas apte à garantir un nettoyage efficace de ces dispositifs médicaux [16,23]. De la même manière que les laveurs-désinfecteurs non dédiés, ceux dédiés aux PId doivent pouvoir bénéficier de QO, QP et requalifications périodiques, modalités qui devraient être contenues dans un contrat de maintenance. La difficulté d’évaluer le nettoyage proposé par les différents appareils dédiés devrait amener les fabricants à proposer des outils et des solutions simples et reproductibles pour garantir un nettoyage optimal [19].
Bibliographie
- NF EN 556-1. Stérilisation des dispositifs médicaux –Exigences relatives aux dispositifs médicaux en vue d’obtenir l’étiquetage STERILE – Partie 1 : exigences relatives aux dispositifs médicaux stérilisés au stade terminal. Février 2002
- Missika P, Drouhet G, Zeitoun R. Hygiène, asepsie, ergonomie, un défi permanent. Collection JPIO, édition CDP, 2001
- Offner D, Wurtz A, Foresti C, Musset AM. Optimiser sa chaîne de stérilisation selon les recommandations actuelles : des clefs pour relever le défi. La Lettre de Stomatologie 2018, 79:38-46
- NF EN 13727+A2. Antiseptiques et désinfectants chimiques – Essai quantitatif de suspension pour l’évaluation de l’activité bactéricide en médecine – Méthode d’essai et prescriptions (phase 2, étape 1). Décembre 2015
- NF EN 14561. Désinfectants chimiques et antiseptiques – Essai quantitatif de porte germe pour l’évaluation de l’activité bactéricide pour instruments utilisés en médecine humaine – Méthode d’essai et prescriptions (phase 2, étape 2). Mars 2007
- NF EN 13624. Désinfectants chimiques et antiseptiques – Essai quantitatif de suspension pour l’évaluation de l’activité fongicide ou levuricide en médecine – Méthode d’essai et prescriptions (phase 2, étape 1). Novembre 2013
- NF EN 14562. Désinfectants et antiseptiques chimiques – Essai quantitatif de porte germe pour l’évaluation de l’activité fongicide ou levuricide pour instruments utilisés en médecine humaine – Méthode d’essai et prescriptions (phase 2, étape 2). Septembre 2006
- Bagg J, Smith AJ, Hurell D, McHugh S, Irvine G. Pre-sterilisation cleaning of re-usable instruments in general dental practice. Brit dent J 2007, 202:E22
- Association dentaire française (ADF). Grille technique d’évaluation pour la prévention des infections associées aux soins. 2015
- Lambert C, pour l’Association Française de Stérilisation (AFS). Les ultrasons. Thématiques 2014 de l’aFS, 2014. accessible sur : Sf2s-sterilisation.fr/wp-content/uploads/ 2016/08/ultrasons%20-%2026%2009%202014.pdf (consulté le 26.06.2019)
- Direction Générale de la Santé (DGS), Ministère de la Santé. Guide de prévention des infections liées aux soins en chirurgie dentaire et en stomatologie, 2006
- Ade A, Chauchat L, Freve JFO, Gagne S, Caron N, Bussieres JF. Comparison of decontamination efficacy of cleaning solutions on a biological safety cabinet workbench contaminated by cyclophosphamide. Can J Hosp Pharm 2017, 70(6):407-14
- Ministère de l’Emploi et de la Solidarité, Ministère de la Santé. Bonnes pratiques de pharmacie hospitalière. 1ère édition, juin 2001.
- NF EN ISO 15883, parties 1, 2, et 5. Laveurs-désinfecteurs : exigences et essais. 2014, 2009, et 2005
- Société Française des Sciences de la Stérilisation (SF2S). Pratiques – Nettoyage. Accessible sur : Sf2ssterilisation.fr/faq/pratiques/3/ (consulté le 26.06.2019)
- Offner D, Brisset L, Musset AM. Cleaning of dental handpieces : a method to test its efficiency, and its evaluation with a washerdisinfectorlubricator- dryer. Dent Open J 2016;3(1):10e6.
- Smith G, Smith A. Microbial contamination of used dental handpieces. am J Infect Control 2014;42(9):1019e21.
- Winter S, Smith A, Lappin D, McDonagh G, Kirk B. Failure of nonvacuum steam sterilization process for dental handpieces. J Hosp Infect 2017;97:343e7.
- Offner D, Brisset L, Musset AM. Evaluation of the mechanical cleaning efficacy of dental handpieces. J Hosp Infect 2018, in press
- Wilder JA, Roth K. Cleaning of instruments: an absolute requirement for successful reprocessing. Biomed Instrum technol 2012:69e72. Spring Suppl.
- Acosta-Gio E, Bednarsh H, Cuny E, Eklund K, Mills S, Risk D. Sterilization of dental handpieces. am J Infect Control 2017;45:935e8.
- Comident. Guide de traitement des porte-instruments dynamiques avant stérlisation. 2013. accessible sur : www.generiqueinternational.com/docs/ 13_comident_guide_optimise.pdf (consulté le 26.06.2019)
- Zhou x, Huang H, He x, Chen H, Zhou x. Effect of manual cleaning and machine cleaning for dental handpieces. Hua Xi Kou Qiang Yi Xue Za Zhi. 2013; 31(4): 369-371.