La résorption de la corticale vestibulaire après une extraction est un problème majeur dans les secteurs visibles, notamment au maxillaire. De nombreuses techniques de préservation d’alvéole à l’aide de biomatériaux, avec ou sans fermeture conjonctive, ont été décrites dans la littérature.
Avec la présentation d’un cas clinique, nous voudrions revenir sur une technique innovante proposée par le Dr Markus Hürtzeler [5] ayant pour objectif de conserver le volume osseux crestal vestibulaire après extraction.
Même si le recul clinique est encore insuffisant, c’est une voie de réflexion destinée à faire réfléchir les praticiens sur d’éventuelles perspectives futures.
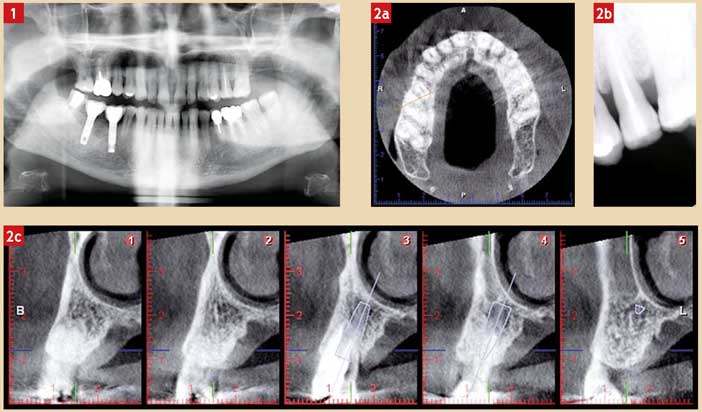
Fig. 1 : radiographie panoramique pré-opératoire Fig. 2 : radiographie rétroalvéolaire et examen cone-beam mettant en évidence la fracture verticale de la dent 25 au niveau du rétrécissement inter-radiculaire
Quel en est le protocole ? Quelles en sont les indications ?
Depuis plusieurs années des protocoles permettant d’obtenir de meilleurs résultats esthétiques pour les implants antérieurs ont été proposés.
La plupart des recherches se sont concentrées sur la préservation tissulaire (osseuse et muqueuse) au moment de l’extraction, de l’implantation et de la mise en esthétique des implants, le but étant de conserver l’architecture et le design des tissus.
Comme l’ont prouvé les travaux d’Araujo et Boticelli [1,2], le seul fait de placer un implant dans une alvéole ne prévient pas la résorption osseuse post-extractionelle.
Même avec le placement immédiat d’un implant, il y a des modifications osseuses et tissulaires qui vont intervenir dans le temps.
Le consensus est qu’une alvéole intacte doit être comblée avec un substitut osseux à résorption lente afin de maîtriser ou de limiter la résorption osseuse [6].
C’est principalement la dimension vestibulolinguale de la crête qui diminue inexorablement les mois qui suivent l’implantation [4].
De plus, chaque alvéole ne va pas réagir de la même manière : les modifications ne seront ni de la même ampleur, ni à la même vitesse selon que le biotype est épais ou fin (Cho, Froum, 2007). En effet, les biotypes fins auront une récession plus grande, que ce soit verticalement ou horizontalement, de l’ordre de 1 mm, contre 0,7 mm pour le biotype épais [4]. L’épaisseur des tissus joue donc un rôle crucial dans leur stabilité.
Enfin, l’épaisseur de la corticale vestibulaire en zone maxillaire antérieure est très fine : comme l’a récemment démontré une étude [6], 97,6 % des incisives et canines maxillaires ont une épaisseur de corticale inférieure à 2 mm.
La cicatrisation des alvéoles d’extraction et les processus de résorption qui se produisent après ont fait l’objet de nombreuses recherches approfondies. Les études cliniques les plus récentes (Araujo, Lindhe, Zuhr, Achermann) ont montré que :
- après une extraction, l’os fasciculé (Bundle-Bone) se résorbe et avec lui, une partie de la corticale vestibulaire (Araujo-Lindhe) ; l’os fasciculé étant intimement lié aux fibres de Sharpey, c’est l’arrachement de celles-ci qui entraîne sa résorption
- l’implantation immédiate ne peut pas prévenir la résorption de l’os fasciculé (Araujo-Lindhe)
- la mise en place d’un substitut osseux ne peut que compenser la perte de la table vestibulaire et préserver le contour de la crête alvéolaire (Zuhr, Hurzeler, Rasperinu)
C’est donc de ce constat qu’une réflexion a été entreprise : aussi surprenant que cela puisse paraître, quand les conditions le permettent, pourquoi extraire la dent dans sa totalité ?
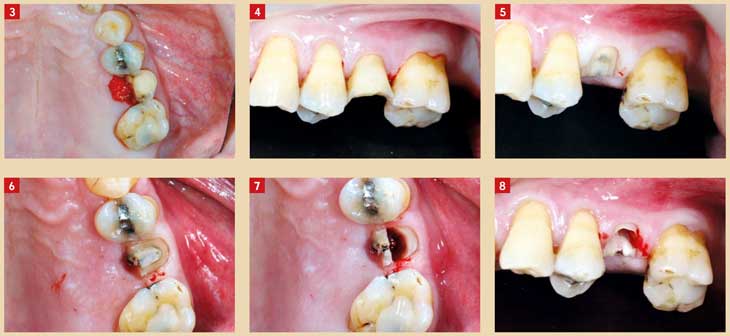
Fig. 3 : traitement initial en urgence ; extraction du fragment palatin, mise en place d’une éponge hémostatique après avoir mis la dent en sous-occlusion Fig. 4 : vue vestibulaire Fig. 5 : traitement implantaire ; meulage du fragment vestibulaire et élaboration d’un congé 1/4 de rond à la fraise légèrement sous-gingival comme pour une taille classique Fig. 6 : vue occlusale Fig. 7 : séparation de la dent en son milieu avec une fraise zékria, en mise en forme de la partie palatine du bouclier Fig. 8 : vue vestibulaire
Quel est le protocole ?
L’idée de l’auteur est de préserver la paroi radiculaire vestibulaire de la racine à extraire et de poser l’implant à son contact, en position palatine ou linguale, après avoir recouvert la racine résiduelle de dérivés de la matrice amélaire.
L’étude histologique à 4 mois chez un beagle dog a permis de valider cette approche puisqu’un néo-cément a pu être observé à l’interface racine-implant, en l’absence de toute réaction inflammatoire.
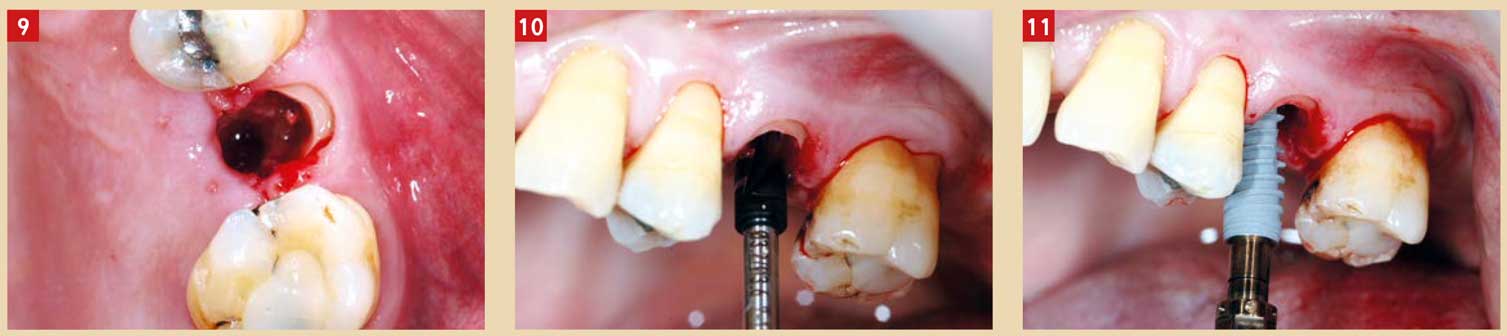
Fig. 9 : retrait du fragment palatin et début de la séquence de forage Fig. 10 : vue vestibulaire foret en place ; le forage doit se faire en palatin du bouclier en l’effleurant légèrement au niveau apical Fig. 11 : mise en place d’un implant NobelActive Rp 4.3*11.5
Quelles sont les indications ?
Les indications et les contre-indications de cette nouvelle approche sont encore à définir. Bien entendu, un examen radiologique par cône beam ou scanner est impératif avant de poser l’indication.
Les 3 indications principales sont :
- les dents ankylosées, comme certaines incisives ayant subi un choc quelques années plus tôt, ou ayant été réimplantées suite à une expulsion
- les dents incluses, comme le plus souvent les canines maxillaires
- les racines résiduelles asymptomatiques enclavées et recouvertes par de l’os
- les dents fêlées ou fracturées, verticalement par exemple, mais sans mobilisation du fragment vestibulaire
Toutes ces dents sont souvent difficiles à extraire et demandent pour cela un délabrement très important, notamment de la corticale vestibulaire, avec souvent la nécessité de reconstruire le site.
En revanche, un délabrement trop important de la dent, une suspicion d’infection, de kyste ou une lésion fibreuse apicale sont des contre-indications à cette technique.
Le net avantage est aussi psychologique car cela rend l’intervention plus simple, tout en soulageant le patient au plus vite. Même en cas d’échec, il est toujours possible de revenir à une technique plus conventionnelle.
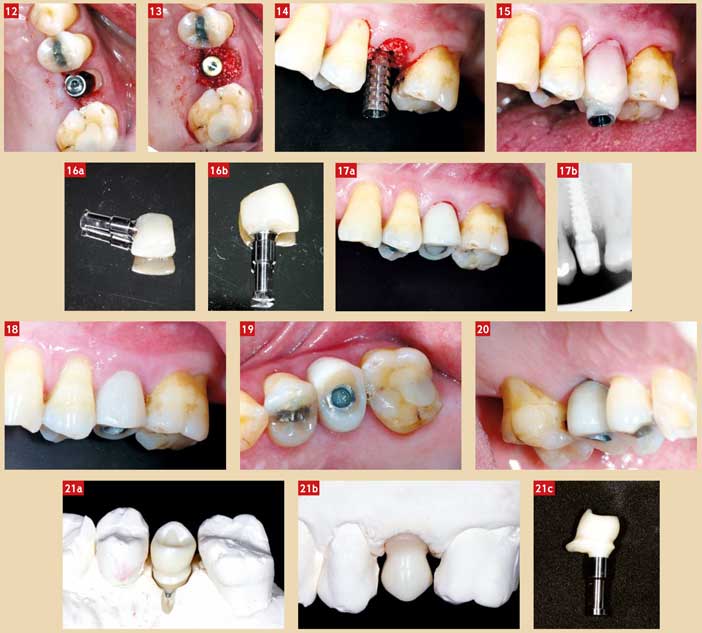
Fig. 12 : vue occlusale implant en place ; l’implant a été placé en vue d’une prothèse vissée, noter le gap entre l’implant et le bouclier Fig. 13 : une vis de cicatrisation étroite est temporairement mise en place et le gap est comblé avec du Bio-Oss après avoir traité l’intrados du bouclier avec de l’Endogain Fig. 14 : un pilier provisoire en titane est connecté à l’implant Fig. 15 : un moule provisoire Ion-3M est perforé et solidarisé au pilier avec de la résine Unifast-GC Fig. 16 : la provisoire est terminée hors bouche ; le profil est concave au niveau de l’implant, et convexe au niveau du congé du bouclier comme une provisoire sur dent naturelle Fig. 17 : couronne provisoire vissée en fin d’intervention et radiographie de contrôle Fig. 18 : résultat à 3 mois, vue vestibulaire ; noter la stabilité verticale des papilles et du collet de la dent Fig. 19 : vue occlusale ; noter la stabilité horizontale de la créte Fig. 20 : vue palatine ; léger affaissement des tissus Fig. 21 : réalisation de l’armature en zircone Procera transvissée ; le design de l’armature est un peu particulier en vestibulaire ; une extension est réalisée pour soutenir la céramique dont la limite se termine comme une couronne sur dent naturelle
Bibliographie
1. Araujo M, Sukekava F, Wennström J, Lindhe J. Ridge alterations following implant placement in fresh extraction sockets: an experimental study in the dog. Journal of Clinical Periodontology. 2005; 32: 645-652.
2. Botticelli D, Berglundh T, Lindhe J. Hard-tissue alterations following immediate placement in extraction sites. Journal of Clinical Periodontology. 2004; 31: 820-828.
3. Davarpanah M, Szmuckler-Moncler S. Unconventional implant treatment. I. Implant placement in contact with ankylosed root fragments. A series of 5 case reports. Clinical Oral Implants Research 2009, 20, 851-856.
4. Evans CD, Chen S. Esthetic outcomes of immediate implant placements. Clinical Oral Implants Research. 2008; 19: 73-80.
5. Markus B. Hürzeler, Otto Zuhr, Peter Schupbach, Stephan F. Rebele, Notis Emmanouilidis, Stefan Fickl, The socket-shield technique: a proof-of-principle report. J Clin Periodontol 2010; 37: 855–862
6. Huynh-Ba G, Pjetursson BE, Sanz M et al. Analysis of the socket bone wall dimensions in the upper maxilla in relation to immediate implant placement. Clin Oral Implants Res. 2010; 21(1): 37-42.
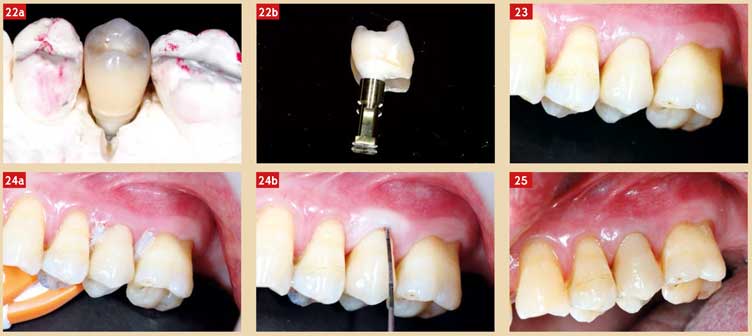
Fig. 22 : montage du cosmétique en céramique Emax (Céramiste Gil Ambrosino – Intégrale Prothèse Avignon) Fig. 24 : vérification des embrasures et des points de contact ; noter la stabilité et la solidité de l’attache épithéliale Fig. 23 : résultat final en bouche à 4 mois Fig. 25 : résultat cilinique à 12 mois





