La fabrication d’éléments par impression 3D répond à certains principes généraux. Tout d’abord, une interface informatique est indispensable, pour modéliser la pièce finale et l’exporter au format « .stl », mais aussi pour diriger l’impression de chaque couche de matériau.
En effet, toutes les technologies d’impression 3D reposent sur le principe de la fabrication additive couche par couche, à partir d’informations issues de l’objet virtuel 3D. Ainsi l’objet est fabriqué par superposition de couches déposées qui vont fusionner entre elles selon des mécanismes propres à chaque technologie.
Même si les méthodes traditionnelles pour moulage ou usinage sont toujours utilisées dans un grand nombre d’applications, les imprimantes 3D trouvent aujourd’hui de nombreuses applications dans l’industrie, dans la vie quotidienne, mais également dans le domaine médical. Ces technologies permettent de fabriquer des objets de formes complexes, de maîtriser l’architecture interne des matériaux et elles permettent souvent d’utiliser moins de matière première que les méthodes traditionnelles.
L’objectif de cet article est de présenter quelles sont les applications de l’impression 3D dans le domaine du vivant, que ce soit pour des applications cliniques en Chirurgie Orale et maxillo-faciale ou bien dans le domaine de la recherche en médecine régénératrice utilisant des techniques d’ingénierie tissulaire.
Impression 3D et chirurgie : applications cliniques
En chirurgie orale et maxillofaciale, l’utilisation de logiciels de planification et de guides chirurgicaux est devenue un outil courant pour les chirurgiens. Les méthodes utilisées dans ce type d’application sont anciennes, il s’agit principalement de la stéréolithographie et de l’extrusion à chaud de fil fondu. Ces deux techniques utilisent des polymères qui peuvent être stérilisés à froid ou à l’aide de rayonnement gamma.
Il peut s’agir de modèles chirurgicaux permettant de planifier les interventions et de préparer le matériel d’ostéosynthèse ou les greffons avant l’intervention [1–3].
Ces modèles peuvent être préparés à l’aide de résines autoclavables, ce qui permet de les utiliser au bloc opératoire dans des conditions stériles. L’utilisation de ces modèles imprimés à partir des données radiologiques du patient (scanner ou cone beam) réduit le temps opératoire, améliore l’ajustage des greffons et devrait permettre d’améliorer les résultats cliniques tout en réduisant la morbidité (Fig. 1).
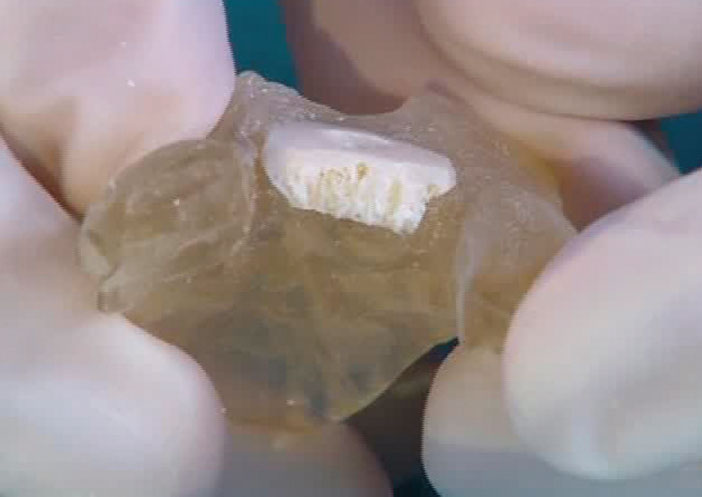
Fig. 1 : modèle en résine imprimé par stéréolithographie à partir du scanner 3D d’un patient. Ce modèle a permis de modeler manuellement un bloc d’allogreffe avant de l’implanter chez le patient (image Dr Laurent VENET, Lyon).
D’autre part, les guides chirurgicaux (guides de forage en implantologie, guides de coupe en chirurgie maxillo-faciale permettent d’améliorer la précision du geste et de réaliser des interventions moins invasives [4]. Il a été démontré que l’utilisation de chirurgie guidée permettait de limiter les suites opératoires [5] et de limiter le recours à certaines procédures d’augmentation tissulaire [6]. Ces guides sont aujourd’hui principalement fabriqués par stéréolithographie (Fig. 2).
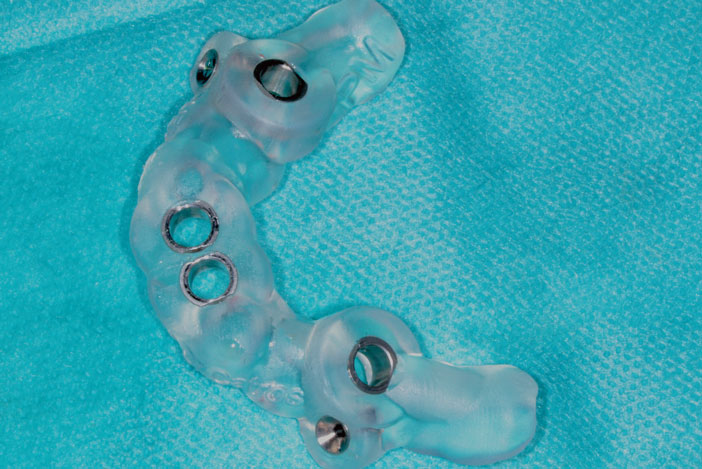
Fig. 2 : guide chirurgical fabriqué par impression 3D (stéréolithographie) pour chirurgie implantaire guidée (Laboratoire Pascal Marseille, Bordeaux).
Depuis quelques années, il est possible de disposer de biomatériaux sur mesure pour réaliser des greffes osseuses en chirurgie implantaire. Ces biomatériaux sont principalement des allogreffes qui sont usinées (fabrication soustractive) à partir d’une planification réalisée sur des images radiologiques. Même s’il existe encore peu d’applications dans ce domaine utilisant des imprimantes 3D, ces nouvelles techniques devraient permettre de fabriquer des formes plus complexes qu’avec une méthode soustractive, tout en contrôlant précisément l’architecture interne de ces greffons. La principale limite actuelle dans ce domaine est le manque de matériau imprimables et biocompatibles validés par les autorités de contrôle pour des applications osseuses chez l’homme [7]. De plus, dans le cas des grandes pertes de substance osseuses maxillaires ou mandibulaires ou chez les patients irradiés, les biomatériaux utilisés seuls ne sont pas efficaces, ce qui justifie les travaux en ingénierie tissulaire.
Ingénierie tissulaire et bio-impression
La Bioimpression (Bio-printing) peut être définie comme la micro-impression d’éléments biologiques, utilisant des imprimantes spécifiques (Bio-Imprimantes) et des matériaux adaptés.
Il existe plusieurs technologies permettant la micro-impression d’éléments biologiques. Le pré-requis de ces méthodes est qu’elles n’altèrent pas la fonction des éléments imprimés, que ce soit la vitalité et les capacités de prolifération et de différentiation des éléments cellulaires ou bien les propriétés biologiques des protéines, hydrogels ou autres biomatériaux imprimés. Ainsi la vérification des propriétés biologiques des structures imprimées après impression est une étape indispensable pour valider un processus de bioimpression.
Comme pour toute imprimante, les méthodes de bioimpression utilisent une encre (bio-ink), contenant les éléments biologiques d’intérêt (cellules, protéines, facteurs de croissance), et un papier (bio-paper) support d’impression, qui peut être une lamelle de verre recouverte d’un gel [8] ou bien une membrane de polymère [9].
La bioimpression par extrusion est la plus simple à mettre en œuvre car elle utilise des systèmes de « pousse-seringue » pour extruder un gel ou une pâte contenant les éléments biologiques. Les volumes imprimés peuvent être importants mais la résolution est plus faible qu’avec les autres méthodes.
Pour maintenir la forme des structures imprimées en 3D, il est nécessaire d’utiliser des systèmes de réticulation des hydrogels imprimés, que ce soit par réticulation chimique (Chlorure de calcium pour l’alginate) ou lumineuse (source UV pour gélatine métacrylée) (Figure 3a).
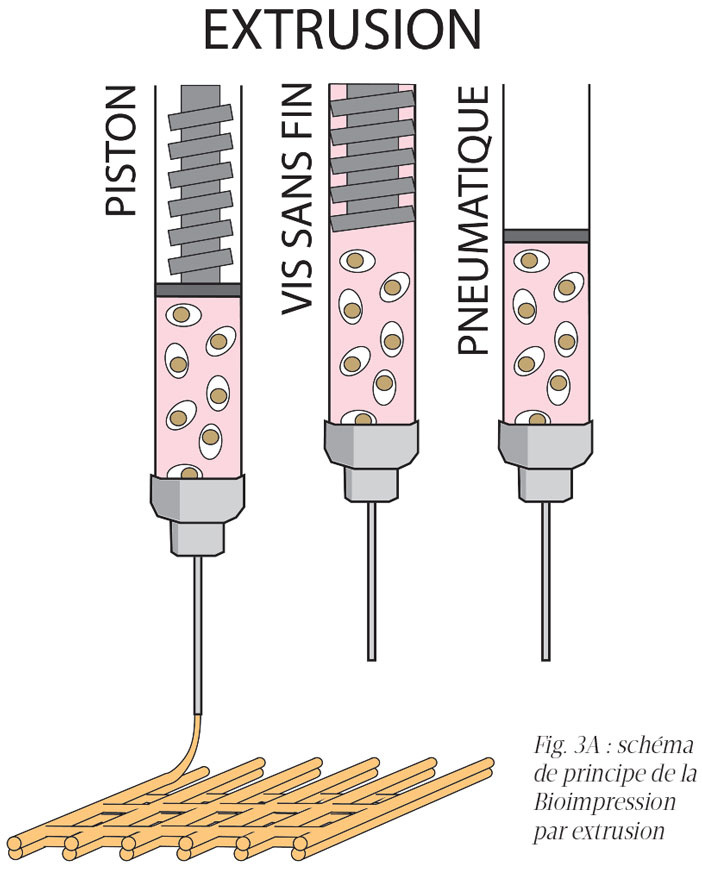
Fig. 3A : schéma de principe de la Bioimpression par extrusion
La bioimpression par jet d’encre (inkjet printing) utilise des têtes d’impression piezzo-électriques ou thermiques, similaires aux imprimantes de bureau. C’est une technique robuste, qui présente cependant la limite de ne pas pouvoir imprimer d’encres cellulaires très concentrées car celles-ci viennent alors boucher les buses d’impression (Figure 3B).
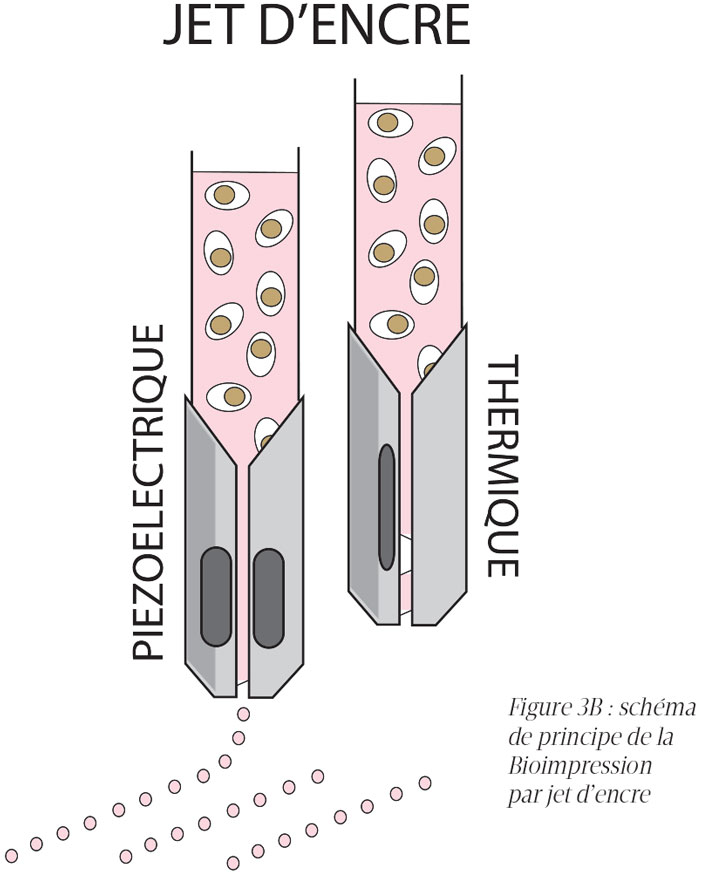
Figure 3B : schéma de principe de la Bioimpression par jet d’encre
La Bioimpression assistée par laser utilise l’énergie d’une source laser focalisée sur une lame de verre recouverte de l’encre pour éjecter des gouttelettes en direction d’un support receveur. Cette technologie de bio-impression est relativement complexe à mettre en œuvre car elle nécessite l’utilisation de sources Laser, mais également car l’environnement (température, hygrométrie…) doit être finement contrôlé pour obtenir des résultats reproductibles. Cependant, c’est la méthode qui permet actuellement d’obtenir la meilleure résolution d’impression avec une densité cellulaire élevée (Figure 3C).
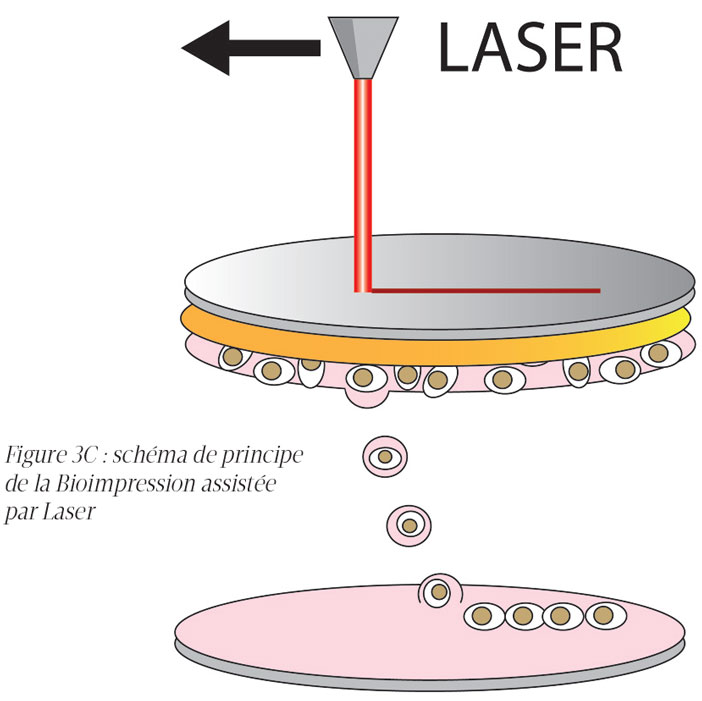
Figure 3C : schéma de principe de la Bioimpression assistée par Laser
Les Bio-imprimantes par jet d’encre et par extrusion existent aujourd’hui sous forme de machines commerciales pour la recherche tandis qu’il n’existe que des prototypes dans des équipes spécialisées pour la bio-impression assistée par laser.
Les méthodes de bioimpression peuvent être utilisées dans tous les champs d’application de l’ingénierie tissulaire. Ainsi, les éléments cellulaires peuvent être organisés finement 2 ou 3 dimensions avec des bioimprimantes afin d’étudier par exemple la communication inter-cellulaire [10]. Par ailleurs, il est possible grâce aux méthodes de bioimpression de créer des « organoïdes », c’est à dire des assemblages cellulaires tridimensionnels reproduisant une fonction biologique: ces structures permettent notamment de tester des molécules thérapeutiques ou de mimer des processus pathologiques [11].
Enfin, la fabrication d’organes par bioimpression (Organ Printing), reste aujourd’hui complètement du domaine de la science fiction, même si c’est une perspective importante dans le domaine de la médecine régénératrice, car cela permettrait de suppléer au manque de donneurs pour les greffes d’organes [12]. Dans cette optique, la bio-impression d’éléments biologiques directement au sein d’un organisme vivant est une perspective intéressante pour comprendre les processus de cicatrisation et mettre en oeuvre de nouveaux procédés thérapeutiques [13].
iNserm U1026 – Bioingénierie Tissulaire (BioTis) ; 146 rue
Léo Saignat ; 33 076 BORDEAUX
UFr d’odontologie de l’Université de Bordeaux, 16-20 cours de la Marne, 33082 Bordeaux cedex
Conclusion
Les bio-imprimantes sont donc de nouveaux outils pour la recherche en ingénierie tissulaire et plus largement dans les domaines de la biologie cellulaire et de la médecine. La plupart de ces méthodes sont aujourd’hui disponibles commercialement.
La micro-impression d’éléments biologiques permet d’organiser précisément les cellules dans leur microenvironnement et ainsi de mieux comprendre certains processus biologiques complexes. L’autre intérêt des ces techniques est de participer à la fabrication d’assemblages tridimensionnels mimant des processus physiologiques afin de servir de plateforme de test de médicaments ou bien de validation de nouveaux biomatériaux. Ceci pourrait permettre de limiter le recours à l’expérimentation animale pour la validation de ces produits.
Bibliographie
1. Cohen a, Laviv a, Berman P, Nashef r, abu-Tair J. Mandibular reconstruction using stereolithographic 3-dimensional printing modeling technology. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2009;108:661–6.
2. Venet L, Perriat m, Jaby P, Fortin T. Intérêt de l’imagerie pour les greffes d’apposition allogéniques par tunnelisation : à propos d’un cas 2015:18–24.
3. Jacotti m, Wang H-L, Fu J-H, Zamboni G, Bernardello F. Ridge augmentation with mineralized block allografts: clinical and histological evaluation of 8 cases treated with the 3-dimensional block technique. Implant Dent 2012;21:444–8.
4. D’haese J, ackhurst J, Wismeijer D, De Bruyn H, Tahmaseb a. Current state of the art of computer-guided implant surgery. Periodontol 2000 2017;73:121–33.
5. Fortin T, Bosson JL, isidori m, Blanchet e. Effect of flapless surgery on pain experienced in implant placement using an image-guided system. Int J Oral Maxillofac Implants 2006;21:298–304.
6. Pommer B, Busenlechner D, Fürhauser r, Watzek G, mailath-Pokorny G, Haas r. Trends in techniques to avoid bone augmentation surgery: Application of short implants, narrowdiameter implants and guided surgery. J Craniomaxillofac Surg 2016;44:1630–4.
7. Desobeau B. Les greffons osseux sur mesure en chirurgie préimplantaire : revue systématique de la littérature. Thèse pour le diplôme d’état en chirurgie dentaire, Bordeaux 2016. n.d. https://dumas.ccsd.cnrs.fr/dumas-01348678v1/tei.
8. Catros s, Guillotin B, Bacáková m, Fricain J-C, Guillemot F. Effect of laser energy, substrate film thickness and bioink viscosity on viability of endothelial cells printed by Laser-Assisted Bioprinting. Appl Surf Sci 2011;257:5142–7.
9. Guduric V, metz C, siadous r, Bareille r, Levato r, engel e, et al. Layer-by-layer bioassembly of cellularized polylactic acid porous membranes for bone tissue engineering. J Mater Sci Mater Med 2017;28:78.
10. Bourget J-m, Kérourédan o, medina m, rémy m, Thébaud NB, Bareille r, et al. Patterning of Endothelial Cells and Mesenchymal Stem Cells by Laser-Assisted Bioprinting to Study Cell Migration. Biomed Res Int 2016;2016:3569843.
11. Horváth L, Umehara Y, Jud C, Blank F, Petri-Fink a, rothenrutishauser B. Engineering an in vitro air-blood barrier by 3D bioprinting. Sci Rep 2015;5:7974.
12. Jung JP, Bhuiyan DB, ogle Bm. Solid organ fabrication: comparison of decellularization to 3D bioprinting. Biomaterials Research
13. Keriquel V, oliveira H, rémy m, Ziane s, Delmond s, rousseau B, et al. In situ printing of mesenchymal stromal cells, by laser-assisted bioprinting, for in vivo bone regeneration applications. Sci Rep 2017;7:1778.




Un commentaire
Intéressant par contre je me demande si on en fait pas un peu trop et qu’il n’y a pas beaucoup de fantasmes avec la bioimpression…