Il ne serait pas pensable d’éditer un numéro spécial sur l’hygiène sans traiter la stérilisation. Deux raisons au moins corroborent cette « obligation » : le risque de transmission de patient à patient, et le contrôle du cabinet.
Rappelons les terribles transmissions de la Clinique du Sport, où plus de 80 personnes ont développé des kystes vertébraux. Les instruments chirurgicaux traités par désinfection finale étaient rincés au lavabo du bloc équipé d’un robinet à filtre bactériologique.
Les instruments furent contaminés par les mycobactéries Xénopi, qui se trouvaient en quantité dans le filtre. Ces bactéries, bien que saprophytes, furent à l’origine de ces infections dont on ignora longtemps l’origine. On estime que 5 % des infections nosocomiales ont pour origine des erreurs dans la chaîne de stérilisation.
En cas de d’accusation d’un patient sur une éventuelle transmission d’une maladie infectieuse contractée au cabinet dentaire, les contrôles, effectués en général par la Drass, porteront en premier sur les procédures de stérilisation.
Bon nombre d’articles ont traité ce sujet et il semble toujours ridicule de le répéter. Il est connu que la « chaîne » de stérilisation comprend plusieurs étapes : traitement préalable : pré désinfection et nettoyage ; conditionnement ; chargement de l’autoclave ; stérilisation. Chaque étape conditionne la suivante. Aussi, proposons-nous d’aborder ce thème en portant notre attention sur les points fondamentaux et les erreurs les plus habituelles.
Traitements initiaux des dispositifs à la stérilisation
L’objectif de la stérilisation est d’obtenir des DM stériles, c’est-à-dire exempts de tout micro-organisme (MO) revivifiable.
Cet objectif est obtenu par l’action de la vapeur d’eau à haute température sur les DM (ex : 134°) : durant un certain temps. Imaginons qu’une goutte de sang se trouve sur le dispositif à stériliser : la vapeur agira sur la partie externe, la croûte de la goutte de sang, mais pas sur l’intérieur de la goutte. Le praticien aura un dispositif contaminant.
Cette vapeur d’eau, en se déposant sur les objets, hydrolyse les MO d’une valeur de 106 au minimum. Si notre instrument supporte à un endroit un nombre de MO qui est supérieur au pouvoir stérilisant de la vapeur, il restera contaminant.
Conclusion : Sans une excellente préparation des DM, la stérilisation n’est pas efficace.
Comment éliminer les souillures et réduire le nombre de MO ? L’action du détergent et du désinfectant
Produit de détergence
Il n’est pas normé. Les produits détergents (savons) décollent les souillures et les micro organismes des dispositifs médicaux placés dans la solution. La détergence est plus efficace lorsque la solution contient des enzymes protéolytiques
Pratique :
- Vérifier la présence d’enzymes sur l’étiquette
- Vérifier l’action du produit :
- Aspirer du sang avec une pompe à salive ;
- Laisser sécher ;
- Mettre la pompe dans le bain de pré désinfection ;
- Laisser une heure ;
- Secouer deux fois le bac délicatement. Il ne doit plus rester de trace de sang dans la pompe, ni sur le fond du bac ( Fig. 1 et 2 ou Fig. 1-2-3-4).
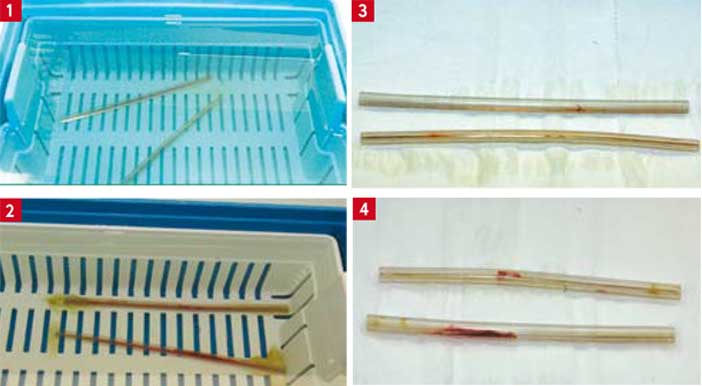
Fig. 1 : Pré désinfection satisfaisante Fig. 2 : Changez de produit Fig. 3 : Résultat de pré désinfection correct Fig. 4 : Produit inefficace
Optimiser l’action détergente
Il est préférable que le sang situé sur le DM n’ait pas eu le temps de sécher quand ceux-ci sont immergés dans le bac.
Pratique :
- Les instruments sont mis dans le bac immédiatement après traitement (premier acte de l’assistante) ;
- Le bac est situé dans la salle de soins ;
- Les DM sont totalement immergés ;
- Ils demeurent dans le bain plus d’un quart d’heure.
Ne pas hésiter à les laisser plus d’une heure.
Produit de désinfection
Un produit normé assurant son efficacité : les MO décollées des DM, baignent dans la solution. Leur nombre va être réduit d’environ de 104 à 105. Pour cela, ce bain doit être propre; il est donc renouvelé au minimum tous les jours.
Pratique :
- Aucune trace de sang ne demeure sur les DM après immersion ;
- Un bain trouble doit être changé ;
- un bain neuf après chaque chirurgie.
Comment optimiser cette action : un nettoyage performant
Le nettoyage manuel
Ce mode de nettoyage, applicable lorsque cinq ou six patients sont traités dans la journée, est déconseillé :
- Risque de pollution de l’environnement ;
- Risques accrus d’accident d’exposition au sang (AES) ;
Pratique :
- Il dépend de la formation de l’assistante ;
- Onéreux pour un cabinet traitant plus de huits patients par jour.
Le nettoyage aux ultrasons
La qualité de nettoyage est mise en doute par la pharmacie centrale des Hôpitaux de Paris et la direction générale de la Santé ; des études sont en cours. La fréquence des ultrasons est comprise entre 25 et 50 hertz.
Ce nettoyage est très utile pour les fraises, les instruments creux.
Pratique :
- Ne pas superposer plus de deux couches de DM ;
- Même solution que le pré désinfectant pour ne pas rincer les DM avant l’immersion dans les ultrasons ;
- Comme pour tous moyens de nettoyage, la solution est changée à chaque traitement.
Le thermo laveur (machine à laver du commerce)
Utiliser un cycle débutant à faible température et terminant à la température la plus élevée. Elle est intéressante pour un cabinet de groupe ou traitant de nombreux patients.
Pratique :
Préférer un thermo laveur avec séchage turbo pour obtenir des DM parfaitement secs.
Le thermo désinfecteur normé (Pr ENISO 15883-1 et 2) (Fig. 5)
Le moyen de nettoyage le plus efficace actuellement, qui permet la traçabilité. Le séchage est efficient avec un filtre à air. Il comprend un cycle de nettoyage des parties internes des instruments dynamiques.
Pratique :
- Pour que les procédures de traitement des IR soit correcte ( le thermo désinfecteur ne faisant que nettoyer les parties internes des instruments dynamiques), le protocole doit inclure l’immersion dans le bain de pré désinfection.
- Attention, son prix est élevé.
Double moyen : Ultrason puis thermo laveur
Un double moyen très efficace si la salle de stérilisation n’est pas équipée d’un thermo désinfecteur.
Pratique :
Un moyen vivement conseillé pour le nettoyage des DM chirurgicaux, les fraises, les instruments creux.
Comment obtenir une surface réceptrice à la vapeur ?
Nous avons vu que les micro-organismes sont tués par la vapeur d’eau saturée à température élevée. Une surface mouillée contaminée, traitée par de la vapeur saturée, deviendra une surface mouillée contenant des MO chauds et vivants. Le séchage des DM est une opération essentielle.
Ce séchage est obtenu facilement en thermo désinfecteur, en thermo laveur turbo, à l’aide d’envoi d’air chaud dans une enceinte spécifique ou encore par l’essuyage manuel, consciencieux, à l’aide de non-tissé.
Pratique :
Il n’est pas conseillé de laisser les DM sécher à l’air libre.
Est-il impératif d’emballer tous les instruments ?
Les instruments de pratique quotidienne ?
L’analyse à l’aide d’un appareil de mesure au laser, révèle un taux d’aéro-contamination très bas dans des tiroirs propres et désinfectés. La contamination aérienne des instruments placés dans ces tiroirs, durant une journée, est plus faible qu’en salle, et les MO peu pathogènes (Fig. 6 et 7).
La question de l’emballage des instruments stérilisés de fraîche date, utilisés pour une pratique quotidienne peu invasive, peut se pose en chirurgie dentaire, et cela a été abordé par des membres d’associations scientifiques éminents. Les instruments d’examen, d’endodontie, de prothèse etc., utilisés le jour ou le lendemain de leur stérilisation, retirés du tiroir par le praticien ou son assistante dont les mains sont traitées selon un protocole reconnu, et placés dans un plateau jetable, ne paraît effectivement pas une faute d’asepsie.
Remarques
- Les instruments qui demeurent plus longtemps dans les tiroirs seront à nouveaux stérilisés, les procédures précédant la stérilisation n’étant pas nécessaires dans ce cas.
- Les instruments unitaires non emballés, conditionnés dans le stérilisateur, sont placés en une couche sur le plateau perforé, de préférence, isolés les uns des autres.
- Les instruments conditionnés dans des cassettes pour une pratique plus ergonomique des traitements dentaires, doivent être emballés.
- Actuellement, des supports de sachets d’instruments d’examen sont très performants et permettent de stériliser 18 sachets par cycle de stérilisation.
- Il ne faut pas sous-estimer l’impact de qualité de l’ouverture des sachets devant les patients.
Les instruments de chirurgie
Certains praticiens équipent la table d’instrumentation chirurgicale directement à la sortie du stérilisateur, instruments non emballés. Or, il arrive fréquemment que des complications ou des modifications de l’intervention nécessitent un instrument imprévu pour obtenir le résultat escompté (pince à suture, fraises spécifiques, pinces gouge, condenseur osseux…). C’est pourquoi, tout instrument ou groupe d’instruments nécessaires pour une intervention chirurgicale ou non chirurgicale indéterminée dans le temps (cassettes séquencées pour des traitements spécifiques), sont impérativement stérilisés emballés, la date de péremption notée.
Pratique :
- Soudure continue de 8 mm d’épaisseur ;
- Emballer rapidement après le nettoyage.
Éviter les multiples erreurs de stérilisation
20 % des stérilisations sont inefficaces. La stérilisation requiert du temps, de l’énergie, de la formation. Si l’on suit toutes les procédures, autant obtenir le résultat escompté !
Le choix du stérilisateur
En chirurgie dentaire, le choix du stérilisateur se portera toujours sur les stérilisateurs à vapeur d’eau de type B, répondant à la norme 13060. La norme NF EN 554 définie le mode de réception et les moyen d’assurer de la qualité de l’appareil fourni (qualification opérationnelle, l’article sur la traçabilité fournit des informations sur ces normes et les contrôles de stérilisation).

Fig. 5 : Thermodésinfecteur Fig. 6 : Contamination aérienne en salle Fig. 7 : Contamination aérienne dans un tiroir Fig. 8 : Test de Bowie Dick’
Surveiller la pénétration de la vapeur
Elle doit être sous forme de vapeur saturée : trop saturée, il y a formation de gouttelettes, la vapeur est humide, de l’eau se dépose sur les DM, l’action n’est plus stérilisante ; insuffisamment saturée, le stérilisateur s’apparentant à un « Poupinel » à faible température. Il devient inefficace. Comment connaître la qualité de la vapeur, le test de Bowie Dick (Fig. 8) :
C’est actuellement le test le plus reconnu. Il informe sur l’évacuation de l’air du stérilisateur (qualité du vide) et sur la capacité de la vapeur à atteindre toutes les surfaces des dispositifs. Il est recommandé de le pratiquer chaque matin, ou plus exactement chaque fois que le stérilisateur est rallumé, le stérilisateur étant déjà chaud. Le coût de ce test est de 6 euros (moyenne sur 8 produits proposés) ce qui équivaut au coût de l’amortissement d’un stérilisateur en 6 ans, c’est dire que ce contrôle est très onéreux. Peu de cabinets suivent ces recommandations. Actuellement, la DGS admet un test de Bowie Dick tous les 8 à 10 cycles.
Pratique :
- Faire le test de Bowie Dick lorsque vous stérilisez les dispositifs médicaux de chirurgie ;
- Conserver les dispositifs chirurgicaux pour les stériliser dans la même journée ;
- Faire un test Hélix (Fig. 9), représentant la forme la plus complexe des corps creux, les autres fois. Ce test, proposé pour remplacer le Bowie Dick, est certes moins performant, mais donne une indication tout à fait intéressante. Il est peu onéreux.
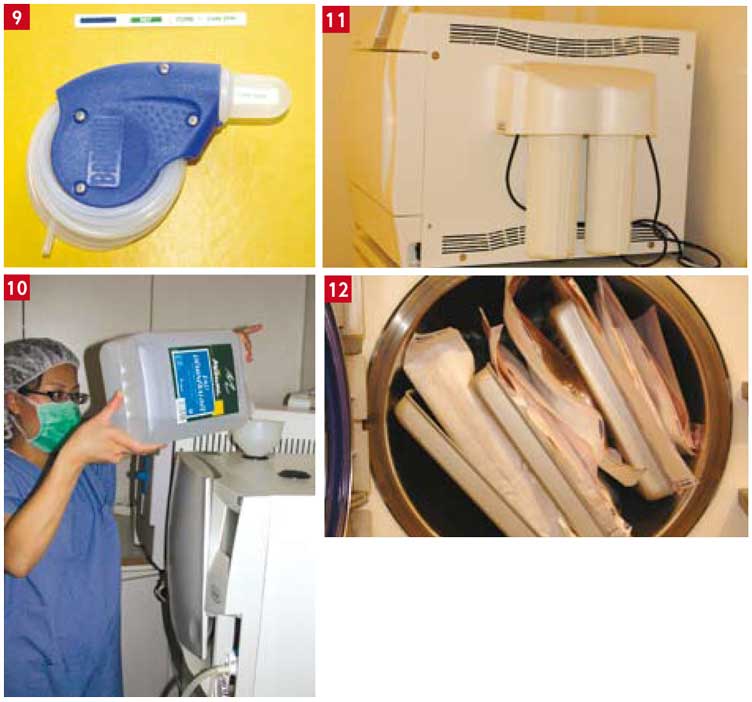
Fig. 9 : Test Hélix Fig. 10 : Stérilisateur à cuve d’eau déminéralisée Fig. 11 : Déminéralisateur adapté sur l’appareil Fig. 12 : Cuve trop chargée
Une vapeur d’eau propre et déminéralisée
Choisir l’eau distillé ou déminéralisée de qualité. Nettoyer la cuve à eau du stérilisateur : risque de biofilm dans le cas d’inutilisation durant plus de 4 jours : vidanger ; remplir de nouveau les cuves. Ajouter 0,3 litre d’alcool , laisser agir 30 minutes ; remplir à nouveau des réservoirs ; il est intéressant de faire cette opération tous les mois (Fig.10).
Pratique :
- Utiliser de préférence un déminéralisateur adapté assurant une qualité d’eau parfaite (Fig. 11).
- Un signal est émis lorsque le déminéralisateur devient inopérant.
Vérifier l’absence de fuite
Des fuites dans les circuits du stérilisateur peuvent occasionner une réduction de la quantité de vapeur. Ce test, facile et rapide, à lancer à froid, est inclus dans le programme du stérilisateur.
Pratique :
L’assistante, en allumant l’appareil le matin, fait démarrer le programme du test de fuite.
Vérifier le cycle de stérilisation
Les stérilisateurs sont souvent équipés d’une carte mémoire des cycles. Sinon, il faut acquérir une imprimante ou tout autre moyen d’enregistrement des différentes étapes du cycle de stérilisation. Vérifier à la lecture le bon déroulement des étapes.
Pratique :
Vérifier que l’enregistrement correspond à l’enregistrement de référence, obtenu lors de la livraison de l’appareil (à la validation de la réception).
« Aérer » la charge dans le stérilisateur
Un appareil surchargé, n’est plus apte à stériliser. Le vide difficile à réaliser ne permet pas à la vapeur d’atteindre toutes les surfaces des DM. Les emballages ne doivent pas être en contact avec les parois (Fig.12).
- Choisir des supports de charge adaptés. Exigez-les auprès de votre vendeur (Fig. 13) ;
- Choisir la taille des cassettes pour en mettre trois par cycle de stérilisation (Fig.14) ;
- Disposer les emballages verticalement, sur la tranche.
Vérifier en sortie du stérilisateur
- La siccité et l’intégrité des emballages ;
- Le virage des indicateurs de passage ;
- Le virage de l’intégrateur physico-chimique.
Entretenir le stérilisateur
Chaque semaine :
- Nettoyer plateaux, cuve, joint de porte à l’alcool (Ph 15, 16). Prendre un détergeant abrasif (Cif) en cas de saleté rebelles ;
- Les taches, avec un produit pour traiter les surfaces inoxydables.
Tous les 1000 cycles :
- Nettoyer les réservoirs : vidanger et remplir de l’eau déminéralisée et 0,3 litre d’alcool à 90° – maintenir 30 minutes – vidanger ;
- Remplacer le joint de porte ;
- Visite de maintenance par un technicien agréé ;

Fig. 13 : Support bien adapté Fig. 14 : Cassettebine séparée, verticales Fig. 15 : Joint de porte à l’alcool Fig. 16 : Nettoyage de la cuve
Conclusion
Actuellement, la qualité de nos stérilisateurs permet la mise en œuvre d’un ensemble de mesures appropriées et systématiques qui certifient l’obtention de la qualité requise (assurance qualité). Toutefois, dans la technique de la stérilisation, le résultat escompté dépend essentiellement du facteur humain. La formation du personnel, la mise au point de protocoles assurant le suivi, la conscience de la prévention des risques infectieux, permettent, par un ensemble de petits gestes et d’attention, la certitude d’une stérilisation bien accomplie.
BIBLIOGRAPHIE
1. AFNOR FD S98-135 :2004 : GOULLET D., ROZENBAUM M : Stérilisation des dispositifs médicaux- maîtrise des traitements appliqués aux dispositifs médicaux réutilisables.
2. CIRCULAIRE DGS/V5C-DHOS/E2 N° 138 du 14 mars 2001 relative aux précautions à observer lors de soins en vue de réduire les risques de transmission d’agents transmissibles non conventionnels.
3. Guide de prévention des infections liées aux soins en chirurgie dentaire et en stomatologie. Htp:/www.sante.gouv.fr ; ministère de la Santé et des Solidarités ; 2006
4. Missika P, Drouhet G. Hygiène, asepsie, ergonomie, un défi permanent. Collection JPIO, Ed. CdP.2001.
5. Normes NF EN 554 : Stérilisation des dispositifs médicaux. Validation et contrôle de routine pour la stérilisation par la vapeur d’eau.
6. ZEITOUN R. : Actualité et évolution de la pratique en stérilisation ; I.D. 40 ; 2529-2532 ; 11.2005.