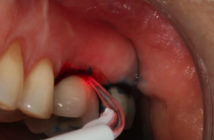
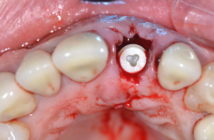
Le maxillaire postérieur édenté présente fréquemment une quantité et une qualité osseuses insuffisantes pour une réhabilitation implantaire prévisible. Ainsi, la résorption osseuse crestale couplée à la pneumatisation du sinus maxillaire sont souvent évidentes après la perte des dents postérieures (Misch and Judy 1987). L’élévation sinusienne par voie latérale (ESVL) a été introduite pour restaurer les maxillaires postérieurs atrophiques (Boyne and James 1980, Tatum 1986).
Cette procédure est largement utilisée de nos jours. En effet, une étude récente a montré que parmi 502 implants placés dans le maxillaire postérieur, 272 implants (54,2 %) ont été associés à une augmentation sinusienne (Seong, Barczak et al. 2013). Ceci nous amène en tant que chirurgiens à bien comprendre l’anatomie et la physiologie du sinus, les différentes techniques chirurgicales ainsi que les biomatériaux couramment utilisés afin de mener avec succès nos greffes sinusiennes.
Dans cet article, nous allons exposer les différentes étapes relatives a l’ESVL tout en mettant en évidence l’importance des nouvelles techniques radiologiques pour la planification et le suivi a long terme ainsi que les progrès relatifs à la technique chirurgicale qui visent à la simplifier et à diminuer les complications en per et en post-opératoire.
Planification préopératoire
La technologie radiographique est un outil majeur pour la planification de l’ ESVL et pour le suivi de l’os greffé (Harris, Horner et al. 2012). Depuis l’introduction de la tomographie volumique numérisée à faisceau conique (CBCT) (Mozzo, Procacci et al. 1998), elle est désormais la technique de choix pour l’exploration des sinus paranasaux notamment avant l’ESVL (Harris, Horner et al. 2012). Le CBCT s’est montré très utile dans l’évaluation et le dépistage des variations anatomiques et pathologiques du sinus (Pelinsari Lana, Moura Rodrigues Carneiro et al. 2012).
Dans une étude récente, des coupes tomographiques ont été réalisées pour explorer les sinus maxillaires chez 275 patients ; 45,1 % de ces scans ont dévoilé des pathologies sinusiennes allant d’un simple épaississement membranaire à l’opacification sinusienne totale (Manji, Faucher et al. 2013) (fig. 1). Ces observations soulignent l’importance de l’exploration radiologique du sinus maxillaire avant toute ESVL afin d’exclure toute condition pathologique qui pourrait compliquer cet acte.
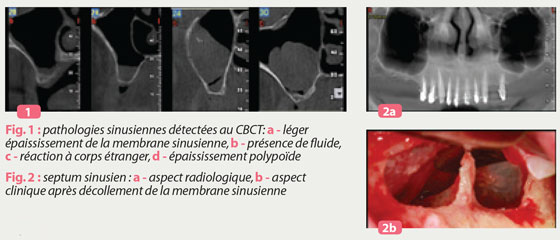
Les variations anatomiques telles que la hauteur de la crête résiduelle, l’épaisseur du mur vestibulaire et la profondeur du sinus doivent être souvent évaluées lors de l’examen radiologique et guident le praticien dans le choix de la technique d’élévation sinusienne. La présence de septa doit aussi être détectée sur le CBCT avant l’ESVL, afin de prévenir une perforation de la membrane de Schneider (fig. 2). En 2012, Pelinsari et al. ont détecté cette variation anatomique dans 44,4 % des 500 sinus explorés à l’aide de CBCT.
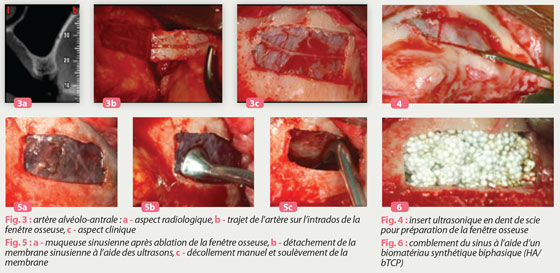
De même, l’artère alvéolo-antrale, anastomose entre la branche dentaire de l’artère alvéolaire postéro-supérieure et l’artère sous-orbitaire, souvent présente dans le mur antérolatéral du sinus, doit être repérée (Rosano, Taschieri et al. 2011) (fig. 3). La lésion de cette artère durant la préparation de la fenêtre osseuse du sinus ne mène généralement pas à une hémorragie dangereuse, mais induit certainement une inondation du champ opératoire gênant l’opérateur pendant le soulèvement de la membrane de Schneider.
Technique chirurgicale
Bien que les instruments rotatifs aient été les outils de choix lors de la réalisation des premières ESVL (Boyne and James 1980), la chirurgie piézoélectrique représente actuellement la technique de choix pour la préparation de la fenêtre latérale et l’élévation de la membrane de Schneider (Vercellotti, De Paoli et al. 2001). Vu leur action sélective, coupant les tissus durs sans léser les tissus mous, les instruments ultrasoniques se sont avérés très précis et efficaces lors de l’ostéotomie de préparation de la fenêtre latérale et très conservateurs vis-à-vis des tissus mous de manière à réduire considérablement les perforations de la membrane de Schneider (Vercellotti 2004).
La technique de base consiste à créer, à l’aide d’inserts ultrasoniques diamantés ou en dent de scie, une fenêtre osseuse au niveau du mur vestibulaire du sinus maxillaire (fig. 4). Une fois le volet osseux enlevé, cette fenêtre permet l’accès direct à la muqueuse sinusienne. Cette muqueuse est ensuite minutieusement détachée de l’os du sinus, afin d’éviter des déchirures de la membrane, à l’aide d’inserts ultrasoniques ou de décolleurs manuels (fig. 5). Une fois la membrane libérée et décollée, le greffon est posé dans l’espace créé entre le fond du sinus et la muqueuse décollée (fig. 6). Une membrane en collagène est ensuite posée sur la fenêtre, en vestibulaire, afin de protéger le biomatériau nouvellement greffé.
Choix du biomatériau
Pour une augmentation sinusienne prévisible, plusieurs biomatériaux peuvent être utilisés :
- blocs d’os autogènes récoltés de sites donneurs extra-oraux (iliaques ou crâniens) (Tulasne 1999) ;
- blocs d’os autogènes récoltés de sites donneurs intra-oraux (menton, ligne oblique externe) (Wood and Moore 1987) ;
- allogreffes, os humain provenant d’une banque d’os recevant un traitement spécial de désinfection et de stérilisation (Froum, Wallace et al. 2006) ;
- xénogreffes, os d’origine animale, notamment bovine, qui suit aussi des processus complexes de préparation et de stérilisation avant son utilisation sur les humains (Yildirim, Spiekermann et al. 2001) ;
- les biomatériaux synthétiques (Zijderveld, Zerbo et al. 2005) : les plus couramment utilisés sont l’hydroxyapatite (HA), le beta Tricalcium phosphate (βTCP) ou la forme biphasique regroupant les deux biomatériaux (HA-βTCP) afin de moduler leur temps de résorption.
Le choix du biomatériau est essentiellement évalué par le chirurgien. Les propriétés du biomatériau utilisé, notamment la biocompatibilité, l’ostéoconduction, la résorption ou éventuellement le coût peuvent guider son choix. L’association de plusieurs biomatériaux, l’adjonction d’os autogène ou l’utilisation de concentrés plaquettaires peuvent être aussi envisagés afin de moduler l’action du greffon.
 Suivi radiographique post-opératoire
Suivi radiographique post-opératoire
Le sinus maxillaire est tapissé d’un épithélium respiratoire cilié pseudostratifié, qui le protège contre les agents exogènes à travers son action de barrière physique et un système de vidange mécanique (Torkkeli, Rautiainen et al. 1994). Suite au traumatisme chirurgical, cette muqueuse subit une réaction inflammatoire intense clairement décrite durant le processus de cicatrisation des muqueuses nasales et paranasales (Watelet, Bachert et al. 2002). En effet, ce processus a été divisé en quatre phases qui s’imbriquent : inflammation, prolifération cellulaire, déposition matricielle et remodelage tissulaire.
Les études radiographique suivant l’ESVL ont montré un aspect normal de la membrane de Schneider après de longues périodes de cicatrisation (Anduze‐Acher, Brochery et al. 2012). Néanmoins, peu d’études ont décrit les altérations dans la membrane immédiatement ou à des courtes périodes post-opératoires. Quirynen et al., dans une étude radiographique, ont été les premiers auteurs à décrire le comportement de la muqueuse sinusienne directement après l’élévation transversale du plancher sinusien (Quirynen, Lefever et al. 2014).
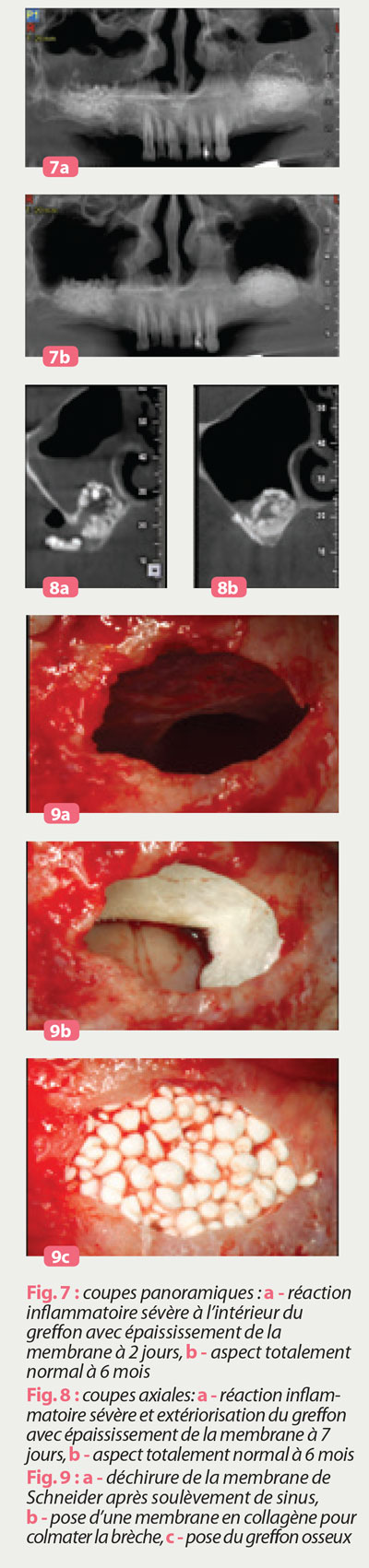
Ils ont démontré un épaississement significatif de la muqueuse sinusienne à une semaine post-opératoire, qui a disparu complètement à un mois. Dans nos données radiographiques en cours de publication, l’épaississement membranaire est également remarquable après l’ESVL toujours accompagné par une réaction inflammatoire à l’intérieur du greffon qui varie de légère à sévère. Cependant, les radiographies de contrôle à 6 mois montrent une rémission totale caractérisée par la disparition complète de la réaction inflammatoire et un retour à la normale de l’épaisseur de la membrane sinusienne (données encore non publiées par les auteurs) (fig. 7-8).
Complications et succès cliniques à long terme
La complication principale rencontrée au cours de l’ESVL est la perforation de la membrane de Schneider. En effet, cette membrane assez fine peut être facilement dilacérée suite à une technique chirurgicale mal appropriée ou suite à la présence de facteurs de risque anatomiques.
L’utilisation des ultrasons afin d’accéder au sinus lors de la préparation de la fenêtre vestibulaire a significativement réduit les risques de perforation de la membrane du sinus (Wallace, Mazor et al. 2007).
Suite à la déchirure de la muqueuse sinusienne, le chirurgien pourra essayer de colmater la brèche si celle-ci est toujours de diamètre réduit. Les membranes en collagène ou plus récemment les membranes en fibrine telles que le PRF de Choukroun peuvent servir à fermer la déchirure avant de continuer normalement la procédure de greffe du sinus.
Toutefois, il convient avant toute chirurgie de détecter les facteurs de risque anatomiques pouvant augmenter le risque de déchirure de la membrane, notamment la présence de septum et l’épaisseur de la membrane, cette dernière étant en rapport direct avec le biotype du patient. Ainsi, les patients présentant un biotype fin présentent une membrane de Schneider fine plus prédisposée à être perforée (Aimetti, Massei et al. 2008).
D’autre part, des sinusites peuvent être rencontrées suite à une greffe sinusienne. Elles sont généralement dues à la présence d’une pathologie préexistante au niveau du sinus ou à la perforation non traitée de la membrane menant à la diffusion du biomatériau à l’intérieur du sinus. Le traitement de ces sinusites nécessite un traitement antibiotique couplé au nettoyage et au lavage de l’os greffé.
Cette procédure a montré un taux de succès élevé qu’elle soit réalisée avant ou pendant la pose d’implants. Del Fabbro et al. en 2004, dans une méta analyse, ont trouvé un taux de survie de 91,49 % pour les implants placés dans des sinus greffés (Del Fabbro, Testori et al. 2004, Pjetursson, Tan et al. 2008). Ces taux de survie étaient de 87,7 % quand le greffon était l’os autogène seul et 95,98 % lors de l’utilisation de biomatériaux. Les implants rugueux avaient un taux de survie nettement meilleur (95,98 %) que les implants lisses (85,64 %). Enfin, aucune différence n’a été notée dans le taux de survie quand les implants étaient placés simultanément avec la greffe de sinus ou de façon différée.
Conclusion
Les soulèvements de sinus par voie latérale représentent la technique chirurgicale de choix au niveau du maxillaire postérieur atrophique. La planification radiographique, à l’aide du CBCT, est un outil précieux afin de mettre en évidence les pathologies sinusiennes, de détecter les obstacles anatomiques et de planifier correctement l’ESVL. L’utilisation des ultrasons a simplifié la technique chirurgicale tout en diminuant les risques de perforation de la membrane de Schneider. Plusieurs biomatériaux d’origine humaine, animale ou synthétiques peuvent être utilisés de façon prévisible à l’intérieur du sinus. Le suivi post-opératoire a mis en évidence une réaction inflammatoire, parfois intense, suite à l’ESVL qui retourne à la normale à 6 mois.
Bibliographie
1. Aimetti, M., G. Massei, M. Morra, E. Cardesi and F. Romano (2008). “Correlation between gingival phenotype and Schneiderian membrane thickness.” Int J Oral Maxillofac Implants 23(6): 1128-1132.
2. Anduze‐Acher, G., B. Brochery, R. Felizardo, P. Valentini, S. Katsahian and P. Bouchard (2012). “Change in sinus membrane dimension following sinus floor elevation: a retrospective cohort study.” Clinical Oral Implants Research.
3. Boyne, P. J. and R. A. James (1980). “Grafting of the maxillary sinus floor with autogenous marrow and bone.” J Oral Surg 38(8): 613-616.
4. Del Fabbro, M., T. Testori, L. Francetti and R. Weinstein (2004). “Systematic review of survival rates for implants placed in the grafted maxillary sinus.” Int J Periodontics Restorative Dent 24(6): 565-577.
5. Froum, S. J., S. S. Wallace, N. Elian, S. C. Cho and D. P. Tarnow (2006). “Comparison of mineralized cancellous bone allograft (Puros) and anorganic bovine bone matrix (Bio-Oss) for sinus augmentation: histomorphometry at 26 to 32 weeks after grafting.” The International journal of periodontics & restorative dentistry 26(6): 543.
6. Harris, D., K. Horner, K. Gröndahl, R. Jacobs, E. Helmrot, G. I. Benic, M. M. Bornstein, A. Dawood and M. Quirynen (2012). “EAO guidelines for the use of diagnostic imaging in implant dentistry 2011. A consensus workshop organized by the European Association for Osseointegration at the Medical University of Warsaw.” Clinical Oral Implants Research 23(11): 1243-1253.
7. Manji, A., J. Faucher, R. R. Resnik and J. B. Suzuki (2013). “Prevalence of Maxillary Sinus Pathology in Patients Considered for Sinus Augmentation Procedures for Dental Implants.” Implant dentistry 22(4): 428-435.
8. Misch, C. E. and K. W. Judy (1987). “Classification of partially edentulous arches for implant dentistry.” Int J Oral Implantol 4(2): 7-13.
9. Mozzo, P., C. Procacci, A. Tacconi, P. T. Martini and I. A. B. Andreis (1998). “A new volumetric CT machine for dental imaging based on the cone-beam technique: preliminary results.” European radiology 8(9): 1558-1564.
10. Pelinsari Lana, J., P. Moura Rodrigues Carneiro, V. de Carvalho Machado, P. Eduardo Alencar de Souza, F. Ricardo Manzi and M. Campolina Rebello Horta (2012). “Anatomic variations and lesions of the maxillary sinus detected in cone beam computed tomography for dental implants.” Clinical Oral Implants Research 23(12): 1398-1403.
11. Pjetursson, B. E., W. C. Tan, M. Zwahlen and N. P. Lang (2008). “A systematic review of the success of sinus floor elevation and survival of implants inserted in combination with sinus floor elevation.” Journal of Clinical Periodontology 35(s8): 216-240.
12. Quirynen, M., D. Lefever, P. Hellings and R. Jacobs (2014). “Transient swelling of the Schneiderian membrane after transversal sinus augmentation: a pilot study.” Clin Oral Implants Res 25(1): 36-41.
13. Rosano, G., S. Taschieri, J. F. Gaudy, T. Weinstein and M. Del Fabbro (2011). “Maxillary sinus vascular anatomy and its relation to sinus lift surgery.” Clinical oral implants research 22(7): 711-715.
14. Seong, W.-J., M. Barczak, J. Jung, S. Basu, P. S. Olin and H. J. Conrad (2013). “Prevalence of sinus augmentation associated with maxillary posterior implants.” Journal of Oral Implantology 39(6): 680-688.
15. Tatum, H., Jr. (1986). “Maxillary and sinus implant reconstructions.” Dent Clin North Am 30(2): 207-229.
16. Torkkeli, T., M. Rautiainen and J. Nuutinen (1994). “Ciliary ultrastructure and mucociliary transport in upper respiratory tract infections.” American Journal of Rhinology 8(5): 211-215.
17. Tulasne, J. F. (1999). “Sinus grafting with calvarial bone.” The Sinus Bone Graft, London: Quintessence Publishing Co: 107-116.
18. Vercellotti, T. (2004). “Technological characteristics and clinical indications of piezoelectric bone surgery.” Minerva Stomatol 53(5): 207-214.
19. Vercellotti, T., S. De Paoli and M. Nevins (2001). “The piezoelectric bony window osteotomy and sinus membrane elevation: introduction of a new technique for simplification of the sinus augmentation procedure.” Int J Periodontics Restorative Dent 21(6): 561-567.
20. Wallace, S. S., Z. Mazor, S. J. Froum, S. C. Cho and D. P. Tarnow (2007). “Schneiderian membrane perforation rate during sinus elevation using piezosurgery: clinical results of 100 consecutive cases.” Int J Periodontics Restorative Dent 27(5): 413-419.
21. Watelet, J.-B., C. Bachert, P. Gevaert and P. Van Cauwenberge (2002). “Wound healing of the nasal and paranasal mucosa: a review.” American journal of rhinology 16(2): 77-84.
22. Wood, R. M. and D. L. Moore (1987). “Grafting of the maxillary sinus with intraorally harvested autogenous bone prior to implant placement.” The International journal of oral & maxillofacial implants 3(3): 209-214.
23. Yildirim, M., H. Spiekermann, S. Handt and D. Edelhoff (2001). “Maxillary sinus augmentation with the xenograft Bio-Oss and autogenous intraoral bone for qualitative improvement of the implant site: a histologic and histomorphometric clinical study in humans.” The International journal of oral & maxillofacial implants 16(1): 23-33.
24. Zijderveld, S. A., I. R. Zerbo, J. P. van den Bergh, E. A. Schulten and C. M. ten Bruggenkate (2005). “Maxillary sinus floor augmentation using a beta-tricalcium phosphate (Cerasorb) alone compared to autogenous bone grafts.” Int J Oral Maxillofac Implants 20(3): 432-440.