L’halitose, de son diagnostic à son traitement, est un aspect peu développé dans l’exercice quotidien du chirurgien-dentiste. Elle est pourtant bien plus commune qu’on ne le croit. L’halitose peut toucher tout le monde, à une occasion précise ou à un moment particulier de la journée. Les étiologies possibles sont variées. Les causes d’origine dentaire représentent au moins 85 % des cas. Les autres étiologies impliquées sont : O.R.L., gastro-intestinale, pulmonaire, respiratoire, métabolique, hormonale, comportementale, psychologique ou liée à la prise de médicaments. L’halitose signe souvent une affection bénigne. Cependant, elle permet de révéler et de diagnostiquer des maladies plus graves telles que tumeurs malignes, insuffisance rénale ou diabète. De ce fait, cette pathologie aux causes multiples ne doit en aucun cas être traitée à la légère.
L’halitose, un fléau social
Dans notre monde aseptisé, le marketing de notre civilisation occidentale de ce début du 21e siècle a réussi à nous convaincre que l’être humain, l’homme, la femme, est un être jeune ou éternellement rempli de jeunesse, beau, dynamique, en pleine possession de ses moyens.
Son sourire est éclatant, il dégage le bonheur de vivre. Il embrasse goulûment la vie et la vie lui sourit. L’espace dans lequel il vit sent la rose, la lavande, le muguet ou le jasmin. Cet humain se doit de sentir bon. Il s’asperge régulièrement de lotions parfumées acquises au mieux dans de luxueuses parfumeries géantes, au pire dans des supermarchés du quartier entre shampoing, dentifrice et mousse à raser. Quand le tout esthétique règne en maître absolu, quand le credo consiste à plaire à tous et le plus longtemps possible, avoir une mauvaise haleine devient un handicap majeur de la vie en société. Dans ce monde de grande promiscuité, exhaler de mauvaises odeurs devient, sans faire de jeux de mots douteux, une affaire de mauvais goût, comme une inaptitude au bonheur. Le temps où le roy Henri IV pouvait écrire à son amante : « cessez de vous laver, ma mie, j’arrive » est révolu.

Fig 1 : l’halitose peut toucher tout un chacun, sans distinction… de distinction ou de niveau social.
Le fléau étend ses tentacules jusqu’au bout du monde car 25-40 % de la population mondiale en est atteinte de manière chronique sans distinction de position sociale ou autre (Fig. 1). Chacun d’entre nous est touché à un quelconque moment de la journée, plus particulièrement au lever ou entre les repas trop espacés. C’est ce qui explique un marché de plusieurs milliards d’euros de chiffre d’affaires que se partagent les marchands de cache-misère de la mauvaise haleine, entre chewing-gum parfumés, bains de bouche et autres liquides ainsi que de petits appareils de détection de mauvaise haleine, fort en vogue au Japon. Une recherche avec le mot-clé « mauvaise haleine » sur Internet mène à 251 000 résultats. Voici quelques uns des cris de désespoir poussés par la communauté des hommes et des femmes atteints de plein fouet par cette maladie qui, socialement, tue à petit feu (Fig. 2).
Le terme « halitose » est un mot créé vers 1930. Cet hybride est formé de la combinaison d’un élément latin et d’un élément grec. Halitus en latin signifie haleine ou souffle, ôsis [-ose] est un suffixe grec désignant un trouble, plus précisément des maladies non inflammatoires ou/et des états chroniques.
Si le mot « halitose » est relativement récent, les maux qu’il recouvre datent depuis les temps les plus reculés de l’humanité. Le Cantique des Cantiques attribué au roi Salomon de Jérusalem, dans une poésie d’amour vieille de 3 000 ans, vante les saveurs suaves de lait et de miel émanant de la bouche de la bien-aimée. La fiancée de la poésie est épargnée par l’halitose, alors qu’aujourd’hui, sur Internet et dans les cabinets dentaires, les amoureux crient leur désespoir de ne pouvoir approcher l’être aimé par crainte d’être repoussés (Fig. 2a, 2b).
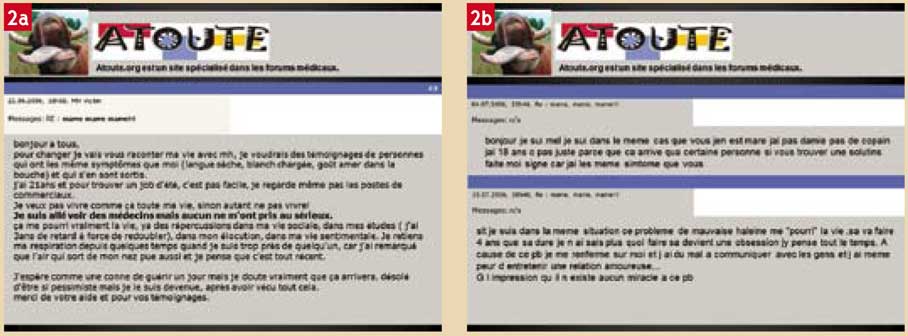
Fig. 2 : cris de désespoir que l’on peut trouver sur Internet. 2a : le désarroi et le déni des médecins face au problème perçu par les patients. 2b : le désarroi des patients qui ne savent comment sortir de cet enfer.
Le fléau ne date pas d’hier car on lui retrouve des traces depuis l’Antiquité. Dans le monde de la littérature grecque, trois hommes, Theodorus, Diodorus et Mentorides, sont célèbres pour leur mauvaise haleine. Mentorides se fait interpeller par le poète qui lui demande :
« Qui serait donc celui qui a déplacé ton postérieur là où avant se trouvait ta bouche ? ». Le trait d’humour touche droit au but, il fait sourire le spectateur, mais imaginez la douleur de celui qui reçoit la flèche.
Ce mal pénètre toutes les sphères, de l’amour au politique en passant par le droit. En amour, une ancienne plaisanterie grecque met en scène un homme affligé par ce trouble. L’homme demande à sa femme : « Chérie, quel est le motif de ta distance envers moi ? » et la femme de lui répondre : « C’est parce que tu m’aimes et m’embrasses ! ».
Sous d’autres latitudes, le protocole de la cour impériale de la Chine ancienne s’en est trouvé affecté. Les empereurs exigeaient de leurs visiteurs de mâcher des clous de girofle avant de venir s’entretenir avec eux.
Depuis toujours, des remèdes ont été proposés à ce mal fort répandu. Le Papyrus Ebers (vers 1700 av. J.-C.) cite une médication en usage dans l’Égypte ancienne afin d’adoucir l’haleine : « Prends de l’encens, de la myrrhe, de la cannelle, de l’écorce et d’autres plantes odorantes. Fais les bouillir avec du miel et fais-en des pastilles. »
Hippocrate (460-377 av. J.-C.) nous livre un remède quelque peu exotique destiné aux femmes souffrant de mauvaise haleine. Il leur recommande de se brosser les dents avec de la poudre de marbre mélangée à de la cendre issue des têtes d’un lièvre et de trois souris.
Chaque pays, comme chaque époque, possède ses remèdes traditionnels à base de plantes : le persil à Rome, le clou de girofle en Mésopotamie, les feuilles de goyave verte en Thaïlande, la coquille d’oeuf pilée en Chine.
Au Moyen Âge, entre 700 et 1 000 après J.-C., le métal argent a connu son heure de gloire thérapeutique au Moyen-Orient. Des remèdes à base d’argent étaient censés contrôler la mauvaise haleine et purifier les sangs.
En 1755, Julien Botot met au point une lotion dentaire à base de badiane, de girofle, de cannelle, d’essence de menthe et d’alcool. Elle doit donner à l’haleine une odeur suave, fortifier les gencives et entretenir la blancheur des dents.
Plus proche de nous, le premier texte totalement dévolu à la mauvaise haleine est publié en 1898 aux États-Unis par J.W. Howe. Dans les années trente, le sujet revient dans les préoccupations du moment. En 1939, Brening met au point l’omoscope, le premier instrument de mesure de la mauvaise odeur. Curieusement, il faut attendre les années soixante et Tonzetich, un biologiste de l’université de Vancouver, pour que des scientifiques s’attellent à ce fléau mondial. En 1993, le premier atelier international sur l’halitose a lieu à Tel Aviv sous l’impulsion de Mel Rosenberg, un autre microbiologiste ayant travaillé sur le sujet. Cette initiative se traduit en 1996 par la création de la Société internationale pour la recherche sur l’halitose avec la présence, enfin, d’odontologistes et de biologistes. Des consultations spécialisées existent en Europe, en Amérique du Nord, en Extrême-Orient et en Israël. A en croire Internet, la consultation de l’Hôpital Américain à Paris est une partie prenante reconnue de ce groupe.
Evaluation de la mauvaise haleine
L’examen clinique repose sur les éléments classiques de toute consultation :
- une anamnèse et un interrogatoire sur les habitudes du sujet :
- le mode de vie : alcool, café, régime riche en protéine, tabagisme
- les allergies
- les antécédents médicaux : dépression, diabète…
- le traitement en cours
- un examen exobuccal
- un examen endobuccal : examen dentaire et de la muqueuse buccale, mesure de différents indices (de plaque, gingival, parodontaux), mesure de la profondeur des poches
- des examens complémentaires (examens radiographiques, halimètre…).
L’évaluation de la mauvaise haleine se fait par 2 méthodes, une subjective et une autre objective. Le patient doit s’abstenir de toute prise alimentaire (surtout des aliments à fortes émanations tels que l’ail, les oignons, etc., et toute prise de boisson alcoolisée), de soins d’hygiène buccodentaire, de soins cosmétiques odorants (parfums, shampooings, crème de visage…) et de fumer quatre heures avant toute mesure.
Méthodes subjectives
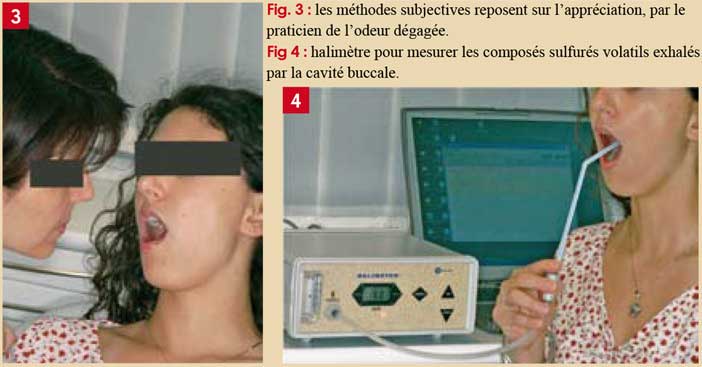
Les méthodes subjectives ou organoleptiques sont très pratiques mais ne permettent pas une évaluation précise de la mauvaise haleine. Elles reposent sur l’appréciation de l’odeur dégagée dans :
- l’air expiré par la bouche ou par le nez du patient ;
- la salive du patient ;
- la plaque dentaire existant au niveau des dents ou des espaces interdentaires ;
- l’enduit de la partie postérieure de la langue.
L’échelle de référence pour les différentes mauvaises odeurs est la suivante :
- 0 = absence d’odeur désagréable ;
- 1 = mauvaise odeur à peine perceptible ;
- 2 = mauvaise odeur légèrement perceptible ;
- 3 = mauvaise odeur d’intensité moyenne ;
- 4 = mauvaise odeur forte ;
- 5 = mauvaise odeur très puissante.
Le test organoleptique peut être réalisé par :
- le praticien qui doit s’assurer que lui-même ne présente pas de troubles olfactifs afin de ne pas compromettre les résultats ;
- le patient lui-même ;
- une personne de confiance présente dans l’entourage du patient.
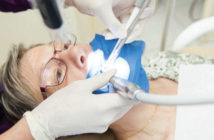
Test organoleptique réalisé par le praticien :
Le test est réalisé au fauteuil (Fig. 3). Chaque étape du test doit être précédée par une période de 1-2 minutes pendant laquelle le patient reste bouche fermée afin de favoriser l’accumulation des composants malodorants : le patient ouvre la bouche sans expirer. Une mauvaise haleine dans ce cas met en cause les différents éléments de la cavité buccale.
- le patient maintient sa bouche fermée et expire l’air par la narine gauche (la narine droite est obturée à l’aide de son doigt). Puis, la même manœuvre a lieu pour la narine droite. L’air expiré a comme origine, dans ce cas, la sphère ORL.
- le patient ouvre la bouche et expire légèrement l’air qui, dans ce cas, a comme origine la cavité buccale ou la partie supérieure des bronches.
- le patient ouvre la bouche et réalise une expiration forcée. Une odeur désagréable peut avoir comme étiologie une pathologie broncho-pulmonaire.
- le patient doit compter de 1 à 20 à haute voix ; ce qui favorise un dessèchement de la muqueuse et la libération de composants volatils malodorants présents au niveau de la cavité buccale.
Pour chaque étape, un score (selon la classification de Rosenberg) est accordé pour l’air émanant de la bouche ou du nez. De même, les dépôts de plaque présents au niveau des surfaces dentaires ou interdentaires ainsi que l’enduit lingual et la salive sont sentis et évalués selon le score de Rosenberg.
Test organoleptique réalisé par le patient
Le patient va évaluer :
- le fil dentaire après l’avoir passé dans les espaces interdentaires ;
- le gratte-langue (ou une petite cuillère) après nettoyage de la face dorsale de la langue ;
- la salive après l’avoir déposée dans une petite cuillère ;
- le dos de la main après l’avoir léché avec la zone la plus postérieure de la langue.
Test organoleptique réalisé par une personne de l’entourage du patient
Il est très difficile au patient lui-même de sentir sa propre haleine car les récepteurs olfactifs s’adaptent rapidement à une certaine odeur. Une personne de son entourage peut lui faire remarquer qu’il a une mauvaise haleine et lui indiquer les différents moments de la journée durant lesquels elle se manifeste.
Méthodes objectives
Les méthodes objectives de mesure de la mauvaise haleine mesurent les composés volatils à la source de l’halitose. Ces derniers sont détectés :
- par une méthode électrochimique (halimètre) qui détecte une partie des composés sulfurés volatils (CSV) ;
- par un procédé de chromatographie en phase gazeuse, plus précis mais bien plus coûteux.
Halimètre
La méthode d’évaluation avec l’halimètre (Fig. 4) ne révèle que la composante sulfurée ou CSV de la mauvaise haleine.
Les composés sulfurés de la mauvaise haleine proviennent de la décomposition des acides aminés soufrés (cystéine, cystine, méthionine) présents dans les substances organiques de la salive, les débris alimentaires, les cellules épithéliales exfoliées par les bactéries anaérobies Gram-négatif. Ils contiennent des groupements thiols (S-H) à l’odeur caractéristique d’œuf pourri.
Plusieurs composés sulfurés simples sont obtenus. Il s’agit du :
- sulfure d’hydrogène (H2S), le gaz nauséabond des « boules puantes ». Son seuil de détection est très faible ; il est de 0,5 ppb (partie par billion c’est-à-dire par milliard) alors que des concentrations de 80 ppb sont considérées comme normales et ne causent pas de mauvaises odeurs ;
- méthyl mercaptan (CH3-SH), un gaz ayant une odeur de chou putréfié, il est produit naturellement dans certains aliments comme le fromage ; son seuil de détection est 1,1 ppb ;
- sulfure de diméthyle (CH3-S-CH3), un gaz évoquant l’odeur de légumes pourris ; son seuil de détection est 1 ppb.
Ces composés sont toujours présents dans la bouche, cependant l’odeur n’est perceptible qu’au-delà d’une certaine concentration.
L’halimètre est composé d’un boîtier électronique qui contient la cellule électrochimique. Il donne une mesure en ppb. Un ordinateur est raccordé afin de visualiser le tracé obtenu. Le tracé montre un diagramme en fonction du temps, trois pics de concentration dont la moyenne donne la mesure finale. Les données peuvent être stockées électroniquement afin de suivre l’évolution de la présence des composés volatils sulfurés (CSV) au cours du temps. La précision de la mesure est de 5 ppb.
La mesure est effectuée dans un air exhalé successivement :
- de la cavité buccale ;
- des fosses nasales ;
- des poumons.
Ces trois séries de mesure permettent de comparer les concentrations de composés sulfurés contenues dans la bouche, le nez et les poumons et donc de mieux déterminer l’origine de l’halitose.
Mesure des composés sulfurés dans la cavité buccale
La bouche est fermée, les lèvres sont closes durant trois minutes avant d’effectuer la mesure. Des pailles sont préparées. La mise à zéro est effectuée sur l’appareil avant chaque mesure.
Le sujet prend une profonde inspiration par le nez et la retient durant dix à quinze secondes. C’est durant cet intervalle qu’a lieu la mesure. Un pic est enregistré dans les secondes suivant la mesure. La paille est retirée de la bouche du patient au bout de dix à quinze secondes. La mesure est répétée trois fois, le score final retenu est la moyenne des trois mesures.
L’halitose est :
- légère, quand les mesures des composés sulfurés varient entre 200-300 ppb (Fig. 5a) ;
- modérée, quand les mesures des composés sulfurés varient entre 300-500 ppb (fig. 5b) ;
- sévère, quand les mesures des composés sulfurés sont supérieures à 500 ppb.
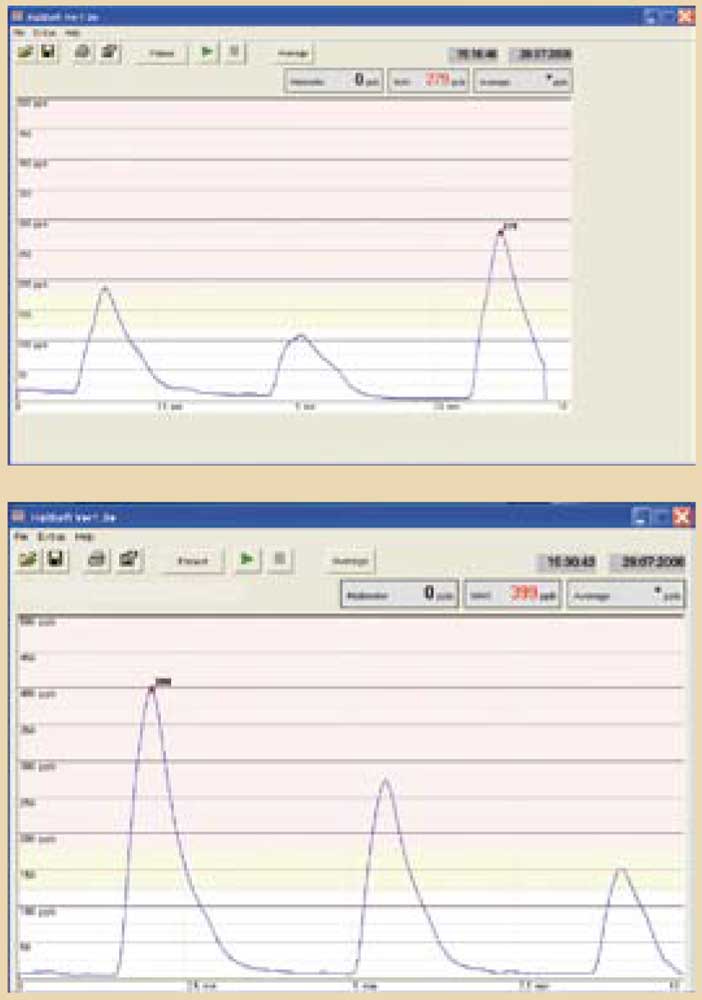
Fig. 5a : spectre caractéristique d’une légère halitose. La moyenne des trois mesures donne le score final. Fig. 5b : spectre caractéristique d’une halitose modérée.
Mesure des composés sulfurés dans la cavité nasale
Le patient se bouche le nez et respire par la bouche durant deux minutes. Une paille en plastique est introduite dans une des narines. Le patient retient sa respiration durant 10 à 15 secondes. Dans les secondes qui suivent, un pic est enregistré comme précédemment décrit. La mesure est triplée et la moyenne des mesures est calculée.
Mesure des composés sulfurés dans les poumons
Le patient respire normalement par la bouche durant trente secondes. À la fin d’une expiration, il lui est demandé de retenir sa respiration. Une paille en plastique est introduite dans la bouche. Le patient complète son expiration en chassant le reste de l’air contenu dans ses poumons. Dans les secondes qui suivent, un pic est enregistré comme précédemment décrit. La mesure est triplée et la moyenne des mesures est calculée.
Chromatographie en phase gazeuse
Contrairement à l’halimètre, la chromatographie en phase gazeuse ne se restreint pas aux composés soufrés. La méthode permet de séparer, d’identifier et de doser différents composants gazeux présents dans l’air expiré au travers de la bouche. Tous les composants volatils de la mauvaise haleine sont mis en évidence. Ce type d’analyse est cependant coûteux et sophistiqué. Courant en laboratoire, il ne peut se faire en routine au cabinet car il exige la présence d’un opérateur hautement qualifié. La méthode consiste à tester un échantillon prélevé lors d’une expiration exécutée dans un sac en plastique.
Comme précédemment pour l’halimètre, la mesure est effectuée dans un air exhalé successivement :
- de la cavité buccale ;
- des fosses nasales ;
- des poumons.
Les quantités de produits nécessaires à la réalisation d’une mesure sont très faibles, de l’ordre de 2 à 3 microlitres. Des concentrations inférieures au ppb (ng) peuvent être détectées.
Les gaz suivants sont typiquement identifiés :
- indole, un composé organique aromatique hétérocyclique (benzénique et pyrrole) C8H7N ;
- skatole, un indole méthylé, le 3-methylindole C9H9N ;
- polyamines (cadaverine NH2(CH2)5NH2 ; putrescine NH2(CH2)4NH2) ;
- dérivés azotés (méthylamine CH3NH2 ; diphénylamine (C6H5)2NH ; ammoniaque NH4OH ; urée CO(NH2)2) ;
- des acides gras à courte chaîne (acide butyrique CH3CH2CH2-COOH ; acide valérique CH3(CH2)3COOH) ;
- des alcools (dodécanol CH3(CH2)11 ; tétradécanol C14H29OH).
OralChroma
Cet appareil portable, léger et de faible encombrement, utilise la chromatographie en phase gazeuse pour détecter les gaz sulfurés malodorants. La machine a été simplifiée dans le but de permettre une plus large diffusion dans les cabinets dentaires ou dans les centres de soins spécialisés dans l’halitose.
La technologie classique de la colonne a été remplacée par des senseurs semi-conducteurs capables de détecter les gaz sulfurés. Cela simplifie les différents organes de l’appareillage et réduit l’encombrement, le poids et le coût de fabrication. La détection a été limitée aux trois CSV les plus courants précédemment cités car ils sont les plus représentatifs de l’halitose.
L’avantage par rapport à l’halimètre est de pouvoir doser la concentration de chacun des trois composés détectés avec, de surcroît, une plus grande précision. Le ou les gaz à incriminer dans la mauvaise haleine sont mieux identifiés et le diagnostic peut éventuellement être affiné. L’usage de l’appareil ne nécessite pas de grande compétence technique, son prix est abordable dans le cadre d’une consultation spécialisée.
Test BANA
Le test utilise un peptide, le N-benzoyl-DL-arginine-2-naphthylamide ou BANA. Seules les trois bactéries les plus pathogènes de la plaque, Treponema denticola, Porphyromonas gingivalis et Bacteroïdes forsythus sur les quelques soixante autres espèces présentes dans la plaque dentaire, possèdent une enzyme capable d’hydrolyser le BANA.
Cette méthode biochimique effectue une mesure indirecte de l’halitose. Elle permet de révéler la présence dans la cavité buccale de certaines bactéries anaérobies capables d’hydrolyser le BANA. Ces espèces, particulièrement pathogènes, sont présentes dans environ 90 % des cas de mauvaise haleine.
Le test (PerioscanTM, Oral B, Redwood City, California, USA) consiste à mettre en culture un prélèvement buccal en présence de la chaîne peptidique BANA.
Les bactéries anaéorobies pathologiques, par l’intermédiaire de leurs enzymes, hydrolysent la BANA en β-naphthylamide. Sur un réactif papier, cette dernière donne une couleur bleue. Le test, quand il est BANA positif, signe par une couleur bleue la présence de ces organismes pathogènes. L’intensité du bleu varie en fonction de la concentration de ces bactéries.
Le test est fort simple à utiliser. Un prélèvement est fait sur le dos de la langue ou dans les poches parodontales à l’aide d’un coton. Il est appliqué sur des bandelettes imbibées d’enzymes BANA et du réactif coloré. Une coloration signe la présence de ces bactéries pathogènes.
Le test est aussi sensible que les tests ADN car il révèle déjà la présence de cent colonies de bactéries, de plus, il est très spécifique. Le résultat peut être accessible dans les cinq minutes, il est donc rapide.
Pathologies bucco-dentaires en rapport avec l’halitose
85-90 % des cas d’halitose ont une origine buccale. Les différentes étiologies buccales incriminées dans la mauvaise haleine sont :
- principalement la langue,
- les maladies parodontales,
- les lésions carieuses profondes,
- la pulpe nécrosée à contenu purulent,
- l’alvéolite,
- les couronnes ou bridges mal adaptés avec mauvais points de contact,
- les prothèses amovibles à surface rugueuses ou mal entretenues,
- certaines pathologies de la muqueuse buccale,
- les troubles salivaires en terme de qualité et de quantité de la salive secrétée.
Les bactéries responsables de maladies parodontales ont une implication dans la dégradation des acides aminés à l’origine des composés volatils dont la concentration est proportionnelle à l’indice de saignement, à la profondeur et au nombre de poches parodontales.
Du fait de sa morphologie, la langue constitue un réservoir pour les pathogènes parodontaux et joue un rôle essentiel dans le dégagement des mauvaises odeurs qui émanent de la bouche.
Toute atteinte de la muqueuse buccale qui dure dans le temps, peut être responsable d’halitose par des mécanismes de surinfection, de nécrose tissulaire ou des difficultés d’hygiène.
La salive est importante dans le maintien de l’équilibre de la flore buccale. Toute altération salivaire est susceptible de provoquer une mauvaise haleine.
Le traitement concernant la cavité buccale consiste à éliminer la cause de la mauvaise haleine sans juste chercher à la masquer :
- soin des caries ;
- reconstitution des dents délabrées ;
- réajustement des prothèses mal adaptées, ou nécessité de les faire à nouveau ;
- assainissement des muqueuses et du parodonte ;
- administration de stimulants salivaires (chewing-gums, citron, médicaments) en cas d’hyposialie ou asialie.
L’utilisation de salives artificielles permet d’assurer une hydratation buccale. Un traitement adjuvant comprenant une application topique fluorée peut être d’un grand bénéfice pour la prévention des caries abondantes dans les syndromes de sécheresse buccale.
L’hygiène et le brossage jouent un rôle prépondérant dans le contrôle de la plaque et des mauvaises odeurs buccales. Un brossage dentaire et lingual adéquat est nécessaire.
L’utilisation des produits et instruments complémentaires au brossage (fil dentaire, brossette…) permet un meilleur contrôle de l’hygiène et de l’halitose.
Etiologies extra-buccales de la mauvaise haleine
Dans le cadre du bilan étiologique du patient consultant pour une mauvaise haleine, la consultation d’ORL doit être envisagée à la recherche des causes extra-orales de l’halitose. La fréquence des causes extra-orales est variable. Selon les études, elle concerne entre 7 et 15 % du total des patients atteints d’une halitose pathologique.
Parmi ces causes extra-orales, les pathologies ORL constituent la seconde cause d’halitose, elles sont plus fréquentes que les facteurs d’origine métabolique ou gastro-intestinale.
Les pathologies de la sphère ORL susceptibles de générer une halitose ont comme dénominateur commun la présence des composés sulfurés volatils (CSV) véhiculés par la respiration oro-nasale. Ces composés confèrent le caractère malodorant à la respiration. Ces CSV sont produits soit par les bactéries impliquées dans un processus infectieux de la sphère ORL, soit par la dégradation des protéines de nature endogène (processus de nécrose tissulaire) ou exogène (processus de putréfaction des détritus alimentaires).
Voici une liste des pathologies infectieuses les plus fréquentes :
Pathologies naso-sinusiennes :
- les rhinites chroniques croûteuses (formes ozéneuses ou non) sont des infections diffuses de la muqueuse des fosses nasales, elles se traduisent par une fétidité importante. Le traitement repose essentiellement sur une antibiothérapie accompagnée d’un lavage des fosses nasales au sérum physiologique.
- la sinusite purulente chronique unilatérale d’origine dentaire est la plus fréquente. Il s’agit d’une inflammation chronique de la muqueuse du sinus maxillaire à partir d’un foyer dentaire. Les signes se manifestent par un écoulement postérieur, parfois un mouchage épais unilatéral, avec une cacosmie et une halitose. Le scanner montre une opacité du sinus maxillaire.
- la sinusite mycosique non invasive est localisée essentiellement au niveau du sinus maxillaire. Les signes cliniques consistent en une sensation d’écoulement postérieur, une halitose et une sensation de pesanteur faciale. Le traitement est exclusivement chirurgical.
- les rhinolithes sont des corps étrangers dans les fosses nasales produisant une inflammation de la muqueuse.
Elle se révéle secondairement par une halitose ou par un écoulement nasal purulent. Le traitement consiste en l’ablation de ces corps étrangers. - l’imperforation choanale unilatérale est une anomalie congénitale se traduisant par un écoulement unilatéral épais et une halitose due à une fermeture postérieure de l’une des fosses nasales. Le traitement est chirurgical.
Les pathologies amygdaliennes :
- l’amygdalite chronique infectante est caractérisée par une colonisation bactérienne latente des amygdales palatines.
Le diagnostic est évoqué lorsque la pression sur le pilier antérieur de l’amygdale fait apparaître des sécrétions louches au niveau des cryptes amygdaliennes. Le traitement est chirurgical lorsque le patient présente un terrain à risque.
- l’amygdalite chronique caséeuse consiste en une production continue de leucocytes qui migrent de la profondeur du parenchyme glandulaire vers les cryptes. Elle s’élimine sous la forme de concrétions blanc-jaunâtre riches en CSV responsables de l’halitose. Des séances de photothérapie au laser et des gargarismes peuvent être proposés.
Les pathologies tumorales malignes :
- le point de départ de ces pathologies se trouve souvent au niveau de la muqueuse des voies aéro-digestives supérieures ;
- les localisations au niveau de l’épiglotte et du carrefour pharyngolaryngé peuvent s’associer fréquemment avec l’halitose ;
- les tumeurs à évolution ulcérative ou végétante se combinent généralement à des phénomènes de nécrose tissulaire en surface. Elles conduisent à une production importante de CSV à l’origine d’une halitose pathologique.
Les diverticules pharyngo-oesophagiens :
- le diverticule de Zenker (Fig. 6) est la forme la plus fréquente. Il se forme par une hernie de la muqueuse à travers une zone de faiblesse à la jonction entre le pharynx et l’oesophage.
- les diverticules peuvent atteindre des dimensions importantes et la stagnation des aliments à l’intérieur engendre des phénomènes de fermentation et putréfaction provoquant une halitose qui peut révéler la pathologie.
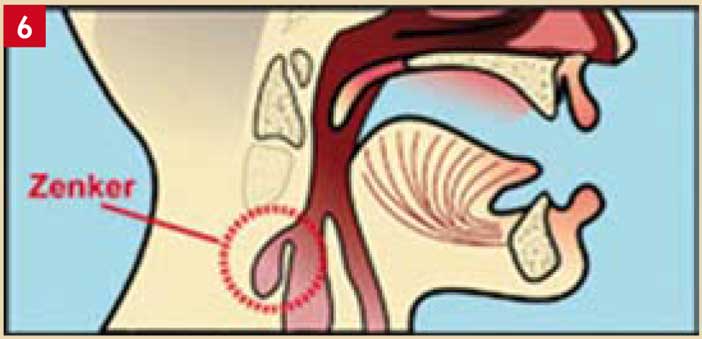
Fig. 6 : diverticule de Zenker. Il est le lieu de fermentation et putréfaction des aliments ingérés
Pathologies médicales générales de l’halitose
En l’absence d’une étiologie bucco-dentaire, le chirurgien-dentiste doit collaborer avec les autres professionnels en considérant qu’elle peut être l’expression d’une pathologie plus générale. L’ensemble des causes d’halitose lié aux pathologies médicales générales est représenté par :
Les pathologies pulmonaires et respiratoires
- des voies aériennes supérieures (infections, inflammations, corps étrangers, soins dentaires)
- des voies aériennes inférieures (bronchite chronique, bronchectasie, cancers pulmonaires, inhala tion de corps étrangers ou du contenu gastrique, tuberculose pulmonaire).
Les pathologies gastro-intestinales
- reflux gastro-oesophagien (Fig. 7) ;
- achalasie ;
- cancer de l’oesophage ;
- ulcère gastroduodénal ;
- sténose du pylore.
Les pathologies fonctionnelles et syndromes de malabsorption
- les causes métaboliques :
- insuffisance hépatocellulaire ;
- insuffisance rénale ;
- diabète ;
- cétose du jeûne ;
- triméthylaminurie.
Les troubles sensoriels et psychologiques
Lors des plaintes d’halitose non objectivées par l’examen clinique, et une fois les causes organiques et fonctionnelles écartées, on peut évoquer une pathologie psychiatrique.
Les cas les plus fréquemment rencontrés sont :
- convictions, plus ou moins « délirantes » ;
- certaines psychoses et dysmorphophobies ;
- certaines mélancolies délirantes, avec l’existence d’un syndrome de Cotard ;
- de véritables halitoses secondaires à des pathologies psychiatriques.
La prise de médicaments
- traitements aux corticostéroïdes par inhalation ;
- traitements à base d’antidépresseurs.
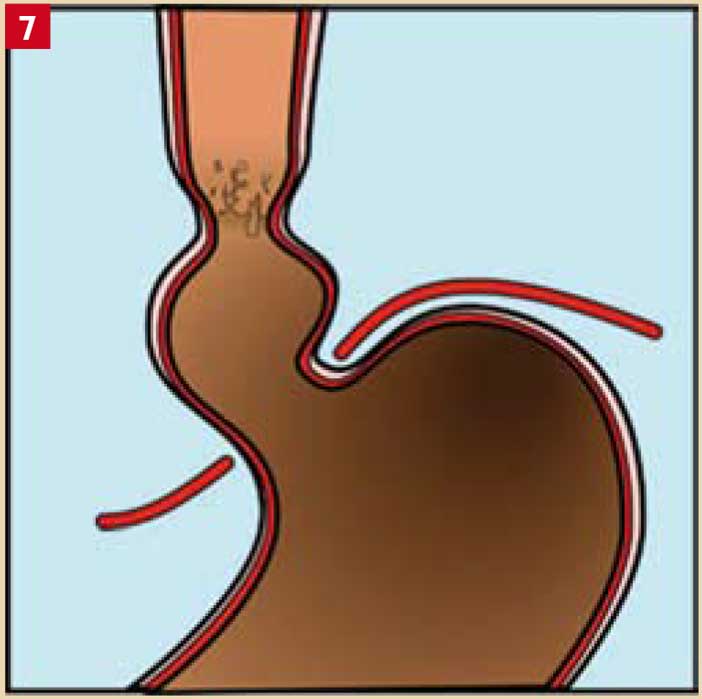
Fig. 7 : reflux gastrooesophagien (RGO). Il est souvent la cause des halitoses d’origine gastrique.
Conclusion
L’halitose est un fléau planétaire car son mode chronique atteint 25 à 40 % de la population mondiale. Elle devrait davantage intéresser la santé publique car les répercussions sociales peuvent être extrêmement handicapantes. Cette maladie continue à être perçue comme honteuse car les personnes qui en sont atteintes n’en parlent pas et se replient sur elles-mêmes. Elle doit être prise à bras le corps par les chirurgiens-dentistes.
Les professions dont la santé de la cavité buccale est l’objet sont les plus qualifiées pour aborder de front le problème avec leurs patients ; ils seront mieux écoutés que l’environnement amical ou familial. Les causes évidentes seront rapidement identifiées par un examen attentif du contenu de la cavité buccale, dents, parodonte et fond de la gorge qui devraient cerner 85 à 90 % des cas. Si aucune cause particulière n’est identifiée pour les 10-15 % des cas, le chirurgien-dentiste orientera son patient soit vers une consultation spécialisée en halitose soit vers un ORL pour une première approche. C’est en procédant par élimination que le corps médical trouvera la cause de l’halitose et offrira la solution recherchée au patient souffrant et désorienté.
Ce texte est dédié à la mémoire du Dr Michel Rugina, ORL à l’Hôpital Américain qui a si soudainement quitté les siens, bien avant l’heure.
Bibliographie
1. Davarpanah M, de Corbière S, Caraman M, Sater S et al. L’halitose. Une approche pluridisciplinaire. Editions CdP, Paris, 2006
2. Davarpanah M, Cymes M. Soyez sur de votre haleine. Marabout Poche, Paris, 2004.
3. Van Steenberghe D. Breath malodor, a step by step approach. Quintessence books, Kopenhagen, 2004.
4. Reingewirtz Y. Halitose et parodontite : Revue de littérature. Journal de Parodontologie et Implantologie orale. 1999 ;18 :27-35.