Les parodontites sont des lésions du parodonte profond, d’étiologie infectieuse, à manifestation inflammatoire entraînant la destruction des tissus de soutien de la dent (Listgarten 1986). Pour comprendre les conditions nécessaires pour déclencher les pertes d’attache, il est nécessaire de s’appuyer sur le modèle infectieux de Socransky qui s’appuie sur 4 conditions devant être réunies :
- Présence de bactéries virulentes.
- Absence de bactéries protectrices
- Défaillances du système immunitaire
- Environnement dento-gingival défavorable
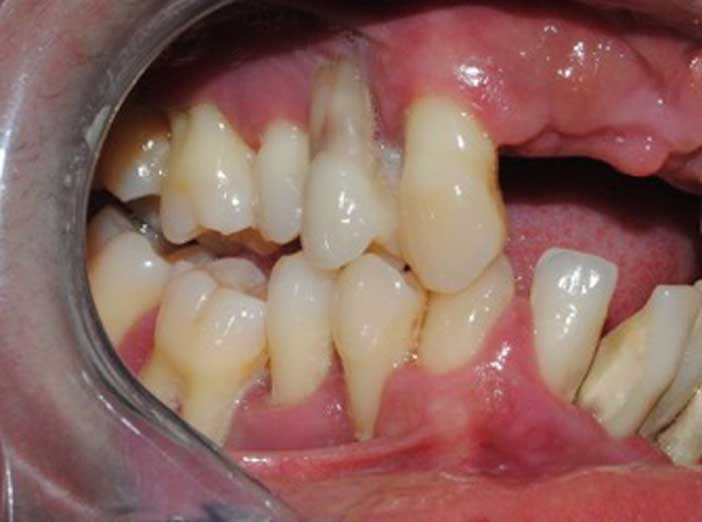
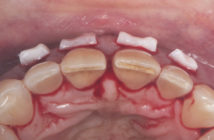
Terrain de parodontite agressive généralisée terminale.
Concernant les défaillances du système immunitaire, Ce dernier est stimulé par certaines bactéries virulentes (par exemple Porphyromonas Gingivalis) et se retourne, dans certaines conditions acquises ou innées (génétique) contre l’hôte infecté en intensifiant la réponse inflammatoire et en «sur-produisant » certaines molécules qui, au lieu d’être protectrices, deviennent alors destructrices En effet, les concentrations abondantes en IL-1 beta, TNFalpha et LPS notamment induisent la production de collagènases et de prostaglandines PGE2 par les fibroblastes gingivaux et jouent par conséquent un rôle majeur dans la pathogénie des pertes d’attaches au cours des parodontites. De plus, cette réaction inflammatoire exacerbée entraine une production importante de dérivés réactifs de l’oxygène, soumettant ainsi les tissus parodontaux à un stress oxydant (Parodontie médicale Charon 2009).
Ainsi, il paraît judicieux d’étudier l’incidence de ces micro-organismes et de cet état inflammatoire chronique sur la santé générale de nos patients. En effet, la prise en charge parodontale étiologique s’inscrit dans une prise en charge globale de nos patients. Cet article aura donc pour objectif de mettre en avant le lien bidirectionnel entre santé générale et santé parodontale.
Pathologies cardiovasculaires
Les infections chroniques peuvent augmenter le risque de maladies cardio-vasculaires. Plusieurs études sont en faveur d’un lien entre les pathologies cardio-vasculaires et les parodontites, mais le niveau de preuve est encore insuffisant 1-2.
Dès 2002, Genco et al. ont évalué l’épidémiologie et les mécanismes possibles liant les maladies parodontales et les maladies cardiaques (3). D’après leur analyse d’articles publiés de 1993 à 2000, chez l’homme et chez l’animal, les infections parodontales constitueraient un facteur de risque modéré de maladies cardiaques. Mais la relation de cause à effet n’est pas connue.
En 2003, Scannapieco et al. ont recensé plus de 1 526 études pour rechercher un lien entre les parodontites, qui sont des affections inflammatoires chroniques, et l’athérosclérose et le risque cardio-vasculaire qui en résultent2. En ne retenant que 31 études scientifiquement validées, ils en sont arrivés aux mêmes conclusions.
Des études plus récentes comme celles de Kapellas et al.4 portant sur 138 sujets ont clairement démontré qu’un patient atteint d’une parodontite traitée et stabilisée présentait moins de risque d’athérosclérose qu’une patient malade.
Il paraît important de mentionner que les travaux de Subramanian et al. en 20135 ont permis de lancer la réflexion sur un lien bidirectionnel entre santé parodontale et maladies cardiovasculaires puisqu’il a été démontré que des patients à risque de pathologies cardiovasculaires bien stabilisés par un traitement hypocholestérolémiant (statines) présentent une diminution de l’inflammation parodontale, probablement via une diminution de l’inflammation extra-artérielle, par exemple au niveau des parodontites.
En 2008, Dietrich et Coll.6 évaluent sur 1203 hommes l’association possible entre parodontites, édentement et pathologies cardiovasculaires et ce sur une période moyenne de 24 ans. En effet, les parodontites sont évaluées cliniquement et radiologiquement par des parodontistes expérimentés tandis que la pression sanguine et les dosages en HDL, triglycérides et glucose sont mesurés, tout en tenant compte de facteurs environnementaux comme le tabac ou l’alcool. A la lecture des résultats, la présence d’une parodontite chronique augmente le risque de pathologies cardiovasculaires chez les hommes les plus jeunes, et ce indépendamment des facteurs de risques cardiovasculaires connus.
En 2013, Dietrich et Coll7 réalisent une méta-analyse afin de déterminer une éventuelle preuve épidémiologique entre parodontite et pathologies cardiovasculaires de type athérosclérotique. Parmi 12 études retenues, il apparaît une preuve de risque augmenté de pathologies cardiovasculaires chez des patients atteints de parodontites néanmoins, il n’y a pas encore de niveau de preuve suffisant pour affirmer le lien direct de cause à effet.
Pathologies ostéo-articulaires
La polyarthrite rhumatoïde, cause la plus fréquente de polyarthrites chroniques, est une pathologie dégénérative inflammatoire chronique caractérisée par une atteinte articulaire souvent bilatérale et symétrique. De par le caractère également inflammatoire des parodontites, de nombreux auteurs se penchent sur un lien potentiel entre les 2 pathologies. En effet, toutes deux induisent une inflammation chronique, une destruction osseuse mais aussi une réponse immunitaire cellulaire et humorale.
En 2005, Ribeiro et Coll.8 étudient l’effet d’une thérapeutique parodontale chez des patients présentant les deux pathologies via un échantillon de 42 patients. Même s’il n’y a pas de différence significative sur l’amélioration de la polyarthrite rhumatoïde, les auteurs constatent qu’une thérapeutique parodontale non chirurgicale influe de manière significative sur la diminution de la vitesse de sédimentation. En 2007, Al-Katma et Coll.9, via une étude portant sur 29 sujets pendant 3 ans, confirment qu’une thérapeutique parodontale d’assainissement non chirurgicale aurait un impact positif sur la diminution des signes et des symptômes de polyarthrite rhumatoïde.
En 2011, Routsias et Coll.10 et Mikuls et Coll. en 201211, étudient le rôle potentiel de Porphyromonas gingivalis dans la polyarthrite rhumatoïde. En effet, Les anticorps antiprotéines citrullinées constituent des facteurs diagnostiques et pronostiques de la polyarthrite rhumatoïde, et sont spécifiques de cette maladie ; néanmoins, certaines bactéries orales comme Porphyromonas gingivalis, possèdent l’enzyme Peptidyl Arginine Deaminase, induisant la citrullinisation de protéines, déclenchant une réaction inflammatoire. Les mécanismes communs à la parodontite et à la polyarthrite rhumatoïde ainsi que Porphyromonas gingivalis joueraient un rôle important dans la rupture de la tolérance immunitaire.
Pathologies respiratoires
En 1999, Scannapieco et Coll.12 établissent quatre mécanismes possibles de contamination des voies respiratoires basses: aspiration oropharyngée, inhalation d’aérosols infectieux, propagation de l’infection depuis des sites voisins et dissémination hématogène à partir de sites extra-pulmonaires (via les voies gastro-intestinales).
En 2006, Azarpazhooh et Coll.13, via une revue de la littérature de plus de 700 articles, confirment que la plaque dentaire constitue un réservoir de pathogènes respiratoires. Un lien est établi entre pneumonie et santé bucco-dentaire défavorable.
Par ailleurs, hygiène et soins bucco-dentaires diminuent de manière significative les risques de pathologies respiratoires chez les personnes fragiles ou âgées.
En 2013, pour Bansal et Coll.14, sinusites et pneumonies peuvent avoir pour étiologie une inhalation de germes comme Streptococcus aureus, Pseudomonas aeruginosa ou encore Porphyromonas gingivalis, confirmant le lien entre pathologies respiratoires et cavité orale.
L’Organisation Mondiale de la Santé (OMS) classe actuellement la broncho-pneumopathie chronique obstructive (BPCO) comme la 5ème cause de mortalité au monde et potentiellement la 3ème d’ici 2020 d’où la nécessité supplémentaire d’avoir une cavité buccale saine.
Diabète de type 2
En 2006, Mealey et Coll.15 proposent une méta-analyse sur une période de 20 ans et couvrant plus de 200 articles afin de répondre aux questions suivantes : « Est ce que le diabète joue un rôle sur le risque de développer une parodontite ? Est ce qu’un terrain de parodontite affecte la physiopathologie du diabète ? Quels sont les mécanismes par lesquels ces deux pathologies interagissent ? Et enfin comment les patients diabétiques atteints de parodontite réagissent-ils aux traitements parodontaux? » Les conclusions de cette analyse établissent les éléments suivants: maladies parodontales et diabète sont des pathologies chroniques liées de par leurs similarités en pathobiologie (particulièrement de par leur caractère inflammatoire). Un patient atteint de diabète présente donc plus de risque de souffrir de parodontites. Concernant l’impact de la parodontite sur le contrôle glycémique, les données montrent une tendance protectrice du traitement parodontal sur le diabète mais ne permettent pas de conclure, faute de niveau de preuve suffisant.
Par ailleurs, depuis 2006, de nombreuses études soulignent l’impact positif d’une santé buccodentaire satisfaisante sur le diabète16-17 et il ressort, malgré certaines données contradictoires liées au type d’étude, au tabagisme etc… qu’une cavité buccale assainie au niveau parodontal présente le même potentiel pour diminuer la concentration sanguine en HbA1c qu’un régime alimentaire ou une activité physique adaptés.
En 2013, Kim et Coll.18, à partir d’une étude portant sur 125 patients atteints de diabète de type 2 explorent la relation entre HbA1c, glycémie à jeun, ancienneté du diabète et gestion personnelle de ce dernier associé au statut parodontal. Il y aurait donc une corrélation significative entre ces éléments qui conforte les travaux précédents.
Dès lors, il paraît plausible d’établir un lien bidirectionnel entre diabète et mauvaise santé bucco-dentaire:
- Les parodontopathies aggravent le diabète en perturbant le métabolisme insulinique (favorisent donc l’hyperglycémie)
- Un diabète non équilibré affecte l’environnement oral par hypersécrétion de cytokines (TNF, IL-1B, IL-6) et formation d’AGEs (produits de glycation avancés entrainant la destruction de fibroblastes et ostéoblastes.)
Syndrômes démentiels
En 2003, Holmes et Coll.19 établissent que les patients présentant un taux élevé de cytokines pro-Inflammatoires (dont TNFα et IL1β) sont plus à risque de déclin cognitif or les pathologies parodontales se caractérisent par un état inflammatoire aigu et/ou chronique impliquant les même cytokines.
En 2007, Stein et Coll.20 sur un échantillon de 144 patients et en 2009 Noble et Al21 sur un échantillon de 2355 participants, établissent un lien entre syndrôme démentiel- Alzheimer et mauvaise santé bucco-dentaire. Cette notion est confirmée en 2012 par Sparks Stein et Coll.22 qui confirment une association entre les Ig G de Porphyromonas gingivalis, (bactérie pathogène des parodontites) et les troubles cognitifs.
Pour Paganini et Coll. 201223, qui ont suivi plus de 5000 patients entre 51 et 102 ans sur 18 ans quant à leurs habitudes de soins dentaires, il y a une plus forte proportion de personnes qui négligent leur cavité buccale parmi celles atteintes de démence ou autres troubles cognitifs.
Cancers des voies aérodigestives supérieures
Les cancers des voies aérodigestives supérieures (VADS) constituent la 5ème cause de cancers le plus fréquent en Europe. Dans 95% des cas, ce sont des carcinomes épidermoïdes diagnostiqués le plus souvent tardivement. L’âge moyen de survenue est de 55 ans mais le tabagisme et l’alcoolisme précoce expliquent qu’aujourd’hui, plus de 25% des cas sont diagnostiqués avant 50 ans.
En se penchant sur les maladies parodontales, Hormia et Coll.24 et Saygun et Coll.25 en 2005 posent les bases d’un lien entre poches parodontales et les infections virales qui sont des facteurs aggravants pour les cancers des VADS (Epstein Barr Virus et Human Papilloma Virus)
En 2006, Karin et Coll. (26) suggèrent une association entre agents infectieux, inflammations chroniques et cancers. Il est communément admis que la cavité buccale peut être une source de foyers infectieux ou d’inflammation ; c’est pourquoi Tezal et Coll., dès 2007 (27) mettent en évidence au travers d’une étude sur 51 sujets, une association possible entre parodontite chronique et risque de survenue de cancer de la langue, et ce indépendamment de l’ethnie, de la consommation de tabac ou autre.
Enfin, via une méta-analyse sur plus de 5000 patients, Wang et Coll. (2013) (28) relient perte de dents et risque de cancer des VADS, indépendamment des autres facteurs de risque comme le tabac et l’alcool.
CONCLUSION
Dans la prise en charge médicale de nos patients, il apparaît clairement que la bouche reste, à tort, séparée du reste du corps humain, minimisant leurs interactions réciproques négatives. Il appartient donc à chaque praticien de sensibiliser ses patients quant à l’importance d’un parodonte sain.
BIBLIOGRAPHIE
1. Desvarieux M, Demmer RT, Rundek T, Boden- Albala B, Jacobs DR, Papapanou PN, et al. (2003). Relationship between periodontal disease, tooth loss, and carotid artery plaque: the Oral Infections and Vascular Disease Epidemiology Study (INVEST). Stroke 2003 ; 34 : 2120-5.
2. Scannapieco FA, Bush RB, Paju S. Associations between periodontal disease and risk for atherosclerosis, cardiovascular disease, and stroke. A systematic review. Ann Periodontol 2003 ; 8 : 38-53.
3. Genco R, Offenbacher S, Beck J. Periodontal disease and cardiovascular disease: epidemiology and possible mechanisms. J Am Dent Assoc 2002 ; 133 : 14S-22S
4. Kapellas K, Maple-Browh LJ, Jamieson LM, Do LG, O’Dea K, Brown A, et al. Effect of periodontal therapy on arterial structure and function among aboriginal Australians: a randomized, controlled trial. Hypertension 2014 ; 64 : 702-8
5. Subramanian S, Emami H, Vucic E, Singh P, Vijayakumar J, Fifer KM, et al. High-dose atorvastatin reduces periodontal inflammation: a novel pleiotropic effect of statins. J Am Coll Cardiol 2013 ; 62 : 2382-91.
6. Dietrich, T., Jimenez, M., Kaye, E. A. K., Vokonas, P. S., & Garcia, R. I. (2008). Age-dependent associations between chronic periodontitis/edentulism and risk of coronary heart disease. Circulation, 117(13), 1668-1674
7. Dietrich, T., Jimenez, M., Kaye, E. A. K., Vokonas, P. S., & Garcia, R. I. (2008). Age-dependent associations between chronic periodontitis/edentulism and risk of coronary heart disease. Circulation, 117(13), 1668-1674.
8. Ribeiro, J., Leao, A., & Novaes, A. B. (2005). Periodontal infection as a possible severity factor for rheumatoid arthritis. Journal of clinical periodontology, 32(4), 412-416.
9. Al-Katma, M. K., Bissada, N. F., Bordeaux, J. M., Sue, J., & Askari, A. D. (2007). Control of periodontal infection reduces the severity of active rheumatoid arthritis. JCR: Journal of Clinical Rheumatology, 13(3), 134-137.
10. Routsias, J. G., Goules, J. D., Goules, A., Charalampakis, G., & Pikazis, D. (2011). Autopathogenic correlation of periodontitis and rheumatoid arthritis. Rheumatology, ker090.
11. Mikuls, T. R., Thiele, G. M., Deane, K. D., Payne, J. B., O’Dell, J. R., Yu, F., … & Norris, J. M. (2012). Porphyromonas gingivalis and disease‐related autoantibodies in individuals at increased risk of rheumatoid arthritis. Arthritis & Rheumatism, 64(11), 3522-3530.




4 commentaires
Merci pour ce bon résumé des interactions entre les parodontites et la santé générale.
Il serait surement intéressant de comparer, pour un groupe significatif de patients guéris, l’état de leur santé générale avant et après leur guérison parodontale.
Cela permettrait de donner plus de signification à ce lien et passer directement à l’action sans crainte, enfin, boucler la boucle.
Guérison étant à notre avis : absence de poches supérieures à 3mm, absence de saignement, flore commensale, absence de cellules inflammatoires à la microscopie et patient autonome sur ses habitudes.
Espérant voir ce genre d’étude bientôt.
Cordialement.
Mark Bonner DMD
Merci de vos observations
Au plaisir
Merci pour votre recherche bibliographique qui met en place la santé buccal
Merci beaucoup pour votre message
Bien confraternellement