L ’élimination du tartre est une des composantes importantes de tous les traitements parodontaux (Fairbrother et Heasman, 2000). Dans l’approche conventionnelle, elle est pratiquée à l’aide de « détartrages profonds » inclus dans le cadre de la préparation initiale. Le détartrage représente probablement l’acte le plus banalisé de la dentisterie, la nomenclature lui ayant conféré un des coefficients le plus bas qui soit en dentisterie.
Les actes de parodontie qui consistent à éliminer le tartre peuvent être comparés à ceux que réalisent les chirurgiens lorsqu’ils éliminent un calcul d’une cavité naturelle (canaux salivaires, vessie, reins, uretères, vésicule, cholédoque). On peut donc assimiler l’élimination du tartre à une « lithotritie »1 ayant pour but de traiter les conséquences de « lithiases infectieuses » du parodonte en agissant avec les mêmes précautions que prennent les chirurgiens pour respecter les tissus qui environnent le calcul.
La lithotritie parodontale est donc un acte délicat, long, nécessitant entraînement et expertise. Lorsqu’elle est réalisée dans les conditions optimales, la lithotritie parodontale est souvent suivie de gains d’attache « spectaculaires » avec le confort que cela entraîne pour le patient.
Pourquoi faut-il éliminer le tartre ?
Il existe trois raisons principales qui justifient l’élimination – la plus totale possible – du tartre :
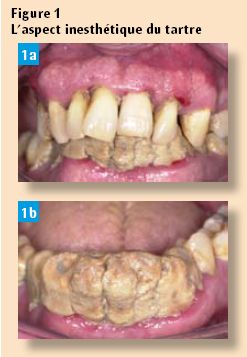
Esthétique
La plupart des patients demandent « un petit détartrage » pour des raisons cosmétiques (Figures 1).
Obstacles aux gains d’attache
Les spicules de tartre sous-gingivaux sont le plus fréquement des obstacles à la fermeture des poches parodontales (Figure 2).
Environnement favorable aux bactéries virulentes
Les anfractuosités du tartre créent des conditions pour que certaines bactéries anaérobies puissent proliférer (Schroeder, 1969). De plus, le tartre peut oblitérer l’entrée des lésions et créer un environnement anaérobie.
Peut-on éliminer la totalité du tartre ?
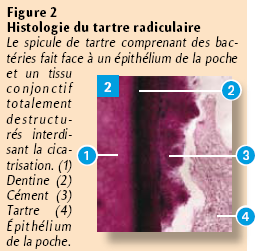 Au niveau microscopique, l’élimination totale du tartre est très souvent impossible quelle que soit la technique employée (avec ou sans chirurgie, manuelle, sonique ou ultrasonique) même si le tartre sous-gingival n’occupe – en moyenne – que moins de la moitié de la surface de la racine (Sherman, Hutchens et Jewson, 1990b).
Au niveau microscopique, l’élimination totale du tartre est très souvent impossible quelle que soit la technique employée (avec ou sans chirurgie, manuelle, sonique ou ultrasonique) même si le tartre sous-gingival n’occupe – en moyenne – que moins de la moitié de la surface de la racine (Sherman, Hutchens et Jewson, 1990b).
On peut donc poser deux questions d’ordre pratique :
- Pourquoi instrumenter la totalité de la racine si une partie seulement est occupée par le tartre ?
- Pourquoi instrumenter la partie radiculaire située sous l’attache épithélio-conjonctive alors qu’il n’existe pas de tartre à ce niveau ?
La zone située sous le tartre le plus apical ne doit pas – délibérément – être instrumentée avec vigueur (Claffey, 1994). Il est également recommandé de ne pas instrumenter l’attache conjonctive pour éviter une prolifération apicale de l’épithélium de jonction (Bowers et coll., 1989).
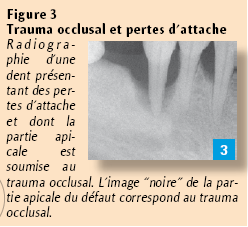 Lorsque le parodonte est infecté, le tissu osseux est déminéralisé sans nécessairement que les fibres soient détachées de la surface radiculaire. D’autre part, la partie osseuse d’une lésion parodontale soumise à un trauma occlusal apparaît, à la radiographie, comme déminéralisée pouvant surestimer la quantité réelle de pertes tissulaires (Figure 3).
Lorsque le parodonte est infecté, le tissu osseux est déminéralisé sans nécessairement que les fibres soient détachées de la surface radiculaire. D’autre part, la partie osseuse d’une lésion parodontale soumise à un trauma occlusal apparaît, à la radiographie, comme déminéralisée pouvant surestimer la quantité réelle de pertes tissulaires (Figure 3).
Autrement dit, une image radiologique de déminéralisation n’est pas nécessairement synonyme de pertes d’attache.
Quand faut-il éliminer le tartre ?
L’abord mécanique des lésions parodontales peut se faire en toute sécurité lorsque les lésions sont cliniquement et micro-biologiquement au repos, c’est-à-dire lorsque l’infection parodontale est sous contrôle.
Comment aborder les lésions parodontales ?
L’attitude en parodontie est comparable à celle des endodontistes :
- Doit-on obturer un canal infecté ?
- Opère-t-on toutes les lésions apicales sous le prétexte qu’elles sont volumineuses ?
- N’avons-nous pas compris qu’en supprimant l’infection pulpaire, le péri-apex pouvait cicatriser ?
L’approche stratifiée
L’approche conventionnelle conseille d’effectuer les détartrages par « quadrants ». Une attitude différente consiste également à éliminer progressivement le tartre mais sur la totalité des sites en procédant de la superficie à la profondeur et en privilégiant les espaces interproximaux (Quirynen et coll., 1999) (Charon et Mouton, 2003).
Cette attitude permet de donner à la cicatrisation une cinétique équivalente de tous les sites sans se laisser surprendre par un éventuel « accident » dans un quadrant pendant que nous en instrumentons un autre.
Effets microbiologiques
Le détartrage provoque des modifications sensibles – mais transitoires – de la flore supra et sousgingivale (Greenstein, 1992).
Ces modifications sont dues – en partie – à l’effet mécanique d’évacuation des bactéries lors de l’instrumentation. De plus, intervenir avec un détartreur au sein d’une lésion bouleverse le potentiel d’oxydo-réduction par apport massif d’oxygène de telle sorte que les bactéries anaérobies se trouvent transitoirement dans un environnement moins favorable à leur croissance.
Cependant, tous les sujets ne répondent pas efficacement au détartrage/surfaçage conventionnel. Cela peut être dû à ce que les parodontites ne sont pas toutes de même nature et que l’hygiène dentaire n’est peut-être pas le meilleur moyen de traiter les patients sévèrement infectés (Haffajee et coll., 1997).
Si des bactéries virulentes sous-gingivales sont laissées après détartrage, le temps de recolonisation est de quelques semaines à quelques mois (Mousques, Listgarten et Philipps, 1980). Dans ce cas, la flore qui se réinstalle dans l’espace dentogingival après détartrage est identique à celle de départ, quelles que soient la technique choisie et la profondeur de la poche (Pedrazzoli et coll., 1991).
 Effets cliniques
Effets cliniques
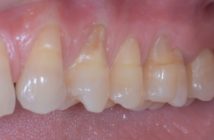
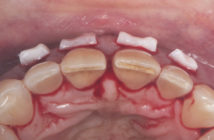
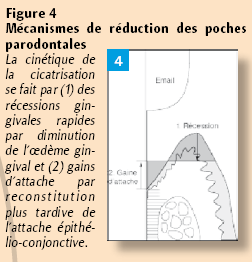
L’élimination du tartre produit – en général – une diminution de la profondeur des poches par la combinaison de deux phénomènes : les récessions gingivales associées aux gains d’attache (Figure 4).
Les récessions gingivales
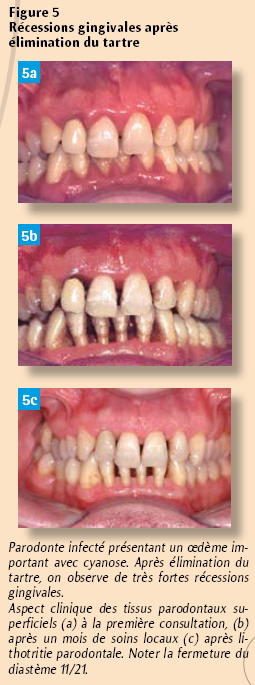
Ces récessions gingivales sont d’autant plus importantes, qu’avant thérapeutique, le parodonte superficiel est oedématié, hypervascularisé, tuméfié et cyanosé.
Ces rétractions de la gencive libre vont entraîner ipso facto une réduction de la profondeur des poches sans qu’il y ait nécessairement et immédiatement gains d’attache. Plus les pertes d’attache sont sévères, plus les récessions gingivales sont en général importantes. Notons qu’elles se produisent surtout durant le premier mois de soins locaux (Figures 5).
Les gains d’attache
Les gains d’attache clinique sont proportionnels à la profondeur de la lésion. Autrement dit, plus la lésion est profonde, plus les gains d’attache sont importants (Greenstein, 1992). Par ailleurs, il n’existe pas de profondeur de poche au-delà de laquelle les traitements non chirurgicaux seraient incapables de gagner de l’attache (Lindhe et coll., 1982).
Après lithotritie parodontale non chirurgicale, les gains d’attache se traduisent, à terme, par :
- Une diminution et l’arrêt de la mobilité dentaire (si absence de trauma occlusal),
- Une texture plus ferme du tissu gingival,
- Une amélioration des images radiologiques,
- Une moins grande pénétration de la sonde dans la lésion,
- Une sensation de force et de confort de la part du patient.
L’élimination du tartre entraîne une amélioration de la situation clinique dans les trois ou quatre semaines qui suivent. Mais, si la flore n’est pas compatible avec la santé parodontale, les paramètres cliniques retournent en trois mois aux valeurs observées avant traitement.
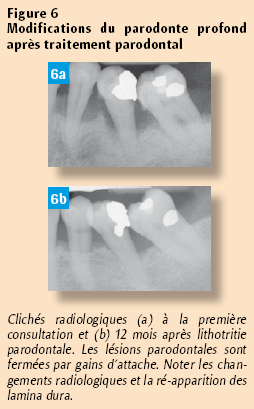
La lithotritie parodontale réalisée en présence d’une flore compatible avec la santé parodontale donne d’excellents résultats cliniques dans un délai moyen de six à douze mois après le début du traitement (Figures 6).
Effets sur les tissus épithélio-conjonctifs
La cicatrisation des lésions parodontales peut se faire par l’une ou plusieurs situations suivantes :
- Une attache épithélio-conjonctive de dimensions et de structures classiques,
- Un long épithélium de jonction,
- Une cicatrisation totale ou partielle des tissus parodontaux profonds.
La cicatrisation des lésions parodontales se fait sur la base d’une compétition entre la vitesse à laquelle migrent les cellules des tissus conjonctifs (fibroblastes) et celle à laquelle migrent les cellules épithéliales (épithélium de jonction et sulculaire). Ces dernières sont plus rapides que les premières et une nouvelle attache épithéliale est rapidement réalisée en moins de deux semaines.
En revanche, il faut attendre plusieurs mois avant que le pourcentage de fibroblastes ne retourne à des valeurs normales (Listgarten, Lindhe et Helden, 1978) (Rabbani, Ash et Caffesse, 1981). Par ailleurs, la nature de l’infiltrat leucocytaire se modifie au cours des mois qui suivent l’élimination du tartre.
Matériel nécessaire à la lithotritie parodontale
a. Les instruments ultrasoniques
Les inserts des détartreurs ultrasoniques vibrent à des fréquences variant de 20 à 30KHz (20 000 à 40 000 cycles par seconde) en produisant un effet de martèlement. Les oscillations sont générées par un courant électrique alternatif ou une piezoélectricité.
Cependant, les détartreurs ultrasoniques sont, à nos yeux, les moins adaptés des instruments pour les patients atteints de pertes d’attache sévères car ils peuvent supprimer jusqu’à 250μm de substance dentaire (épaisseur du cément).
b. Les instruments soniques
Les détartreurs soniques fonctionnent à l’aide d’air comprimé faisant vibrer un insert. Comme la turbine, ils peuvent être facilement branchés sur le cordon de l’équipement. La fréquence de vibration varie de 2 à 6KHz (2 000 à 6 000 cycles Paro par seconde), ce qui est considérablement plus bas que celle des détartreurs ultrasoniques. Les inserts sont adaptés pour permettre l’accès à un grand nombre de lésions parodontales, des plus simples aux plus tortueuses.
Nous appuyant sur l’expérience clinique, nous avons choisi d’utiliser les instruments de W.H.™ et de Kavo® (SonicFlex™).
c. Les instruments à mains
Les instruments manuels ont longtemps été considérés comme supérieurs aux détartreurs ultrasoniques pour créer des surfaces lisses et dures (Garett, 1977). Cependant, la cicatrisation des lésions parodontales n’est que peu dépendante de la rugosité de la surface radiculaire (Landry et coll., 1999).
 d. Les fibres optiques
d. Les fibres optiques
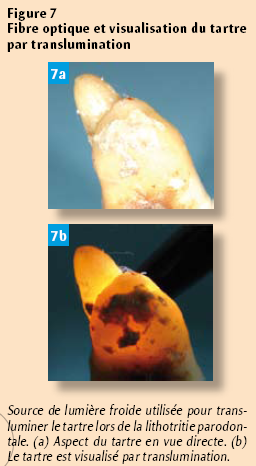
En utilisant la sonde pour détecter la présence de tartre, on a tort une fois sur deux quand on dit qu’il n’en reste plus (Sherman et coll., 1990a et 1990b). L’utilisation d’une lumière froide et d’une fibre optique permet de transluminer la surface dentaire et de visualiser les spicules de tartre difficiles à localiser à l’oeil nu (Figures 7).
e. Les binoculaires
L’utilisation de loupes binoculaires améliore considérablement le pouvoir de définition compte tenu de la taille quelquefois très faible des spicules de tartre.
Le protocole de lithotritie parodontale
Un mois (minimum) après la première consultation, si le patient a été observant, le praticien abordera les lésions parodontales dans des conditions optimales de confort, d’efficacité et de sécurité.
a. Entretien au bureau
Il est essentiel d’écouter le patient de chaque côté d’un bureau. Il s’agira donc de :
- s’enquérir des améliorations que le patient a pu percevoir par rapport à la première consultation,
- D’écouter avec empathie les problèmes rencontrés au cours des soins locaux.
- Avant les soins, le praticien donnera toutes les explications nécessaires sur le « pourquoi » et le « comment » de la séance de lithotritie parodontale.
b. Examen clinique
Il est essentiel d’enregistrer, grâce à la macrophotographie, les nouvelles données cliniques et les comparer avec celles photographiées à la première consultation. On s’assurera également que l’halitose et les suppurations ont disparu. Un prélèvement de plaque sous-gingivale examiné sous le microscope est conseillé afin de confirmer que les lésions parodontales sont microbiologiquement au repos.
c. Désinfection et préparation des lésions à traiter
Afin de s’assurer que les lésions sont cliniquement au repos, on passera préalablement, à la jonction dento-gingivale, un mélange antiseptique d’eau oxygénée, de bicarbonate de soude et de chlorhexidine à l’aide d’un stimulateur Butler™ suivi d’une irrigation avec une solution d’eau oxygénée puis de chlorhexidine.
On repérera les lésions qui saignent au passage du stimulateur, ce qui est rare lorsque le patient a suivi les prescriptions.
d. Lithotritie de la totalité des sites
On abordera la totalité des lésions, de la superficie à la profondeur, en transluminant les dents à l’aide de la fibre optique et en utilisant les binoculaires. Les espaces interproximaux seront traités en priorité.
La séquence est la suivante :
- Repérer le spicule de tartre à éliminer,
- Poser l’instrument à la jonction tartre/dent,
- Activer l’instrument,
- Attendre que le spicule de tartre se détache de la racine,
- Procéder vers un autre spicule de tartre.
- Irrigation avec des antiseptiques
Après avoir éliminé le plus de tartre possible, on procèdera à l’irrigation de l’entrée des lésions avec une solution d’eau oxygénée puis de chlorhexidine. Il n’est souvent pas nécessaire de réaliser une anesthésie. Ceci est peut-être dû à ce que les tubuli dentinaires sont minéralisés par l’utilisation d’eau oxygénée et de bicarbonate de soude.
f. Polissage des colorations dues à la chlorhexidine
Ce polissage se fera préférentiellement avec un aéropolisseur.
La disparition de l’oedème gingival et l’élimination des spicules de tartre modifient l’anatomie des embrasures et par conséquent la taille et la forme des brossettes à utiliser par le patient. Lorsque les lésions sont au repos, on peut également diminuer la posologie de la chlorhexidine afin de diminuer les colorations (diminution de la fréquence et/ou de la concentration).
À ce stade, si des soins sont à réaliser, ils pourront l’être à la condition que la jonction dento-gingivale soit respectée.
h. Entretien au bureau
Avant de libérer le patient, il est conseillé d’avoir un court entretien au bureau pour les raisons suivantes :
- Confirmer des améliorations par rapport aux observations de la première consultation,
- Indiquer au patient que la séance a été facile par rapport à ce qu’elle aurait été si on avait “détartré” d’emblée à la première consultation.
Les séances de lithotritie sont répétées autant de fois que nécessaire à un mois (minimum) d’intervalle en appréciant chaque fois les gains d’attache (et donc la fermeture des poches). On progressera de plus en plus apicalement jusqu’à ce que la lithotritie parodontale non chirurgicale ait fermé toutes les lésions.
Le respect du cément
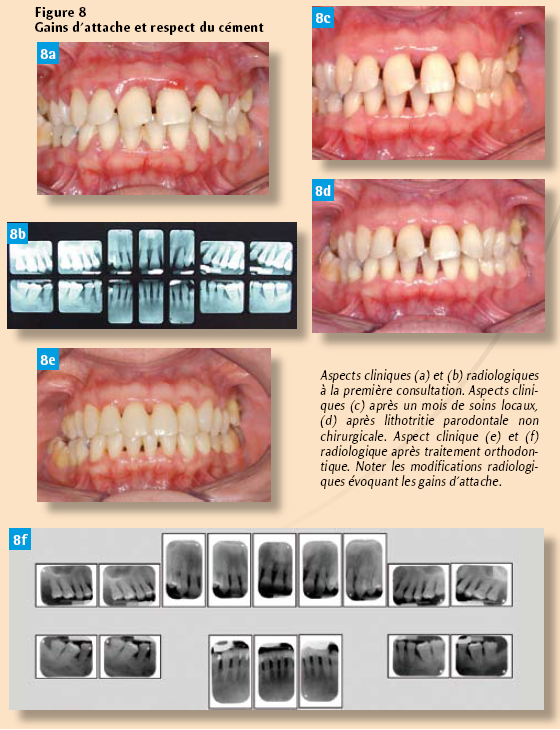
Les lésions parodontales peuvent regagner de l’attache après élimination du tartre sans recourir nécessairement à l’élimination du cément par surfaçage (Nyman et coll., 1988) (Figures 8).
D’autre part, le surfaçage vigoureux entraîne des effets « iatrogènes » :
Sensibilités dentinaires
Il apparaît souvent de très désagréables sensibilités dentinaires.
Les caries radiculaires
Les caries radiculaires représentent l’une des complications majeures des traitements parodontaux conventionnels.
Les pertes de substance
Les surfaçages répétés tous les trois mois entraînent des pertes de substance.
Conclusions
Les lésions parodontales peuvent être approchées autrement que d’emblée avec une vigueur exagérée. En effet, si les lésions sont au repos et abordées avec respect des tissus parodontaux, le patient et le praticien auront toutes les satisfactions attendues du traitement parodontal.
Drs Jacques Charon*, Frédéric Joachim*, Sébastien Dujardin** et Joël Beaulieu***.
* : Parodontiste, Lille, France
** : Post Graduate in Periodontics, Temple University, Philadelphia, USA
*** : Chirurgien-dentiste, Laval, Québec
Références bibliographiques
1. Bowers G.M., Chadroff B., Carnavale R., Mellonig J., Corio J. Emerson J., Stevens M. et Romberg E. – Histologic evaluation of new attachment apparatus formation in humans – Part III. J Periodontol 60 : 683 – 693, 1989
2. Charon J. et Mouton C. – Parodontie Médicale – Editions CDP, Paris, 2003
3. Claffey N. – Comment gagner ou perdre de l’attache parodontale. J Parodontol 13 : 193 – 202, 1994
4. Fairbrother K.J. et Heasman P.A. – Anticalculus agents. J Clin Periodontol 27 : 285 – 301, 2000
5. Garett J.S. – Root planing : A perspective. J Periodontol 48 : 553 – 557, 1977
6. Greenstein G. – Periodontal response to mechanical non-surgical therapy : A review. J Periodontol 63 : 118 – 130, 1992
7. Haffajee A.D., Cugini M.A., Dibart S., Smith C., Kent R.L. et Socransky S. – The effect of SRP on the clinical and microbiological parameters of periodontal diseases. J Clin Periodontol 24 : 324 – 334, 1997
8. Landry C., Long B., Singer D. et Senthilselvan A. – Comparison between a short and a conventional blade periodontal curet : an in vitro study. J Clin Periodontol 26 : 548 – 551, 1999
9. Lindhe J., Socransky S., Nyman S., Haffajee A. et Westfelt E. – «Critical probing depths» in periodontal therapy. J Clin Periodontol 9 : 323 – 336, 1982
10. Listgarten M.A., Lindhe J. et Hellden L. – Effect of tetracycline and/or scaling on human periodontal disease. Clinical, microbiological and histological observations. J Clin Periodontol 5 : 246 – 271, 1978
11. Mousques T., Listgarten M.A. et Philipps R.W. – Effect of scaling et root planing on the composition of humans subgingival microbial flora. J Periodont Res 15 : 144 – 151, 1980
12. Nyman S., Westfelt E., Sarhed G. et Karring T. – Role of diseased root cementum in healing following treatment of periodontal disease. J Clin Periodontol 15 : 464 – 468, 1988
13. Pedrazzoli V., Kilian M., Karring T. et Kirkegaard E. – Effects of surgical and non-surgical periodontal treatment on periodontal status and subgingival microbiota. J Clin Periodontol 18 : 598 – 604, 1991
14. Quirynen M., Mongardini C., Pauwels M., Bollen C.M., Van Eldere J. et van Steenberghe D. – One stage full versus partial-mouth disinfection in the treatment of chronic adult or generalized early-onset periodontitis. II. Long-term impact on microbial load. J Periodontol 70 : 646 – 656, 1999
15. Rabbani G.M., Ash M.M. et Caffesse R.G. – The effectiveness of subgingival scaling and root planing in calculus removal. J Periodontol 52 : 119 – 123, 1981
16. Schroeder H.E. – Formation and inhibition of dental calculus. Berne : Hans Huber Publishers, 1969
17. Sherman P.R., Hutchens L.H. Jr., Jewson L.G., Moriarty J.M., Greco G.W. et McFall W.T. Jr. – The effectiveness of subgingival scaling and root planing. I. Clinical detection of residual calculus. J Periodontol 61 : 3 – 8, 1990a
18. Sherman P.R., Hutchens L.H. Jr. et Jewson L.G. – The effectiveness of subgingival scaling and root planing. II. Clinical responses related to residual calculus. J Periodontol 61 : 9 – 15, 1990b